-
Hintergrund der Erfindung
-
Gebiet der Erfindung
-
Die
vorliegende Erfindung betrifft bestimmte 3-(4-Amidopyrrol-2-ylmethyliden)-2-indolinonderivate,
die die Aktivität
von Proteinkinasen („PK's") modulieren. Die Verbindungen dieser
Erfindung sind daher bei der Behandlung von Störungen, die mit einer abnormalen
PK-Aktivität
in Zusammenhang stehen, verwendbar. Pharmazeutische Zusammensetzung,
die diese Verbindungen umfassen, die Verwendung von pharmazeutischen Zusammensetzungen,
die diese Verbindungen für
die Herstellung eines Medikamentes zur Behandlung und zum Verhindern
von Erkrankungen umfassen, und Verfahren zur Herstellung dieser
Verbindungen sind ebenfalls offenbart.
-
Stand der Technik
-
PK's sind Enzyme, die
die Phosphorylierung von Hydroxy-Gruppen
an Tyrosin-, Serin- und Threoninresten von Proteinen katalysieren.
Die Konsequenzen dieser scheinbar einfachen Aktivität sind erstaunlich; Zellwachstum,
Differenzierung und Proliferation, d.h., nahezu alle Aspekte des
Zelllebens hängen
auf die eine oder die andere Art von der PK-Aktivität ab. Die
PK-Aktivität
ist mit einer Menge von Erkrankungen, die sich von relativ nicht
lebensbedrohlichen Erkrankungen, wie zum Beispiel Psoriasis, bis
zu extrem virulenten Erkrankungen, wie zum Beispiel Glioblastom
(Gehirnkrebs), erstrecken, in Zusammenhang gebracht worden.
-
Die
PK's können auf
geeignete Weise auf zwei Klassen reduziert werden, die Protein-Tyrosinkinasen (PTK's) und die Serin-Threoninkinasen
(STK's).
-
Einer
der Hauptaspekte der PTK-Aktivität
ist ihr Verhältnis
zu Wachstumsfaktorrezeptoren. Wachstumsfaktorrezeptoren sind Zelloberflächenproteine.
Wenn sie durch einen Wachstumfaktorliganden gebunden werden, werden
Wachstumsfaktorrezeptoren in eine aktive Form umgewandelt, die mit
Proteinen auf der Innenseite der Zellmembran wechselwirkt. Dies
führt zur
Phosphorylierung von Tyrosin-Resten des Rezeptors und anderer Proteine
und zur Bildung von Komplexen innerhalb der Zelle mit einer Vielfalt
von cytoplasmatischen Signalmolekülen die wiederum zahlreiche
zelluläre
Reaktionen auslösen,
wie zum Beispiel die Zellteilung (Proliferation), Zelldifferenzierung,
Zellwachstum, Expression von metabolischen Effekten auf die extrazelluläre Mikroumgebung,
etc. Für
eine vollständigere
Diskussion siehe Schlessinger und Ullrich, Neuron, 9: 303–391 (1992),
der hierin einschließlich
aller Zeichnungen aufgenommen wird, als ob er hier vollständig dargestellt
würde.
-
Wachstumsfaktorrezeptoren
mit PTK-Aktivität
sind als Rezeptor-Tyrosinkinasen („RTK's")
bekannt. Sie umfassen eine große
Familie von Transmembranrezeptoren mit verschiedenartiger biologischer
Aktivität. Derzeit
sind wenigstens neunzehn (19) verschiedene RTK-Subfamilien identifiziert
worden. Ein Beispiel für
sie ist die Subfamilie, die als „HER"-RTK's
bezeichnet wird, und die EGFR (epithelialer Wachstumsfaktorrezeptor) HER2,
HER3 und HER4 einschließt.
Diese RTK's bestehen
aus einer extrazellulären,
glycosylierten ligandenbindenden Domäne, einer Transmembrandomäne und einer
intrazellulären
cytoplasmatischen, katalytischen Domäne, die Tyrosin-Reste an Proteinen
phosphorylieren kann.
-
Eine
andere RTK-Unterfamilie besteht aus dem Insulinrezeptor (IR), dem
insulinähnlichen
Wachstumsfaktor I Rezeptor (IGF-1R) und dem Insulinrezeptor verwandten
Rezeptor (IRR). IR und IGF-1R interagieren mit Insulin, IGF-I und
IGF-II, um ein Heterotetramer aus zwei vollständig extrazellulären, glycosylierten α-Untereinheiten
und zwei β-Untereinheiten,
die die Zellmembran überwinden,
und die die Tyrosinkinasedomäne
enthalten, auszubilden.
-
Eine
dritte RTK-Unterfamilie wird als Plättchenwachstumsfaktorrezeptor
(Platelet Derived Growth Factor Receptor) („PDGFR")-Gruppe bezeichnet, die PDGFRα, PDGFRβ, CSFIR,
c-kit und c-fms einschließt.
Diese Rezeptoren bestehen aus glycosilierten extrazellulären Domänen, die
aus einer variablen Anzahl von immunoglobulinähnlichen Schleifen zusammengesetzt
sind, und einer intrazellulären
Domäne,
wobei die Tyrosinkinasedomäne
durch nichtverwandte Aminosäuresequenzen
unterbrochen wird.
-
Eine
andere Gruppe, die aufgrund ihrer Ähnlichkeit zur PDGFR-Unterfamilie
manchmal in die spätere Gruppe
subsumiert wird, ist die Fetus-Leberkinase (fetus liver kinase)
(„flk")-Rezeptorunterfamilie. Man glaubt, dass
diese Gruppe aus der Kinase Insert Domain-Receptor Fetal Liver Kinase-1
(KDR/FLK-1, VEGF-R2), flk-1R, flk-4 und der fms-ähnlichen Tyrosinkinase 1 (flt-1)
zusammengesetzt ist.
-
Ein
weiteres Mitglied der Tyrosinkinase-Wachstumsfaktorrezeptorfamilie ist die
Fibroblastenwachstumsfaktor („FGF)-Rezeptoruntergruppe.
Diese Gruppe besteht aus vier Rezeptoren, FGFR1-4, und sieben Liganden,
FGF1-7. Obwohl sie zum jetzigen Zeitpunkt noch nicht genau definiert
sind, scheint es, dass die Rezeptoren aus einer glycosilierten extrazellulären Domäne, die
eine variable Anzahl von Immunoglobulin ähnlichen Schleifen enthält, und
eine intrazellulären
Domäne,
in der die Tyrosinkinasesequenz durch Bereiche mit nichtverwandten
Aminosäuresequenzen
unterbrochen ist, bestehen.
-
Ein
noch anderes Mitglied der Tyrosinkinasewachstumsfaktor-Rezeptorfamilie
ist die vaskuläre
Endothel-Wachstumsfaktor („VEGF")-Rezeptor-Untergruppe. VEGF
ist ein dem PDGF ähnliches
dimeres Glycoprotein, das jedoch unterschiedliche biologische Funktionen
und Zielzellspezifität
in vivo aufweist. Man glaubt besonders, dass VEGF eine wichtige
Rolle bei der Vaskulogenese und Angiogenese spielt.
-
Eine
vollständigere
Auflistung der bekannten RTK-Unterfamilien
wird von Plowman et al., DN&P,
7 (6): 334–339
(1994) beschrieben, der hiermit einschließlich aller Zeichnungen hierin
aufgenommen wird, als ob er hier vollständig dargestellt würde.
-
Zusätzlich zu
den RTK's gibt es
auch eine Familie aus vollständig
intrazellulären
PTK's, genannt „Nichtrezeptor-Tyrosinkinasen" oder "zelluläre Tyrosinkinasen". Die letztere Bezeichnung,
abgekürzt „CTK", wird im Folgenden
verwendet. CTK's
enthalten keine extrazellulären
und Transmembrandomänen.
Derzeit sind über
24 CTK's in 11 Unterfamilien
(Scr, Frk, Btk, Csk, Abl, Zap70, Fes, Fps, Fak, Jak und Ack) identifiziert worden.
Die Scr-Unterfamilie scheint bisher die größte Gruppe an CTK's zu sein und schließt Src,
Yes, Fyn, Lyn, Lck, Blk, Hck, Fgr und Yrk ein. Für eine detailliertere Diskussion
der CTK's, siehe
Bolen, Oncogene, 8: 2025–2031
(1993), der hiermit hierin einschließlich aller Zeichnungen aufgenommen
wird, als ob er vollständig hier
dargestellt würde.
-
Die
Serin/Threonin-Kinasen, STK's,
wie die CTK's, sind
vornehmlich intrazellulär,
obwohl es einige Rezeptorkinasen des STK-Typs gibt. STK's sind die gebräuchlichsten
der cytosolischen Kinasen; d.h., Kinasen die ihre Funktion in einem
anderen Teil des Cytoplasmas als dem cytoplasmatischen Organellen
und dem Cytoskelett ausführen.
Das Cytosol ist der Bereich innerhalb der Zelle, in dem ein Großteil der
intermediären
metabolischen und biosynthetischen Aktivität der Zelle zu finden ist;
z.B. werden die Proteine an Ribosomen im Cytosol synthetisiert.
-
RTK's, CTK's und STK's stehen alle mit
pathogenischen Zuständen
in einer Zelle, einschließlich,
besonders bedeutsam, Krebs, im Zusammenhang. Andere pathogenische
Zustände,
die mit PTK's im
Zusammenhang stehen, schließen,
ohne Begrenzung, Psoriasis, Leberzirrhose, Diabetes, Angiogenese,
Restenose, Augenerkrankungen, rheumatoide Arthritis und andere entzündliche
Störungen,
immunologische Störungen, wie
zum Beispiel eine Autoimmunerkrankung, eine Herz-Kreislauf-Erkrankung,
wie zum Beispiel Atherosklerose und eine Vielzahl von Nierenerkrankungen
ein.
-
In
Bezug auf Krebs beziehen sich zwei der Haupthypothesen, die zur
Erklärung
der exzessiven zellulären
Proliferation, die die Tumorentwicklung antreibt, aufgestellt wurden,
auf Funktionen, die bekanntermaßen durch
PK reguliert werden. Zumindest ist vorgeschlagen worden, dass sich
das maligne Zellwachstum aus einem Zusammenbruch des Mechanismus
ergibt, der die Zellteilung und/oder Differenzierung kontrolliert.
Es ist gezeigt worden, dass die Proteinprodukte mehrerer Proto-Onkogene
in den Signaltransduktionswegen, die das Zellwachstum und die Differenzierung
regulieren, involviert sind. Diese Proteinprodukte der Proto-Onkogene
schließen
die extrazellulären
Wachstumsfaktoren, die transmembranen Wachstumsfaktor-PTK-Rezeptoren
(RTK's), cytoplasmatische
PTK's (CTK's) und cytosolische
STK's, wie weiter
oben diskutiert, ein.
-
Im
Hinblick auf die offensichtliche Verbindung zwischen PK-verwandten
zellulären
Aktivitäten
und einer großen
Vielzahl von humanen Störungen, überrascht
es nicht, dass große
Anstrengungen in einem Ansatz unternommen wurden, um Wege zu identifizieren,
um die PK-Aktivität
zu modulieren. Einige dieser Bemühungen
involvieren biomimetische Ansätze,
die große
Moleküle
verwenden, die nach dem Vorbild derer gestaltet sind, die in den
tatsächlichen
zellulären
Prozessen involviert sind (z.B. mutante Liganden (U.S. Anm. Nr. 4,966,849);
lösliche
Rezeptoren und Antikörper
(Anm. Nr. WO 94/10202, Kendall und Thomas, Proc. Nat'l Acad. Sci., 90:
10705–09
(1994), Kim, et al., Nature, 362: 841–844 (1993)); RNA-Liganden
(Jelinek, et al., Biochemistry, 33: 10450–56); Takano, et al., Mol.
Bio. Cell 4: 358A (1993); Kinsella, et al., Exp. Cell Res. 199: 56–62 (1992);
Wright, et al., J. Cellular Phys., 152: 448–57) und Tyrosinkinaseinhibitoren
(WO 94/03427; WO 92/21660; WO 91/15495; WO 94/14808; U.S. Pat. Nr.
5,330,992; Mariani, et al., Proc. Am. Assoc. Cancer Res., 35: 2268
(1994)).
-
Zusätzlich zum
oben genannten, sind Versuche vorgenommen worden, um kleine Moleküle zu identifizieren,
die als PK-Inhibitoren
agieren. Zum Beispiel sind bis-monocyclische, bicyclische und heterocyclische Arylverbindungen
(PCT WO 92/20642), Vinylenazaindolderivate (PCT WO 94/14808) und
1-Cyclopropyl-4-Pyridylchinolone (U.S. Pat. Nr. 5,330,992) als Tyrosinkinaseinhibitoren
beschrieben worden. Styrylverbindungen (U.S. Pat. Nr. 5,217,999),
Styrylsubstituierte Pyridyl-Verbindungen (U.S. Pat. Nr. 5,302,606),
Chinazolinderivate (EP Anm. Nr. 0 566 266 A1), Selenaindole und
Selenide (PCT WO 94/03427), tricyclische polyhydroxyle Verbindungen
(PCT WO 92/21660) und Benzylphosphonsäureverbindungen (PCT WO 91/15495)
alle als PTK-Inhibitoren, die für
die Behandlung von Krebs verwendbar sind, beschrieben worden.
-
Darüber hinaus
sind tricyclische 4,5-Azolooxindole als Inhibitoren der Cyclin-abhängigen Kinasen (PCT
WO 00/035920) beschrieben worden.
-
3' substituierte Indolin-2-one
wurden als neue Klasse von Tyrosinkinaseinhibitoren beschrieben,
die sich sehr selektiv gegen verschiedene Rezeptor-Tyrosinkinasen
zeigen, und es wurde vermutet, dass sie eine spezifische chemische
Hauptrolle bei der Entwicklung von RTK-spezifischen Arzneimitteln
mit breiter Anwendung für
die Behandlung von humanen Erkrankungen spielen würden (Sun
et al., J. Med. Chem. 41 (14): 2588–2603 (1998)).
-
Zusammenfassung der Erfindung
-
Die
vorliegende Erfindung betrifft bestimmte 3-(4-Amidopyrrol-2-ylmethyliden)-2-Indolinonderivate,
die eine PK-modulierende
Fähigkeit
zeigen und daher für
die Behandlung von Erkrankungen, die mit einer abnormalen PK-Aktivität in Verbindung
stehen, verwendbar sind.
-
Eine
Ausführungsform
dieser Erfindung ist eine Verbindung der Formel (I):
wobei
R
1 aus der Gruppe, die aus Wasserstoff, Halo,
C
1-C
10 Alkyl, C
1-C
4 Haloalkoxy,
C
3-C
8 monocyclischem
Cycloalkyl, [5,6]- oder [6,6]-fusioniertem bicyclischem Cycloalkyl,
Adamantyl, einer 5–9
gliedrigen heteroalicyclischen Gruppe, die 1 oder 2 Heteroatome
besitzt, die aus N, O oder -S(O)
n ausgewählt werden,
wobei n = 0–2
ist, Hydroxy, C
1-C
10 Alkoxy,
unsubstituiertem C
3-C
8 Cycloalkoxy,
-C(O)-R
8, -NR
9R
10 und -C(O)NR
12R
13 besteht, ausgewählt wird;
R
2 aus
der Gruppe, die aus Wasserstoff, Halo, C
1-C
10 Alkyl, Trihalomethyl, Hydroxy, C
1-C
10 Alkoxy, unsubstituiertem
C
3-C
8 Cycloalkoxy,
Cyano, -NR
9R
10,
-NR
9C(O)R
10, -C(O)R
8, -S(O)
2NR
9R
10 und -SO
2R
14 (wobei R
14 C
1-C
10 Alkyl,
C
6-C
12 Aryl, C
1-C
4 Alkyl, das mit C
6-C
12 Aryl substituiert ist, 5–12 gliedrigem
Heteroaryl, das 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt werden,
und C
1-C
4 Alkyl,
das mit einem 5–12
gliedrigem Heteroaryl, der 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt sind,
substituiert ist, ist) besteht, ausgewählt wird;
R
3,
R
4 und R
5 unabhängig Wasserstoff
oder C
1-C
10 Alkyl
sind;
Z C
6-C
12 Aryl,
5–12 gliedriges
Heteroaryl, das 1–4
Ringheteroatome ausgewählt
aus N, O oder S besitzt, 3–8 gliedriges
gesättigtes
Heterocyclyl, das 1 oder 2 Ringheteroatome ausgewählt aus
N, O oder S(O)
n, wobei n = 0–2 ist,
besitzt, -NR
15R
16,
wobei R
15 und R
16 unabhängig Wasserstoff
oder C
1-C
10 Alkyl
sind; oder R
15 und R
16 zusammen
mit dem Stickstoffatom, an welches sie gebunden sind, eine 3–8 gliedrige
Heterocycloaminogruppe bilden, die optional 1 oder 2 zusätzliche
Ringheteroatome besitzt, die aus N, O oder S(O)
n ausgewählt werden, wobei
n = 0–2
ist, ist;
R
6 aus der Gruppe, die aus
Wasserstoff oder C
1-C
10 Alkyl
besteht, ausgewählt
wird;
R
7 aus der Gruppe, die aus Wasserstoff,
C
1-C
10 Alkyl, C
6-C
12 Aryl, 5–12 gliedrigem Heteroaryl,
das 1–4
Ringheteroatome, die aus N, O oder S ausgewählt werden, besitzt, und -C(O)R
17 wie unten definiert besteht, ausgewählt wird;
R
8 aus der Gruppe, die aus Hydroxy, C
1-C
10 Alkoxy, unsubstituiertem
C
3-C
8 Cycloalkoxy,
C
6-C
12 Aryloxy,
und einem 5–12
gliedrigem Heteroaryloxy, das 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt werden,
besteht, ausgewählt
wird;
R
9 und R
10 unabhängig aus
der Gruppe, die aus Wasserstoff, C
1-C
10 Alkyl, C
1-C
10 Cyanoalkyl, C
3-C
8 monocyclischem Cycloalkyl, [5,6]- oder
[6,6]-fusioniertem bicyclischem Cycloalkyl, Adamantyl, C
6-C
12 Aryl und einem 5–12 gliedrigem
Heteroaryl, das 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt werden,
besteht, ausgewählt
werden; oder R
9 und R
10 zusammengenommen
eine 3–8
gliedrige Heterocycloaminogruppe bilden, die optional 1 oder 2 zusätzliche
Ringheteroatome besitzt, die aus N, O oder S(O)
n,
wobei n = 0–2
ist ausgewählt
werden;
R
12 und R
13 unabhängig aus
der Gruppe, die aus Wasserstoff, C
1-C
10 Alkyl, C
1-C
10 Hydroxyalkyl und C
6-C
12 Aryl besteht, ausgewählt werden; oder R
12 und
R
13 zusammen mit dem Stickstoffatom an das
sie gebunden sind, eine 3–8
gliedrige Heterocycloaminogruppe bilden, die optional 1 oder 2 zusätzliche
Ringheteroatome besitzt, die aus N, O oder S(O)
n ausgewählt werden,
wobei n = 0–2
ist, besteht, ausgewählt
werden;
R
17 aus der Gruppe, die aus
C
1-C
10 Alkyl, C
3-C
8 monocyclischem
Cycloalkyl, [5,6]- oder [6,6]-fusioniertem bicyclischem Cycloalkyl,
Adamantyl, C
6-C
12 Aryl,
Hydroxy und 5–12
gliedrigem Heteroaryl, das 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt werden,
besteht, ausgewählt
wird;
oder ein pharmazeutisch annehmbares Salz davon;
vorausgesetzt
dass die Verbindung nicht
ist und wobei
C
1-C
10 Alkyl substituiert
oder unsubstituiert sein kann, und falls es substituiert ist die
Substituentengruppe(n) aus Halo, Hydroxy, C
1-C
4 Alkoxy, C
6-C
12 Aryl, C
6-C
12 Aryloxy, 5–12 gliedrigem Heteroaryl,
das 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt werden,
einer 5–9
gliedrigen heteroalicyclischen Gruppe, die 1 oder 2 Heteroatome
besitzt, die aus N, O oder -S(O)
n ausgewählt werden,
wobei n = 0–2
ist, -C(O)R
8, -NR
9R
10 und -C(O)NR
9R
10 ausgewählt
wird;
C
3-C
8 monocyclisches
Cycloalkyl, [5,6]- oder [6,6]-fusioniertes
bicyclisches Cycloalkyl und Adamantyl substituiert oder unsubstituiert
sein können,
und falls sie substituiert sind die Substituentengruppe(n) eine
oder zwei Gruppen ist, die unabhängig
aus C
1-C
4 Alkyl,
C
1-C
4 Trihaloalkyl,
Halo, Hydroxy, C
1-C
4 Alkoxy,
C
6-C
12 Aryl, C
6-C
12 Aryloxy, 6-gliedrigem
Heteroaryl, das 1–3
Stickstoffringatome besitzt, 5-gliedrigem Heteroaryl, das 1–3 Heteroatome
besitzt, die aus N, O oder S ausgewählt werden, eine 5 oder 6-gliedrige
heteroalicyclische Gruppe, die 1–3 Heteroatome besitzt, die
aus N, O oder S ausgewählt
werden, Mercapto, C
1-C
4 S-Alkyl,
C
6-C
12 S-Aryl, Cyano,
-C(O)R'', -C(S)-R'', -OC(O)NR
12R
13, R
9OC(O)NR
10-, -OC(S)NR
12R
13, R
9OC(S)NR
10-, -C(O)NR
9R
10, R
9C(O)NR
10-, Nitro, NR
9S(O)
2R
10, -S(O)
2NR
9R
10,
R
9S(O)-, R
9S(O)
2-, C(O)OR
9, R
9C(O)O- und -NR
9R
10 ausgewählt
werden;
C
6-C
12 Aryl
substituiert oder unsubstituiert sein kann, und falls es substituiert
ist die Substituentengruppe(n) eine oder zwei Gruppen ist, die unabhängig aus
Halo, C
1-C
4 Alkyl,
C
1-C
4 Trihaloalkyl,
Hydroxy, Mercapto, Cyano, Carboxy, NR
9S(O)
2R
10, R
9C(O)NR
10-, -NHR oder -NRR, wobei R C
1-C
4 Alkyl, C
3-C
8 monocyclisches Cycloalkyl, [5,6]- oder
[6,6]-fusioniertes
bicyclisches Cycloalkyl oder Adamantyl ist, ausgewählt werden;
5–12 gliedriges
Heteroaryl substituiert oder unsubstituiert sein kann, und falls
es substituiert ist die Substituentengruppe(n) wie oben für C
6-C
12 Aryl definiert
ist;
5–9
gliedriger Heteroalicyclus substituiert oder unsubstituiert sein
kann, und falls er substituiert ist, die Substituentengruppe wie
oben für
C
6-C
12 Aryl definiert
ist;
3–8
gliedriges gesättigtes
Heterocyclyl substituiert oder unsubstituiert sein kann, und falls
es substituiert ist die Substituentengruppe(n) eine oder zwei Gruppen
ist, die unabhängig
aus =O (als ein C-Substituent, um so eine Carbonylgruppe zu bilden),
Halo, C
1-C
4 Alkyl,
C
1-C
4 Alkyl substituiert
mit Carboxy oder -C(O)O-R''- mit R'' wie hierin definiert, außer das
R'' nicht Wasserstoff
sein kann, Hydroxy, und -NHR oder -NRR, wobei R C
1-C
4 Alkyl oder C
3-C
8 monocyclisches Cycloalkyl ist, [5,6]- oder
[6,6]-fusioniertem bicyclischem Cycloalkyl, oder Adamantyl ausgewählt werden;
3–8 gliedrige
Heterocycloamino substituiert oder unsubstituiert sein kann, und
falls es substituiert ist, die Substituentengruppe(n) wie oben für 3–8 gliedriges
gesättigtes
Heterocyclyl definiert ist;
C
1-C
10 Alkoxy substituiert oder unsubstituiert
sein kann, und falls es substituiert die Substituentengruppe wie oben
für C
1-C
10 Alkyl definiert
ist;
C
6-C
12 Aryloxy
und 5–12
gliedriges Heteroaryloxy substituiert oder unsubstituiert sein können, und
falls sie substituiert sind, die Substituentengruppe(n) wie oben
für C
6-C
12 Aryl definiert
ist;
R'' aus der Gruppe,
die aus Wasserstoff, C
1-C
4 Alkyl,
Trihalomethyl, C
3-C
8 monocyclischem
Cycloalkyl, C
6-C
12 Aryl,
5–12 gliedrigem
Heteroaryl, das 1–4
Ringheteroatome besitzt, die aus N, O oder S ausgewählt werden, und
einer 5–9
gliedrigen heteroalicyclischen Gruppe, die 1 oder 2 Heteroatome
besitzt, die aus N, O oder -S(O)
n ausgewählt werden,
wobei n = 0–2
ist, besteht, ausgewählt
wird.
-
Eine
andere Ausführungsform
ist eine Verbindung der Formel I, wobei
R1 aus
der Gruppe, die aus Wasserstoff, Halo, C1-C10 Alkyl, C3-C8 monocyclischem Cycloalkyl, [5,6]- oder [6,6]-fusioniertem bicyclischem
Cycloalkyl, Adamantyl, einer 5–9
gliedrigen heteroalicyclischen Gruppe, die 1 oder 2 Heteroatome
besitzt, die aus N, O oder -S(O)n ausgewählt werden,
wobei n = 0–2
ist, Hydroxy, C1-C10 Alkoxy,
unsubstituiertem C3-C8 Cycloalkoxy,
-C(O)-R8, -NR9R10 und -C(O)NR12R13 besteht, ausgewählt wird;
R2,
R14, R3, R4, R5, Z, R15, R16, R6, R7, R8,
R9, R10 wie für Anspruch
1 definiert sind;
R12 und R13 unabhängig
aus der Gruppe, die aus Wasserstoff, C1-C10 Alkyl und C6-C12 Aryl besteht, ausgewählt werden; oder R12 und
R13 zusammen mit dem Stickstoffatom, an
welches sie gebunden sind, eine 3–8 gliedrige Heterocycloaminogruppe
bilden, die optional 1 oder 2 zusätzliche Ringheteroatome besitzt,
die aus N, O oder S(O)n ausgewählt werden,
wobei n = 0–2
ist;
R17 wie für Anspruch 1 definiert ist;
oder
ein pharmazeutisch annehmbares Salz davon.
-
Eine
andere Ausführungsform
ist eine Verbindung der Formel (Ia):
wobei:
R
1, R
3, R
4 und
R
5 Wasserstoff sind;
R
2 Fluor
ist und an der 5-Position des Indolinonrings platziert ist; und
Z
Morpholin-4-yl ist;
R
6 und R
7 Methyl sind.
-
Die
Stereochemie am *C ist bevorzugt (S).
-
Eine
andere Ausführungsform
ist eine pharmazeutische Zusammensetzung, die eine Verbindung oder ein
Salz der Formeln I oder Ia und einen pharmazeutisch annehmbaren
Träger
oder Hilfsstoff umfasst.
-
Eine
andere Ausführungsform
ist ein Verfahren zum Modulieren der katalytischen Aktivität einer
Proteinkinase in vitro, dass das in Kontakt bringen der Proteinkinase
mit einer Verbindung oder einem Salz der Formel I oder Ia umfasst.
Die Proteinkinase für
dieses Verfahren kann eine Rezeptor-Tyrosinkinase, eine Nichtrezeptor-Tyrosinkinase
und eine Serin-Threoninkinase sein.
-
Eine
andere Ausführungsform
ist die Verwendung einer pharmazeutischen Zusammensetzung, die eine
Verbindung oder ein Salz der Formel I oder Ia und einen pharmazeutisch
geeigneten Träger
oder Hilfsstoff für
die Herstellung eines Arzneimittels zur Behandlung oder zum Verhindern
einer mit einer Proteinkinase zusammenhängenden Störung in einem Organismus umfasst.
Die mit einer Proteinkinase zusammenhängende Störung kann eine mit einer Rezeptor-Tyrosinkinase zusammenhängende Störung, eine
mit einer Nichtrezeptor-Tyrosinkinase zusammenhängende Störung und eine mit einer Serin-Threoninkinase
zusammenhängende Störung sein.
Die mit einer Proteinkinase im Zusammenhang stehende Störung kann
eine mit EGFR zusammenhängende
Störung,
eine mit PDGFR zusammenhängende
Störung,
eine mit IGFR zusammenhängende Störung und
eine mit flk zusammenhängende
Störung
sein. Die Proteinkinasestörung
kann auch ein Plattenepithelzellkarzinom, ein Astrozytom, ein Kaposi's Sarkom, ein Glioblastom,
Lungenkrebs, Blasenkrebs, Kopf- und Halskrebs, ein Melanom, Ovarialkrebs,
Prostatakrebs, Brustkrebs, kleinzelliger Lungenkrebs, ein Gliom, colorektaler
Krebs, urogenitaler Krebs und gastrointestinaler Krebs sein. Darüber hinaus
kann die Proteinkinasestörung
auch Diabetes, eine Autoimmunstörung,
eine Hyperproliferationsstörung,
Restenose, Fibrose, Psoriasis, die von Heppel-Lindau-Krankheit,
Osteoarthritis, rheumatoide Arthritis, Angiogenese, eine entzündliche Störung, eine
immunologische Störung
und eine kardiovaskuläre
Störung
sein. In einer Ausführungsform
ist der oben genannte Organismus ein Mensch.
-
In
einer anderen Ausführungsform
betrifft diese Erfindung Verfahren zum Herstellen von Verbindungen der
Formel (I).
-
Zu
guter Letzt betrifft diese Erfindung auch das Identifizieren einer
chemischen Verbindung, die die katalytische Aktivität einer
Proteinkinase moduliert, durch in Kontakt bringen der Zellen, die
die Proteinkinase exprimieren, mit einer Verbindung oder einem Salz
der vorliegenden Erfindung, und dann das Überwachen der Zellen auf eine
Wirkung.
-
DETAILLIERTE
BESCHREIBUNG DER ERFINDUNG
-
Definitionen
-
Soweit
nicht anderweitig etwas anderes gesagt wird, haben die folgenden
in der Beschreibung und den Ansprüchen verwendeten Begriffe die
unten angegebene Bedeutung:
„Alkyl" betrifft ein gesättigtes, aliphatisches Kohlenwasserstoffradikal,
das gerade Ketten- und verzweigte Kettengruppen von 1 bis 20 Kohlenstoffatomen
(wann immer ein numerischer Bereich, z.B. „1–20", hierin beschrieben wird, bedeutet
das, dass die Gruppe, in diesem Fall die Alkylgruppe, ein Kohlenstoffatom,
zwei Kohlenstoffatome, drei Kohlenstoffatome, etc. bis zu und einschließlich 20
Kohlenstoffatome enthalten kann) einschließt. Noch bevorzugter ist es
ein mittelgroßes
Alkyl mit 1 bis 10 Kohlenstoffatomen, z.B. Methyl, Ethyl, Propyl,
2-Propyl, n-Butyl,
Iso-butyl, Tert-butyl, Pentyl und ähnliche. Am meisten bevorzugt
ist es ein niederes Alkyl mit 1 bis 4 Kohlenstoffatomen, z.B. Methyl,
Ethyl, Propyl, 2-Propyl, n-Butyl,
Iso-butyl, oder Tert-butyl und ähnliche.
Das Alkyl kann substituiert oder unsubstituiert sein, und wenn es
substituiert ist, ist/sind die substituierende(n) Gruppe(en) bevorzugt
Halo, Hydroxy, niederes Alkyl, Aryl, Aryloxy, Heteroaryl, heteroalicyclisch, C(O)R
8, NR
9R
10 und
C(O)NR
9R
10.
„Cycloalkyl" betrifft einen 3
bis 8 gliedrigen monocyclischen Vollkohlenstoff-Ring, einen Vollkohlenstoff
5 gliedrigen/6 gliedrigen oder 6 gliedrigen/6 gliedrigen fusionierten
bicyclischen Ring oder einen multicyclische fusionierte Ring(ein „fusioniertes" Ringsystem bedeutet,
dass jeder Ring in dem System ein benachbartes Paar von Kohlenstoffatomen
mit jedem anderen Ring im System teilt)-Gruppe, wobei einer oder
mehrere der Ringe eine oder mehrere Doppelbindungen enthalten können, jedoch
keiner der Ringe ein vollständig
konjugiertes Pi-Elektronensystem hat. Beispiele, ohne Begrenzung,
von Cycloalkyl-Gruppen sind Cyclopropan, Cyclobutan, Cyclopentan,
Cyclopenten, Cyclohexan, Cyclohexadien, Adamantan, Cycloheptan,
Cycloheptatrien und ähnliche.
Eine Cycloalkyl-Gruppe kann substituiert oder unsubstituiert sein.
Wenn sie substituiert ist, besteht(en) die Substituentengruppe(n)
bevorzugt aus einem oder mehreren, noch bevorzugter einem oder zwei Substituenten,
die unabhängig
aus der Gruppe ausgewählt
werden, die aus einem niederen Alkyl, Trihaloalkyl, Halo, Hydroxy,
niederem Alkoxy, Aryl, das ggf. mit einer oder mehreren, bevorzugt
einer oder zwei Gruppen unabhängig
voneinander Halo, Hydroxy, niederen Alkyl- oder niederen Alkoxy-Gruppen
substituiert ist, Aryloxy, das ggf. mit einer oder mehreren, bevorzugt
einer oder zwei Gruppen unabhängig
voneinander Halo, Hydroxy, niederem Alkyl oder niederen Alkoxy-Gruppen
substituiert ist, einem 6 gliedrigen Heteroaryl mit von 1 bis 3
Stickstoffatomen im Ring, wobei die Kohlenstoffe im Ring ggf. mit
einer oder mehreren, bevorzugt einer oder zwei Gruppen unabhängig voneinander
Halo, Hydroxy, niederem Alkyl oder niederen Alkoxy-Gruppen substituiert
sind, einem 5 gliedrigen Heteroaryl mit von 1 bis 3 Heteroatomen,
die aus der Gruppe aus Stickstoff, Sauerstoff und Schwefel ausgewählt werden,
wobei die Kohlenstoff- und Stickstoffatome der Gruppe ggf. mit einer
oder mehreren, bevorzugt einer oder zwei Gruppen unabhängig voneinander
Halo, Hydroxy, niederen Alkyl- oder niederen Alkoxy-Gruppen substituiert
sind, einer 5 oder 6 gliedrigen heteroalicyclischen Gruppe mit von
1 bis 3 Heteroatomen, die aus der Gruppe bestehend aus Stickstoff,
Sauerstoff und Schwefel ausgewählt werden,
wobei die Kohlenstoff- und Stickstoff (falls vorhanden)-Atome in
der Gruppe ggf. mit einer oder mehreren, bevorzugt einer oder zwei
Gruppen unabhängig
voneinander Halo, Hydroxy, niederem Alkyl oder niederen Alkoxy-Gruppen
substituiert sind, Mercapto, (niederem Alkyl)thio, Arylthio, das
ggf. mit einer oder mehreren, bevorzugt einer oder zwei Gruppen
unabhängig
voneinander Halo, Hydroxy, niederem Alkyl oder niederen Alkoxy-Gruppen
substituiert ist, Cyano, Acyl, Thioacyl, O-Carbamyl, N-Carbamyl,
O-Thiocarbamyl, N-Thiocarbamyl, C-Amido, N-Amido, Nitro, N-Sulfonamido,
S-Sulfonamido, R
9S(O)-, R
9S(O)
2-, -C(O)OR
9, R
9C(O)O- und -NR
9R
10 sind wie weiter oben definiert, besteht.
„Alkenyl" betrifft eine Alkyl-Gruppe,
wie hierin definiert, die aus wenigstens zwei Kohlenstoffatomen
und wenigstens einer Kohlenstoff-Kohlenstoff-Doppelbindung besteht.
Repräsentative
Beispiele schließen
ein, sind jedoch nicht begrenzt auf Ethenyl, 1-Propenyl, 2-Propenyl,
1-, 2-, oder 3-Butenyl und ähnliche.
„Alkynyl" betrifft eine Alkyl-Gruppe,
wie hierin definiert, die aus wenigstens zwei Kohlenstoffatomen
und wenigstens einer Kohlenstoff-Kohlenstoff-Dreifachbindung besteht.
Repräsentative
Beispiele schließen
ein, sind jedoch nicht begrenzt auf Ethynyl, 1-Propynyl, 2-Propynyl,
1-, 2-, oder 3-Butynyl und ähnliche.
„Aryl" betrifft einen monocyclischen
Vollkohlenstoff- oder
fusionierten Ring polycyclischer (d.h., Ringe, die benachbarte Paare
von Kohlenstoffatomen teilen) Gruppen von 1 bis 12 Kohlenstoffatomen
mit einem vollständig konjugierten
Pi-Elektronensystem. Beispiele, ohne Begrenzung, für Aryl-Gruppen sind Phenyl,
Naphthalenyl und Anthracenyl. Die Arylgruppe kann substituiert oder
unsubstituiert sein. Wenn sie substituiert ist, ist/sind die substituierte(n)
Gruppe(n) bevorzugt eine oder mehrere, noch bevorzugter eine, zwei
oder drei, am meisten bevorzugt eine oder zwei, die unabhängig aus
der Gruppe ausgewählt
wird/werden, die aus einem niederem Alkyl, Trihaloalkyl, Halo, Hydroxy,
niederem Alkoxy, Mercapto, (niederem Alkyl)thio, Cyano, Acyl, Thioacyl, O-Carbamyl, N-Carbamyl,
O-Thiocarbamyl, N-Thiocarbamyl, C-Amido, N-Amido, Nitro, N-Sulfonamido,
S-Sulfonamido, R
9S(O)-, R
9S(O)
2-, -C(O)OR
9, R
9C(O)O- und -NR
9R
10, mit R
9 und R
10 wie weiter oben definiert, besteht. Die
Aryl-Gruppe wird bevorzugt ggf. mit einem oder zwei Substituenten
substituiert, die unabhängig
voneinander aus Halo, niederem Alkyl, Trihaloalkyl, Hydroxy, Mercapto,
Cyano, N-Amido, Mono- oder
Dialkylamino, Carboxy oder N-Sulfonamido ausgewählt werden.
„Heteroaryl" betrifft eine monocyclische-
oder fusionierte Ring (d.h., Ringe die ein benachbartes Paar von
Atomen teilen)-Gruppe von 5 bis 12 Ringatomen, die ein, zwei, drei
oder vier Ring-Heteroatome enthalten, die ausgewählt werden aus N, O oder S,
wobei die verbleibenden Ringatome C sind und zusätzlich ein vollständig konjugiertes
Pi-Elektroniksystem
aufweisen. Beispiele, ohne Begrenzung, für unsubstituierte Heteroaryl-Gruppen
sind Pyrrol, Furan, Thiophen, Imidazol, Oxazol, Thiazol, Pyrazol,
Pyridin, Pyrimidin, Chinolin, Isochinolin, Purin, Tetrazol, Triazin
und Carbazol. Die Heteroarylgruppe kann substituiert oder unsubstituiert
sein. Wenn sie substituiert sind, ist/sind die substituierte(n)
Gruppe(n) bevorzugt eine oder mehrere, noch bevorzugter eine, zwei
oder drei, am meisten bevorzugt eine oder zwei, die unabhängig voneinander
aus der Gruppe ausgewählt
werden, die aus einem niederem Alkyl, Trihaloalkyl, Halo, Hydroxy,
niederem Alkoxy, Mercapto, (niederem Alkyl)thio, Cyano, Acyl, Thioacyl,
O-Carbamyl, N-Carbamyl, O-Thiocarbamyl, N-Thiocarbamyl, C-Amido, N-Amido,
Nitro, N-Sulfonamido, S-Sulfonamido, R
9S(O)-,
R
9(O)
2-, -C(O)OR
9, R
9C(O)O- und -NR
9R
10, mit R
9 und R
10 wie weiter
oben definiert, besteht. Bevorzugt ist die Heteroarylgruppe ggf.
mit einem oder zwei Substituenten substituiert, die unabhängig voneinander
aus Halo, niederem Alkyl, Trihaloalkyl, Hydroxy, Mercapto, Cyano,
N-Amido, Mono- oder Dialkylamino, Carboxy oder N-Sulfonamido ausgewählt werden.
„Heteroalicyclisch" betrifft eine monocyclische
oder fusionierte Ring-Gruppe, die im/in den Ring(en) 5 bis 9 Ringatome
aufweist, in dem/denen ein oder zwei Ringatome Heteroatome sind,
die aus N, O oder S(O)
n (wobei n eine ganze
Zahl von 0 bis 2 ist) ausgewählt
werden, wobei die verbleibenden Ringatome C sind. Die Ringe können auch
eine oder mehrere Doppelbindungen aufweisen. Jedoch weisen die Ringe
kein vollständig
konjugiertes Pi-Elektronensystem auf. Beispiele, ohne Begrenzung,
für unsubstituierte
heteroalicyclische Gruppen sind 2-Pyrrolidon, Piperidin, Piperazin,
Morpholin, Thiomorpholin, Homopiperazin und ähnliche. Der heteroalicyclische
Ring kann substituiert oder unsubstituiert sein. Wenn er substituiert
ist, ist/sind die substituierte(n) Gruppe(n) bevorzugt eine oder
mehrere, noch bevorzugter eine, zwei oder drei, am meisten bevorzugt
eine oder zwei, die unabhängig
ausgewählt
werden aus der Gruppe, die aus niederem Alkyl, Trihaloalkyl, Halo,
Hydroxy, niederem Alkoxy, Mercapto, (niederem Alkyl)thio, Cyano,
Acyl, Thioacyl, O-Carbamyl, N-Carbamyl, O-Thiocarbamyl, N-Thiocarbamyl,
C-Amido, N-Amido, Nitro, N-Sulfonamido, S-Sulfonamido, R
9S(O)-, R
9S(O)
2-, -C(O)OR
9, R
9C(O)O-, und -NR
9R
10, mit R
9 und R
10 wie weiter oben definiert, besteht. Bevorzugt
ist die heteroalicyclische Gruppe ggf. mit einem oder zwei Substituenten
substituiert, die unabhängig
voneinander ausgewählt
werden aus Halo, niederem Alkyl, Trihaloalkyl, Hydroxy, Mercapto,
Cyano, N-Amido, Mono- oder Dialkylamino, Carboxy, oder N-Sulfonamido.
„Heterocyclisch" bedeutet ein gesättigtes
cyclisches Radikal aus 3 bis 8 Ringatomen, in dem ein oder zwei Ringatome
Heteroatome sind, die ausgewählt
werden aus N, O oder S(O)
n (wobei N eine
ganze Zahl von 0 bis 2 ist), wobei die verbleibenden Ringatome C
sind, wobei ein oder zwei C-Atome ggf. durch eine Carbonyl-Gruppe
ersetzt werden können.
Der Heterocyclyl-Ring kann ggf. unabhängig mit einem, zwei oder drei Substituenten
substituiert werden, die ausgewählt
werden aus niederem Alkyl, das ggf. mit einem oder zwei Substituenten
substituiert ist, die unabhängig
ausgewählt
werden aus einer Carboxy- oder Ester-Gruppe, Haloalkyl, Cyanoalkyl,
Halo, Nitro, Cyano, Hydroxy, Alkoxy, Amino, Monoalkylamino, Dialkylamino,
Aralkyl, Heteroaralkyl und -COR (wobei R ein Alkyl ist). Der Begriff
Heterocyclyl schließt
ganz besonders ein, ist jedoch nicht begrenzt auf Tetrahydropyranyl,
2,2-Dimethyl-1,3-Dioxolan, Piperidin, N-Methylpiperidin-3-yl, Piperazin, N-Methylpyrrolidin-3-yl,
2-Pyrrolidon, Morpholin,
Thiomorpholin, Thiomorpholin-1-oxid, Thiomorpholin-1,1-dioxid, 4-Ethyloxycarbonylpiperazin,
3-Oxopiperazin,
2-Imidazolidon, 2-Pyrrolidon, 2-Oxohomopiperazin,
Tetrahydropyrimidin-2-on und den Derivaten davon. Die heterocyclische
Gruppe ist bevorzugt ggf. mit einem oder mehreren Substituenten
substituiert, die unabhängig
ausgewählt
werden aus Halo, niederem Alkyl, niederem Alkyl, das mit Carboxy,
Esterhydroxy, oder Mono- oder
Dialkylamino substituiert ist.
„Heterocycloamino" bedeutet ein gesättigtes
cyclisches Radikal aus 3 bis 8 Ringatomen, in dem wenigstens eines
der Ringatome Stickstoff ist, und wobei ggf. ein oder zwei zusätzliche
Ringatome Heteroatome sind, die ausgewählt werden aus N, O oder S(O)
n (wobei n eine ganze Zahl von 0 bis 2 ist),
wobei die verbleibenden Ringatome C sind, wobei ein oder zwei C-Atome
ggf. durch eine Carbonyl-Gruppe ersetzt werden können. Der Heterocycloamino-Ring
kann ggf. unabhängig
mit einem, zwei oder drei Substituenten substituiert werden, die ausgewählt werden
aus niederem Alkyl, das gegebenenfalls mit einem oder zwei Substituenten
substituiert ist, die unabhängig
voneinander ausgewählt
werden aus einer Carboxy- oder
Estergruppe, Haloalkyl, Cyanoalkyl, Halo, Nitro, Cyano, Hydroxy,
Alkoxy, Amino, Monoalkylamino, Dialkylamino, Aralkyl, Heteroaralkyl
und -COR (wobei R ein Alkyl ist). Der Begriff Heterocycloamino schließt noch
spezifischer ein, ist jedoch nicht begrenzt auf Piperidin-1-yl,
Piperazin-1-yl, Pyrrolidin-1-yl, Morpholin-4-yl, Thiomorpholin-4-yl,
Thiomorpholin-1-oxid, Thiomorpholin-1,1-dioxid, 4-Ethyloxycarbonylpiperazin-1-yl,
3-Oxopiperazin-1-yl, 2-Imidazolidon-1-yl, 2-Pyrrolidon-1-yl, 2-Oxohomopiperazin,
Tetrahydropyrimidin-2-on und die Derivate davon. Bevorzugt ist die
heterocyclische Gruppe ggf. mit einem oder zwei Substituenten, die
unabhängig
ausgewählt
werden aus Halo, niederem Alkyl, niederem Alkyl, das mit Carboxy
oder einem Ester substituiert ist, Hydroxy, oder Mono- oder Dialkylamino,
substituiert. Die Heterocycloamino-Gruppe ist eine Teilmenge der
weiter oben definierten heterocyclischen Gruppe.
„Hydroxy" betrifft eine -OH-Gruppe.
„Alkoxy" betrifft sowohl
eine -O-(Alkyl) als auch eine -O-(unsubstituiertes Cycloalkyl)Gruppe.
Repräsentative Beispiele
schließen
ein, sind jedoch nicht begrenzt auf, z.B. Methoxy, Ethoxy, Propoxy,
Butoxy, Cyclopropyloxy, Cyclobutyloxy, Cyclopentyloxy, Cyclohexyloxy
und ähnliche.
„Haloalkoxy" betrifft eine -O-(Haloalkyl)Gruppe.
Repräsentative
Beispiele schließen
ein, sind jedoch nicht begrenzt auf, z.B. Trifluormethoxy, Tribrommethoxy
und ähnliche.
„Arlyoxy" betrifft sowohl
eine -O-Aryl- als auch eine -O-Heteroaryl-Gruppe, wie hierin definiert.
Repräsentative Beispiele
schließen
ein, sind jedoch nicht begrenzt auf Phenoxy, Pyridinyloxy, Furanyloxy,
Thienyloxy, Pyrimidinyloxy, Pyrazinyloxy, und ähnliche und Derivate davon.
„Mercapto" betrifft eine -SH-Gruppe.
„Alkylthio" betrifft sowohl
eine -S-(Alkyl)- als auch eine -S-(unsubstituierte Cycloalkyl-)Gruppe.
Repräsentative Beispiele
schließen
ein, sind jedoch nicht begrenzt auf, z.B. Methylthio, Ethylthio,
Propylthio, Butylthio, Cyclopropylthio, Cyclobutylthio, Cyclopentylthio,
Cyclohexylthio und ähnliche.
„Arylthio" betrifft sowohl
eine -S-Aryl- als auch eine -S-Heteroaryl-Gruppe, wie hierin definiert.
Repräsentative Beispiele
schließen
ein, sind jedoch nicht begrenzt auf Phenylthio, Pyridinylthio, Furanylthio,
Thienylthio, Pyrimidinylthio, und ähnliche und Derivate davon.
„Acyl" betrifft eine -C(O)-R''-Gruppe, wobei R'' aus
der Gruppe ausgewählt
wird, die aus Wasserstoff, niederem Alkyl, Trihalomethyl, unsubstituiertem
Cycloalkyl, Aryl, das ggf. mit einem oder mehreren, bevorzugt einem, zwei
oder drei Substituenten substituiert wird, die aus der Gruppe ausgewählt werden,
die aus niederem Alkyl, Trihalomethyl, niederem Alkoxy, Halo und
-NR
9R
10-Gruppen
besteht, Heteroaryl (das durch einen Kohlenstoffring gebunden ist),
das ggf. mit einem oder mehreren, bevorzugt einem, zwei oder drei
Substituenten substituiert ist, die aus der Gruppe ausgewählt werden,
die aus einem niederem Alkyl, Trihaloalkyl, niederem Alkoxy, Halo
und -NR
9R
10-Gruppen
besteht, und Heteroalicyclen (das durch einen Kohlenstoffring gebunden
ist), die ggf. mit einem oder mehreren, bevorzugt einem, zwei oder
drei Substituenten substituiert sind, die aus der Gruppe ausgewählt werden,
die aus niederem Alkyl, Trihaloalkyl, niederem Alkoxy, Halo und
-NR
9R
10-Gruppen besteht.
Repräsentative
Acyl-Gruppen schließen
ein, sind jedoch nicht begrenzt auf Acetyl, Trifluoracetyl, Benzoyl
und ähnliche.
„Aldehyd" betrifft eine Acyl-Gruppe,
in der R'' Wasserstoff ist.
„Thioacyl" betrifft eine -C(S)-R''-Gruppe, mit R'' wie
hierin definiert.
„Ester" betrifft eine -C(O)O-R''-Gruppe, mit R'' wie
hierin definiert, mit der Ausnahme, dass R'' nicht
Wasserstoff sein kann.
„Acetyl"-Gruppe betrifft
eine -C(O)CH
3-Gruppe.
„Halo"-Gruppe betrifft
Fluor, Chlor, Brom oder Iod, bevorzugt Fluor oder Chlor.
„Trihalomethyl"-Gruppe betrifft
eine -CX
3-Gruppe, wobei X ein Halo ist,
wie weiter oben definiert.
„Trihalomethansulfonyl"-Gruppe betrifft
X
3CS(=O)
2-Gruppen mit X wie
weiter oben definiert.
„Cyano" betrifft eine -C≡N-Gruppe.
„S-Sulfonamido" betrifft eine -S(O)
2NR
9R
10-Gruppe,
mit R
9 und R
10 wie
hierin definiert.
„N-Sulfonamido" betrifft eine -NR
9S(O)
2R
10-Gruppe,
mit R
9 und R
10 wie
hierin definiert.
„O-Carbamyl"-Gruppe betrifft
eine -OC(O)NR
12R
13-Gruppe,
mit R
12 und R
13 wie
hierin definiert.
„N-Carbamyl" betrifft eine R
9OC(O)NR
10-Gruppe,
mit R
9 und R
10 wie
hierin definiert.
„O-Thiocarbamyl" betrifft eine -OC(S)NR
12R
13-Gruppe, mit
R
12 und R
13 wie
hierin definiert.
„N-Thiocarbamyl" betrifft eine R
9OC(S)NR
10-Gruppe,
mit R
9 und R
10 wie
hierin definiert.
„Amino" betrifft eine -NR
9R
10-Gruppe, wobei
R
9 und R
10 beide
Wasserstoffe sind.
„C-Amido" betrifft eine -C(O)NR
9R
10-Gruppe, mit
R
9 und R
10 wie hierin
definiert.
„N-Amido" betrifft eine R
9C(O)NR
10-Gruppe,
mit R
9 und R
10 wie
hierin definiert.
„Nitro" betrifft eine -NO
2-Gruppe.
„Haloalkyl" bedeutet ein Alkyl, bevorzugt ein niederes
Alkyl, wie weiter oben definiert, das mit einem oder mehreren gleichen
oder unterschiedlichen Halo-Atomen, z.B. -CH
2Cl,
-CF
3, -CH
2CF
3, -CH
2CCl
3 und ähnlichem, substituiert
ist.
„Hydroxyalkyl" bedeutet ein Alkyl,
bevorzugt ein niederes Alkyl, wie weiter oben definiert, das mit
einer, zwei oder drei Hydroxy-Gruppen, z.B. Hydroxymethyl, 1- oder
2-Hydroxyethyl, 1,2-, 1,3-, oder 2,3-Dihydroxypropyl und ähnlichem
substituiert ist.
„Aralkyl" bedeutet Alkyl,
bevorzugt ein niederes Alkyl, wie weiter oben definiert, das mit
einer Aryl-Gruppe, wie oben definiert, z.B. -CH
2Phenyl,
-(CH
2)
2Phenyl, -(CH
2)
3Phenyl, CH
3CH(CH
3)CH
2Phenyl, und ähnlichen und Derivaten davon,
substituiert ist.
„Heteroaralkyl"-Gruppe bedeutet
ein Alkyl, bevorzugt ein niederes Alkyl, wie weiter oben definiert,
das mit einer Heteroaryl-Gruppe, z.B. -CH
2Pyridinyl,
-(CH
2)
2Pyrimidinyl, -(CH
2)
3Imidazolyl, und ähnlichen
und Derivaten davon, substituiert ist.
„Monoalkylamino" bedeutet ein Radikal
-NHR, wobei R ein Alkyl oder eine unsubstituierte Cycloalkyl-Gruppe, wie
weiter oben definiert, ist, z.B. Methylamino, (1-Methylethyl)amino,
Cyclohexylamino und ähnliche.
„Dialkylamino" bedeutet ein Radikal
-NRR, wobei jedes R unabhängig
ein Alkyl oder eine unsubstituierte Cycloalkyl-Gruppe, wie weiter oben definiert, ist,
z.B. Dimethylamino, Diethylamino, (1-Methylethyl)-Ethylamino, Cyclohexylmethylamino,
Cyclopentylmethylamino und ähnliche.
„Wahlweise" oder „gegebenenfalls
(ggf.)" bedeutet,
dass das nachfolgend beschriebene Ereignis oder Umstand auftreten
kann aber nicht muss, und dass die Beschreibung Beispiele enthält, in denen
das Ereignis oder der Umstand auftritt und Beispiele in denen es
das nicht tut. Zum Beispiel bedeutet „heterocyclische Gruppe, die
ggf. mit einer Alkyl-Gruppe substituiert ist", dass das Alkyl vorliegen kann, jedoch
nicht vorliegen muss, und die Beschreibung Situationen einschließt, in denen
die heterocyclische Gruppe mit einer Alkylgruppe substituiert ist
und Situationen, in denen die Heterocyclo-Gruppe nicht mit einer
Alkyl-Gruppe substituiert ist.
Die Begriffe „2-Indolinon", „Indolin-2-on" und „2-Oxindol" werden hierin miteinander
austauschbar verwendet, um ein Molekül mit der chemischen Struktur
zu bezeichnen:
Der Begriff „Pyrrol" betrifft ein Molekül mit der
chemischen Struktur:
-
-
Verbindungen,
die die gleiche Molekularformel aufweisen, jedoch in der Natur oder
Sequenz der Bindung ihrer Atome oder der Anordnung ihrer Atome im
Raum verschieden sind, werden „Isomere" genannt. Isomere,
die sich in der Anordnung ihrer Atome im Raum unterscheiden, werden „Stereoisomer" genannt. Stereoisomere,
die nicht Spiegelbilder voneinander sind, werden „Diastereomere" genannt und solche,
die nicht miteinander in Deckung bringende Spiegelbilder voneinander
sind, werden „Enantiomer" genannt. Wenn eine Verbindung
ein asymmetrisches Zentrum aufweist, zum Beispiel ist es an vier
verschiedene Gruppen gebunden, ist ein Paar von Enantiomeren möglich. Ein
Enantiomer kann durch die absolute Konfiguration seines asymmetrischen
Zentrums charakterisiert sein und wird durch R- und S-Sequenzregeln
von Cahn und Prelog oder durch die Art und Weise wie das Molekül die Ebene
des polarisierten Lichtes dreht, beschrieben, und als rechtsdrehend
oder linksdrehend (d.h. als (+) bzw. (–)-Isomere) gekennzeichnet.
Eine chirale Verbindung kann entweder als individuelles Enantiomer
oder als eine Mischung davon existieren. Eine Mischung, die gleiche Anteile
der Enantiomere enthält,
wird eine „razemische
Mischung" genannt.
-
Die
Verbindungen dieser Erfindung können
ein oder mehrere asymmetrische Zentren besitzen; diese Verbindungen
können
daher als individuelle (R)- oder (S)-Stereoisomere oder als Mischungen
davon hergestellt werden. Zum Beispiel ist das Kohlenstoffatom,
das die Hydroxy-Gruppe in -CONHCHR3-CR4(OH)CR5 2 in einer Verbindung
der Formel (I) trägt,
ein asymmetrisches Zentrum und daher kann die Verbindung der Formel (I)
als ein (R)- oder (S)-Stereoisomer existieren. So lange nichts Gegenteiliges
angegeben wird, soll die Beschreibung oder Benennung einer bestimmten
Verbindung im beschreibenden Teil und den Ansprüchen sowohl die individuellen
Enantiomere als auch die Mischungen, razemisch oder anders, davon
einschließen.
Die Verfahren zur Bestimmung der Stereochemie und der Auftrennung
von Stereoisomeren sind im Stand der Technik gut bekannt (siehe
die Erörterung
im Kapitel 4 von „Advanced
Organic Chemistry",
4. Ausgabe, J. March, John Wiley and Sons, New York, 1992).
-
Die
Verbindungen der Formel (I) können
das Phänomen
der Tautomerie und der strukturellen Isomerie zeigen. Zum Beispiel
können
die hierin beschriebenen Verbindungen eine E- oder eine Z-Konfiguration bzgl. der
Doppelbindung, die den 2-Indolinon-Rest mit dem Pyrrol-Rest verbindet,
annehmen, oder sie können
eine Mischung aus E und Z sein. Diese Erfindung umfasst jede tautomere
oder strukturell isomere Form und Mischungen davon, die die Fähigkeit
besitzen, die RTK, CTK und/oder STK-Atkivität zu modulieren, und ist nicht auf
eine tautomere oder strukturell isomere Form beschränkt.
-
Eine „pharmazeutische
Zusammensetzung" betrifft
eine Mischung aus einer oder mehreren der hierin beschriebenen Verbindungen,
oder physiologisch/pharmazeutisch annehmbaren Salzen oder Arzneimittelvorstufen
davon mit anderen chemischen Komponenten, wie zum Beispiel physiologisch/pharmazeutisch
annehmbaren Trägern
und Hilfsstoffen. Der Zweck einer pharmazeutischen Zusammensetzung
ist es, das Verabreichen einer Verbindung an einen Organismus zu
erleichtern.
-
Die
Verbindung der Formel (I) kann auch als eine Arzneimittelvorstufe
wirken. Eine „Arzneimittelvorstufe" betrifft ein Agens,
dass in vivo in die Arzneimittelendstufe umgewandelt wird. Arzneimittelvorstufen
sind häufig
nützlich,
da sie in einigen Situationen einfacher verabreicht werden können als
die Arzneimittelendstufe. Sie können
zum Beispiel durch orale Verabreichung biologisch verfügbar sein,
während
es die Arzneimittelendstufe nicht ist. Die Arzneimittelvorstufe
kann auch eine bessere Löslichkeit
in pharmazeutischen Zusammensetzungen gegenüber der Arzneimittelendstufe
aufweisen. Eine ohne zur Begrenzung dienendes Beispiel einer Arzneimittelvorstufe
wäre eine
Verbindung der vorliegenden Erfindung, die als ein Ester (die „Arzneimittelvorstufe") verabreicht wird,
um die Übertragung über eine
Zellmembran zu erleichtern, bei der die Wasserlöslichkeit nachteilig für die Mobilität ist, dann
jedoch metabolisch zur Carboxylsäure,
der aktiven Einheit, hydrolisiert wird, sobald sie in der Zelle
ist, in der die Wasserlöslichkeit
besser ist.
-
Ein
weiteres Beispiel einer Arzneimittelvorstufe kann ein kurzes Polypeptid
sein, zum Beispiel, ohne Begrenzung, ein 2–10 Aminosäurepolypeptid, das durch eine
terminale Amino-Gruppe an eine Carboxy-Gruppe einer Verbindung dieser
Erfindung gebunden ist, wobei das Polypeptid in vivo hydrolisiert
oder metabolisiert wird, um das aktive Molekül freizusetzen. Die Arzneimittelvorstufen
einer Verwendung der Formel (I) liegen innerhalb des Schutzumfangs
dieser Erfindung.
-
Zusätzlich wird
in Erwägung
gezogen, dass eine Verbindung der Formeln (I) durch Enzyme im Körper des
Organismus, wie zum Beispiel eines Menschen, metabolisiert wird,
um einen Metaboliten zu erzeugen, der die Aktivität der Proteinkinase
modulieren kann. Solche Metabolite liegen innerhalb des Schutzumfangs
der vorliegenden Erfindung.
-
Wie
hierin verwendet, betrifft ein „physiologisch/pharmazeutisch
annehmbarer Träger" einen Träger oder
ein Verdünnungsmittel,
der keine wesentliche Reizung eines Organismus verursacht und die
biologische Aktivität
und die Eigenschaften der verabreichten Verbindung nicht aufhebt.
-
Ein „pharmazeutisch
geeignetes Hilfsmittel" betrifft
eine inerte Substanz, die zu einer pharmazeutischen Zusammensetzung
gegeben wird, um das Verabreichen einer Verbindung weiter zu erleichtern.
Beispiele, ohne Begrenzung, für
Hilfsmittel schließen
Calciumcarbonat, Calciumphosphat, verschiedene Zucker und Stärketypen,
Zellulosederivate, Gelatine, Pflanzenöle und Polyethylenglycole ein.
-
Wie
hierin verwendet, betrifft der Begriff „pharmazeutisch annehmbares
Salz" solche Salze,
die die biologische Wirksamkeit und die Eigenschaften der Verbindungsendstufe
beibehalten. Solche Salze schließen ein:
- (i)
Säureadditionssalz,
dass durch Reaktion der freien Base der Verbindungsendstufe mit
anorganischen Säuren,
wie zum Beispiel Salzsäure,
Bromwasserstoffsäure,
Salpetersäure,
Phosphorsäure,
Schwefelsäure
und Perchlorsäure
und ähnliche,
oder mit organischen Säuren,
wie zum Beispiel Essigsäure,
Oxalsäure, (D)
oder (L) Apfelsäure,
Maleinsäure,
Methansulfonsäure,
Ethansulfonsäure,
p-Toluensulfonsäure,
Salicylsäure,
Tartarsäure,
Zitronensäure,
Succinsäure
oder Malonsäure
und ähnliche,
bevorzugt Salzsäure
oder (L)-Apfelsäure, erhalten
wird; oder
- (2) Salze, die gebildet werden, wenn ein Säureproton vorhanden ist, das
in der Verbindungsendstufe entweder durch ein Metallion, z.B. ein
Alkalimetallion, ein Erdalkaliion oder ein Aluminiumion, ersetzt
wird; oder sich an eine organische Base, wie zum Beispiel Ethanolamin,
Diethanolamin, Triethanolamin, Tromethanmin, N-Methylglucamin und ähnliche
anlagert.
-
„PK" betrifft die Rezeptorprotein-Tyrosinkinase
(RTK's), die Nichtrezeptor-
oder „zelluläre" Tyrosinkinase (CTK's) und die Serin-Threoninkinasen
(STK's).
-
„Verfahren" betrifft die Art
und Weise, die Mittel, die Techniken und Prozeduren zum Ausführen einer vorgegebenen
Aufgabe, die einschließen,
jedoch nicht begrenzt sind auf eine solche Art und Weise, Mittel, Techniken
und Prozeduren, die entweder bekannt sind, oder bereits aus einer
bekannten Art und Weise, Mitteln, Techniken und Prozeduren von Praktikern
der chemischen, pharmazeutischen, biologischen, biochemischen und
medizinischen Techniken entwickelt worden sind.
-
Die „Modulation" oder „das Modulieren" betrifft das Verändern der
katalytischen Aktivität
von RTK's, CTK's und STK's. Das Modulieren
betrifft besonders die Aktivierung der katalytischen Aktivität von RTK's, CTK's und STK's, bevorzugt die
Aktivierung oder Inhibierung der katalytischen Aktivität von RTK's, CTK's und STK's, abhängig von
der Konzentration der Verbindung oder des Salzes dem gegenüber die
RTK, CTK oder STK ausgesetzt wird, oder noch bevorzugter die Inhibierung
der katalytischen Aktivität
der RTK's, CTK's und STK's.
-
Die „katalytische
Aktivität" betrifft die Phosphorylierungsrate
des Tyrosins unter dem Einfluss, direkt oder indirekt, von RTK's und/oder CTK's, oder die Phosphorylierung
von Serin und Threonin unter dem Einfluss, direkt oder indirekt,
von STK's.
-
Das „in Kontakt
bringen" betrifft
das Zusammenbringen einer Verbindung dieser Erfindung und einer Ziel-PK
auf eine Art und Weise, bei der die Verbindung die katalytische Aktivität der PK,
entweder direkt, d.h. durch Interagieren mit der Kinase selber,
oder indirekt, d.h. durch Interagieren mit einem anderen Molekülen von
dem die katalytische Aktivität
der Kinase abhängt,
beeinflussen kann. Ein solches „in Kontakt bringen" kann „in vitro", d.h. in einem Teströhrchen,
einer Petrischale oder ähnlichem,
durchgeführt
werden. In einem Teströhrchen
kann das in Kontakt bringen nur eine Verbindung und eine entsprechende
PK involvieren, oder es kann ganze Zellen involvieren. Zellen können auch
in Zellkulturschalen beibehalten, oder herangezogen werden und in
dieser Umgebung mit einer Verbindung in Kontakt gebracht werden.
In diesem Zusammenhang kann die Fähigkeit einer bestimmten Erfindung
eine mit PK zusammenhängende
Störung
zu beeinflussen, d.h. den IC50 der Verbindung,
der weiter unten definiert wird, vor der Verwendung der Verbindungen
in vivo bestimmt werden, wobei dies mit komplexeren lebenden Organismen
versucht wird. Für
Zellen außerhalb
des Organismus gibt es vielfältige
Verfahren und diese sind dem Fachmann gut bekannt, um die PK's in Kontakt mit
den Verbindungen zu bringen, die einschließen, jedoch nicht begrenzt
sind auf direkte Zell-Mikroinjektion und zahlreiche Transmembran-Träger-Techniken.
-
„In vitro" betrifft Prozeduren,
die in einer künstlichen
Umgebung, wie zum Beispiel, ohne Begrenzung, in einem Teströhrchen oder
im Kulturmedium, durchgeführt
werden.
-
„In vivo" betrifft Prozeduren,
die innerhalb eines lebenden Organismus, wie zum Beispiel, ohne
Begrenzung, einer Maus, Ratte oder einem Hasen, durchgeführt werden.
-
„Mit PK
zusammenhängende
Störung", „PK getriebene
Störung" und „abnormale
PK-Aktivität" betreffen alle einen
Zustand, der durch eine ungeeignete, d.h. unter oder, gebräuchlicher über, PK
katalytische Aktivität
gekennzeichnet ist, wobei die bestimmte PK eine RTK, eine CTK oder
eine STK sein kann. Eine ungeeignete katalytische Aktivität kann sich
als ein Ergebnis ergeben, entweder: (1) der PK-Expression in Zellen, die
normalerweise keine PK's
exprimieren, (2) der erhöhten
PK-Expression, die zur ungewollten Zellproliferation, Differenzierung
und/oder Wachstum führt,
oder (3) der verringerten PK-Expression, die zu ungewollten Verringerungen
der Zellproliferation, Differenzierung und/oder Wachstum führt. Die Überaktivität einer
PK betrifft entweder die Amplifikation des Gens, dass für eine bestimmte
PK kodiert, oder das Erzeugen eines PK-Aktivitätsniveaus, das mit einer Zellproliferations-,
Differenzierungs- und/oder Wachstumsstörung (dass heißt, wenn
das PK-Niveau zunimmt, nimmt der Schweregrad eines oder mehrerer
der Symptome der zellulären
Störung
zu) korreliert. Die zu geringe Aktivität ist selbstverständlich das
Gegenteil, wobei der Schweregrad eines oder mehrerer Symptome einer
zellulären
Störung
zunimmt, wenn das PK-Aktivitätsniveau
sich verringert.
-
Das „Behandeln" und die „Behandlung" betreffen ein Verfahren
zum Lindern oder Aufheben einer durch PK vermittelten zellulären Störung und/oder
ihrer begleitenden Symptome. Besonders in Bezug auf Krebs bedeuten
diese Begriffe einfach, dass die Lebenserwartung eines Individuums,
das vom Krebs betroffen ist, zunehmen wird, oder dass eines oder
mehrere der Symptome der Erkrankung verringert werden.
-
Ein „Organismus" betrifft jede lebende
Entität,
die aus wenigstens einer Zelle besteht. Ein lebender Organismus
kann etwas so einfach sein, wie zum Beispiel eine einzelne eukaryotische
Zelle, oder so Komplex wie ein Säugetier,
einschließlich
eines Menschen.
-
Die „therapeutisch
wirksame Menge" betrifft
die zu verabreichende Menge der Verbindung, die bis zu einem gewissen
Umfang ein oder mehrere der Symptome der zu behandelnden Erkrankung
lindert. In Bezug auf die Behandlung von Krebs betrifft eine therapeutisch
wirksame Menge die Menge, die die Wirkung hat:
- (1)
Verringern der Größe des Tumors;
- (2) Inhibieren (das heißt,
zumindest in einem gewissen Umfang verlangsamen, bevorzugt stoppen)
der Tumormetastase;
- (3) Inhibieren, bis zu einem gewissen Ausmaß (das heißt, zumindest in einem gewissen
Umfang verlangsamen, bevorzugt stoppen), des Tumorwachstums und/oder
- (4) Lindern, bis zu einem gewissen Ausmaß (oder bevorzugt eliminieren),
eines oder mehrerer Symptome, die mit dem Krebs im Zusammenhang
stehen.
-
„Überwachen" bedeutet, Beobachten
oder Detektieren der Wirkung beim in Kontakt bringen einer Verbindung
mit einer Zelle, die eine bestimmte PK exprimiert. Die beobachtete
oder detektierte Wirkung kann eine Veränderung des Zellphänotyps,
der katalytische Aktivität
einer PK, oder eine Veränderung
der Wechselwirkung einer PK mit einem natürlichen Bindungspartner sein.
Techniken zum Beobachten oder Detektieren solcher Wirkungen sind
im Stand der Technik gut bekannt.
-
Die
oben beschriebene Wirkung wird ausgewählt aus einer Veränderung
oder einer Abwesenheit einer Veränderung
in einem Zellphänotyp,
eine Veränderung
oder Abwesenheit einer Veränderung
in der katalytischen Aktivität
der Proteinkinase oder eine Veränderung
oder Abwesenheit einer Veränderung
bei der Wechselwirkung der Proteinkinase mit einem natürlichen
Bindungspartner in einem letzten Aspekt dieser Erfindung.
-
Der „Zellphänotyp" betrifft die äußere Erscheinung
einer Zelle oder eines Gewebes, oder die biologische Funktion der
Zelle oder des Gewebes. Beispiele, ohne Begrenzung, eines Zellphänotyps sind
die Zellgröße, das
Zellwachstum, die Zellproliferation, die Zelldifferenzierung, das
Zellüberleben,
die Apoptose, die Nährstoffaufnahme
und die die Verwendbarkeit. Solche phänotypischen Charakteristika
sind durch im Stand der Technik gut bekannte Techniken messbar.
-
Der „natürliche Bindungspartner" betrifft ein Polypeptid,
das an eine bestimmte PK in einer Zelle bindet. Natürliche Bindungspartner
können
eine Rolle beim Verbreiten eines Signals in einem PK-vermittelten
Signaltransduktionsprozess spielen. Eine Veränderung der Wechselwirkung
des natürlichen
Bindungspartners mit der PK kann sich selbst als eine erhöhte oder
verringerte Konzentration des PK/natürlichen Bindungspartner-Komplexes
manifestieren und, als eine Folge davon, in einer beobachtbaren
Veränderung
der Fähigkeit der
PK, die Signaltransduktion zu vermitteln.
-
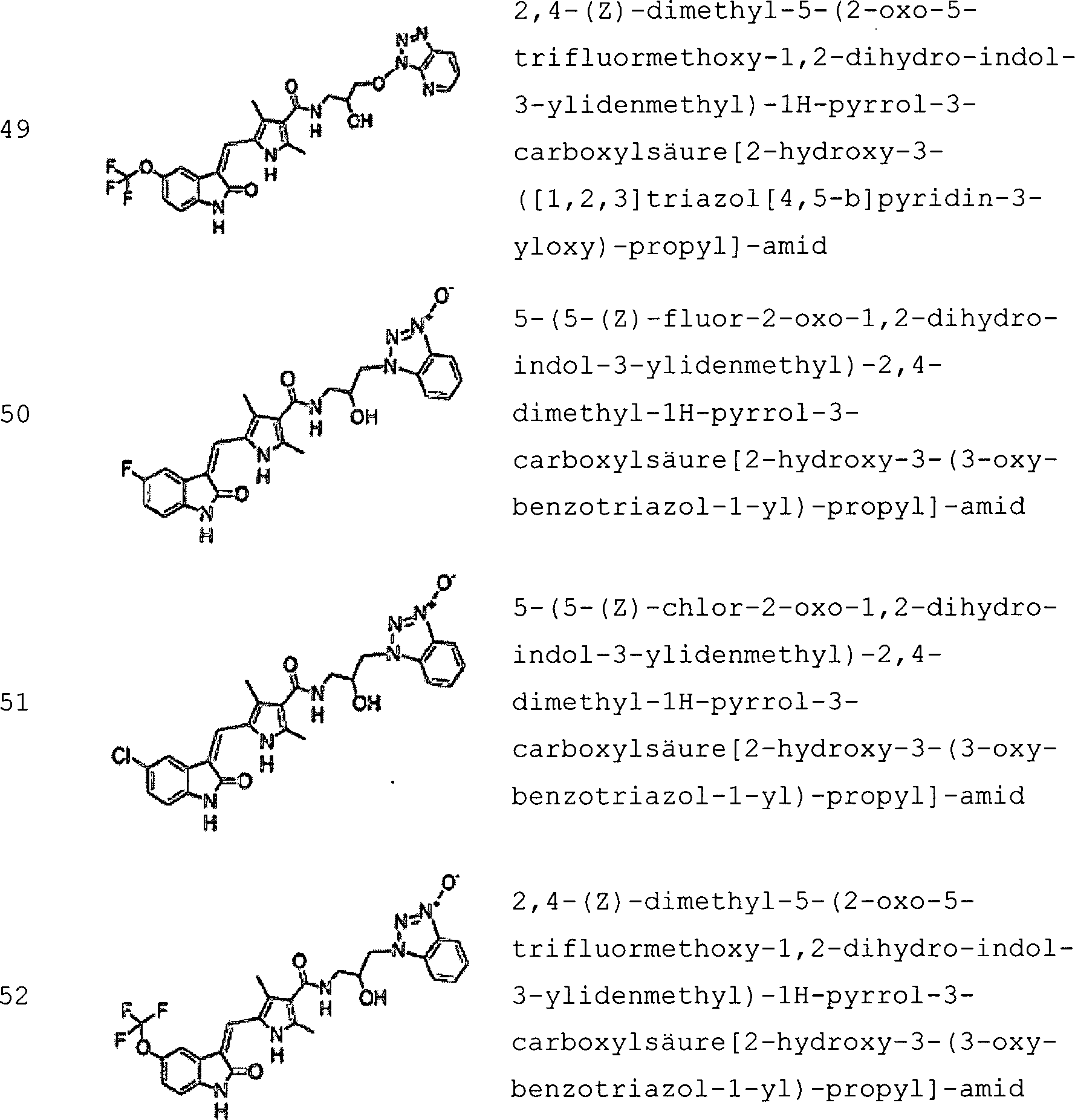
Repräsentative
Verbindungen der vorliegenden Erfindung werden unten in Tabelle
1a gezeigt.
-
-
-
-
-
-
-
-
-
-
-
Andere
repräsentative
Verbindungen der vorliegenden Erfindung werden weiter unten in Tabelle
1b gezeigt.
-
-
-
-
-
-
-
-
-
-
-
-
Die
in den Tabellen 1a–1b
dargestellten Verbindungen sind nur exemplarisch und sollen nicht
dazu dienen den Schutzumfang dieser Erfindung in irgendeiner Art
und Weise zu begrenzen.
-
BEVORZUGTE
AUSFÜHRUNGSFORMEN
-
Während die
breiteste Definition in der Zusammenfassung der Erfindung gegeben
wird, werden bestimmte Verbindungen der Formel (I), die weiter unten
dargestellt werden, bevorzugt.
-
Eine
bevorzugte Gruppe von Verbindungen der Formel (I) ist die, in der:
R6 aus der Gruppe ausgewählt wird, die aus Wasserstoff
und Alkyl, bevorzugt Wasserstoff, Methyl, Ethyl, Isopropyl, tert-Butyl,
Isobutyl oder n-Butyl, noch bevorzugter Wasserstoff oder Methyl
besteht; und
R7 aus der Gruppe ausgewählt wird,
die aus Wasserstoff, Alkyl, Aryl, Heteroaryl und -C(O)R17 besteht,
wobei R17 Hydroxy, Alkyl, Cycloalkyl, Aryl
oder Heteroaryl ist, und noch bevorzugter ist R7 Wasserstoff,
Methyl, Ethyl, Isopropyl, n-, Iso- oder tert-Butyl, Phenyl, Benzoyl,
Acetyl oder Carboxy, am meisten bevorzugt Methyl, Wasserstoff oder
Phenyl.
-
2.
Eine andere bevorzugte Gruppe der Verbindungen der Formel (I) ist
die, in der:
R6 aus der Gruppe ausgewählt wird,
die aus Wasserstoff und Alkyl, bevorzugt Wasserstoff, Methyl, Ethyl,
Isopropyl, tert-Butyl, Isobutyl oder n-Butyl, noch bevorzugter Wasserstoff
oder Methyl, am meisten bevorzugt Methyl besteht;
R7 aus der Gruppe ausgewählt wird, die aus Wasserstoff,
Alkyl, Aryl, Heteroaryl und -C(O)R17 besteht,
wobei R17 Wasserstoff, Alkyl oder Aryl ist,
und R7 noch bevorzugter Wasserstoff, Methyl,
Ethyl, Isopropyl, n-, Iso- oder tert-Butyl, Phenyl, Benzoyl, Acetyl
oder Carboxy, am meisten bevorzugt Methyl, Wasserstoff oder Phenyl
ist; und R3, R4 und
R5 Wasserstoff sind; und
Z Aryl ist.
-
3.
Eine andere bevorzugte Gruppe von Verbindungen der Formel (I) ist
die, in der:
R6 aus der Gruppe ausgewählt wird,
die aus Wasserstoff und Alkyl, bevorzugt Wasserstoff, Methyl, Ethyl,
Isopropyl, tert-Butyl, Isobutyl oder n-Butyl, noch bevorzugter Wasserstoff
oder Methyl, am meisten bevorzugt Methyl besteht;
R7 aus der Gruppe ausgewählt wird, die aus Wasserstoff,
Alkyl, Aryl, Heteroaryl und -C(O)R17 besteht,
wobei R17 Hydroxy, Alkyl oder Aryl ist und
R7 noch bevorzugter Wasserstoff, Methyl,
Ethyl, Isopropyl, n-, Iso- oder tert-Butyl, Phenyl, Benzoyl, Acetyl
oder Carboxy, am meisten bevorzugt Methyl, Wasserstoff oder Phenyl,
am allermeisten bevorzugt Methyl ist; und
R3,
R4 und R5 Wasserstoff
sind; und
Z ein Heteroaryl, bevorzugt Triazinyl, Tetrazolyl,
Imidazolyl, Pyridinyl, Pyrimidinyl oder Pyrazinyl ist.
-
4.
Eine andere bevorzugte Gruppe von Verbindungen der Formel (I) ist
die, in der:
R6 aus der Gruppe ausgewählt wird,
die aus Wasserstoff und Alkyl, bevorzugt Wasserstoff, Methyl, Ethyl,
Isopropyl, tert-Butyl, Isobutyl oder n-Butyl, noch bevorzugter Wasserstoff
oder Methyl, am meisten bevorzugt Methyl besteht;
R7 aus der Gruppe ausgewählt wird, die aus Wasserstoff,
Alkyl, Aryl, Heteroaryl und -C(O)R17 besteht,
wobei R17 Hydroxy, Alkyl oder Aryl ist,
und R7 noch bevorzugter Wasserstoff, Methyl,
Ethyl, Isopropyl, n-, Iso- oder tert-Butyl, Phenyl, Benzoyl, Acetyl
oder Carboxy, am meisten bevorzugt Methyl, Wasserstoff oder Phenyl
ist; und
R3, R4 und
R5 Wasserstoff sind; und
Z heterocyclisch
ist.
-
5.
Eine andere bevorzugte Gruppe von Verbindungen der Formel (I) ist
die, in der:
R6 aus der Gruppe ausgewählt wird,
die aus Wasserstoff und Alkyl, bevorzugt Wasserstoff, Methyl, Ethyl,
Isopropyl, tert-Butyl, Isobutyl, oder n-Butyl, noch bevorzugter
Wasserstoff oder Methyl, am meisten bevorzugt Methyl besteht;
R7 aus der Gruppe ausgewählt wird, die aus Wasserstoff,
Alkyl, Aryl, Heteroaryl und -C(O)R17 besteht,
wobei R17 Hydroxy, Alkyl oder Aryl ist,
und R7 noch bevorzugter Wasserstoff, Methyl,
Ethyl, Isopropyl, n-, Iso- oder tert-Butyl, Phenyl, Benzoyl, Acetyl
oder Carboxy, noch bevorzugter Methyl, Wasserstoff oder Phenyl,
am meisten bevorzugt Methyl ist; und
R3,
R4 und R5 Wasserstoff
sind; und
Z -NR15R16 ist,
wobei R15 und R16 kombiniert
werden, um Heterocycloamino, bevorzugt Piperidin-1-yl, N-Methylpiperidin-1-yl, Piperazin-1-yl,
N-Methylpyrrolidin-1-yl, Pyrrolidin-1-yl, Morpholin-4-yl, Thiomorpholin-4-yl, Thiomorpholin-1-oxid,
Thiomorpholin-1,1-dioxid, 4-Ethyloxycarbonylmethylpiperazin-1-yl, 3-Oxopiperazin-1-yl,
Imidazolidin-1-yl-2-on, Pyrrolidin-1-yl-2-on, Oxohomopiperazin-1-yl
oder Tetrahydropyrimidin-1-yl-2-on, noch bevorzugter Morpholin-4-yl zu bilden.
-
5.
Eine andere bevorzugte Gruppe von Verbindungen der Formel (I) ist
die, in der:
R6 aus der Gruppe ausgewählt wird,
die aus Wasserstoff und Alkyl, bevorzugt Wasserstoff, Methyl, Ethyl,
Isopropyl, tert-Butyl, Iso-butyl oder n-Butyl, noch bevorzugter
Wasserstoff oder Methyl besteht;
R7 aus
der Gruppe ausgewählt
wird, die aus Wasserstoff, Alkyl, Aryl, Heteroaryl und -C(O)R17 besteht, wobei R17 Hydroxy,
Alkyl oder Aryl ist und R7 noch bevorzugter
Wasserstoff, Methyl, Ethyl, Isopropyl, n-, Iso- oder tert-Butyl, Phenyl, Benzoyl,
Acetyl oder Carboxy, am meisten bevorzugt Methyl, Wasserstoff oder
Phenyl ist; und
R3, R4 und
R5 Wasserstoff sind; und
Z -NR15R16 ist, wobei
R15 und R16 Alkyl,
bevorzugt Diethylamino, Dimethylamino oder Ethylamino sind.
-
7.
Innerhalb der oben bevorzugten und noch bevorzugteren Gruppen (1)–(6) ist
eine sogar noch bevorzugtere Gruppe von Verbindungen die, in der:
R1 Wasserstoff, Alkyl, -C(O)NR12R13, unsubstituiertes Cycloalkyl, bevorzugt
Wasserstoff, 3,4-Dimethoxyphenylaminocarbonyl,
4-Methoxy-3-chlorphenylaminocarbonyl, noch bevorzugter Wasserstoff
oder Methyl, am meisten bevorzugt Wasserstoff ist; und
R2 Wasserstoff, Cyano, Halo, ein niederes
Alkoxy oder -S(O)2NR9R10 ist, wobei R9 Wasserstoff
ist und R10 Wasserstoff, Aryl oder Alkyl
ist und in der 5-Position des Oxindolrings liegt, R2 bevorzugt
Wasserstoff, Chlor, Brom, Fluor, Methoxy, Ethoxy, Phenyl, Dimethylaminosulfonyl,
3-Chlorphenylaminosulfonyl, Carboxy, Methoxy, Aminosulfonyl, Methylaminosulfonyl,
Phenylaminosulfonyl, Pyridin-3-yl-aminosulfonyl, Dimethylaminosulfonyl, Isopropylaminosulfonyl,
noch bevorzugter Wasserstoff, Fluor oder Brom ist. Am meisten bevorzugt
ist R2 Fluor und ist in der 5-Position des
Indolinonrings angeordnet. In den oben bevorzugten, noch bevorzugteren
und am meisten bevorzugten Verbindungen ist die Stereochemie am
Kohlenstoffatom, dass die Hydroxy-Gruppe in der -CONHCH(R3)*CR4(OH)CR5Z-Kette trägt und durch ein * angezeigt
wird, entweder RS, R, oder S, noch bevorzugter S.
-
Anwendbarkeit
-
Die
PK's, dessen katalytische
Aktivität
durch die Verbindungen dieser Erfindung moduliert werden, schließen Protein-Tryosinkinasen
ein, von denen es zwei Typen gibt, die Rezeptor-Tyrosinkinasen (RTK's) und die zellulären Tyrosinkinasen
(CTK's) und die
Serin-Threoninkinasen (STK's).
Die RTK vermittelte Signaltransduktion wird durch die extrazelluläre Wechselwirkung
mit einem spezifischen Wachstumsfaktor (Ligand), gefolgt durch eine
Rezeptordimerisierung, transiente Stimulation der intrinsischen
Protein-Tyrosinkinaseaktivität und
einer Phosphorylierung initiiert. Dadurch werden Bindungsstellen
für die
intrazellulären
Signaltransduktionsmoleküle
erzeugt und führen
zur Bildung von Komplexen mit einem Spektrum von cytoplasmatischen
Signalmolekülen,
die die geeignete zelluläre
Antwort (z.B. Zellteilung, metabolische Wirkungen auf die extrazelluläre Mikroumgebung,
etc.) erleichtern. Siehe, Schlessinger und Ullrich, 1992, Neuron
9: 303–391.
-
Es
ist gezeigt worden, dass Tyrosin-Phosphorylierungsstellen
an Wachstumsfaktorrezeptoren als hochaffine Bindungsstellen für SH2 (src
Homolog)-Domäne
von Signalmolekülen
funktionieren. Fantl et al., 1992, Cell 69: 413–423, Songyang et al., 1994,
Mol. Cell. Biol. 14: 2777–2785),
Songyang et al., 1993, Cell 72: 767–778, und Koch et al., 1991,
Science 252: 668–678.
Mehrere intrazelluläre
Substratproteine, die mit RTK's im
Zusammenhang stehen, sind identifiziert worden. Sie können zwei
Hauptgruppen aufgeteilt werden: (1) Substrate, die eine katalytische
Domäne
haben, und (2) Substrate, denen eine solche Domäne fehlt, die jedoch als Adapter
dienen und mit katalytisch aktiven Molekülen im Zusammenhang stehen.
Songyang et al., 1993, Cell 72: 767–778. Die Spezifität der Wechselwirkungen
zwischen den Rezeptoren und den SH2-Domänen ihrer Substrate, wird durch
die Aminosäurereste
bestimmt, die den phosphorylierten Tyrosinrest sofort umgeben. Unterschiede
bei den Bindungsaffinitäten
zwischen SH2-Domänen
und den Aminosäuresequenzen,
die die Phosphotyrosinreste an bestimmten Rezeptoren umgeben, stimmen
mit den beobachteten Unterschieden in ihren Substratphosphorylierungsprofilen überein.
Songyang et al., 1993, Cell 72: 767–778. Diese Beobachtungen legen
nahe, dass die Funktion jeder RTK nicht nur durch die Expressionsmuster
und die Ligandenverfügbarkeit
bestimmt wird, sondern auch durch das Array von stromabwärts liegenden
Signaltransduktionswegen, die durch einen bestimmten Rezeptor aktiviert
werden. Demnach stellt die Phosphorylierung einen wichtigen regulatorischen
Schritt bereit, der die Selektivität von Signalwegen, die sowohl
durch spezifische Wachstumsfaktorrezeptoren als auch durch Differenzierungsfaktorrezeptoren
rekrutiert werden, bestimmt.
-
STK's, die primär cytosolisch
sind, beeinflussen die interne Biochemie der Zelle häufig als Down-Line-Reaktion
auf ein PTK-Ereignis. STK's
sind mit dem Signalprozess, der die DNA-Synthese und die nachfolgende
Mitose, die zur Zellproliferation führt, initiiert, in Verbindung
gebracht wurden.
-
Demnach
führt die
PK-Signaltransduktion, neben anderen Reaktionen, zur Zellproliferation,
Differenzierung, Wachstum und zum Metabolismus. Die abnormale Zellproliferation
kann zu einer großen
Breite von Störungen
und Erkrankungen führen,
die die Entwicklung einer Neoplasie, wie zum Beispiel Krebs, Sarkom, Glioblastom
und Hämangiom,
Erkrankung, wie zum Beispiel Leukämie, Psoriasis, Atherosklerose,
Arthritis und diabetische Retinopathie und andere Störungen,
die mit einer unkontrollierten Angiogenese und/oder Vaskulogenese
zusammenhängen,
einschließen.
-
Ein
genaues Verständnis
des Mechanismus, durch den die Verbindungen dieser Erfindung PK's inhibieren, ist
nicht erforderlich, um die folgende Erfindung auszuführen. Obwohl
man hierdurch jedoch nicht an irgendeinen bestimmten Mechanismus
oder eine Theorie gebunden ist, glaubt man, dass die Verbindungen mit
den Aminosäuren
in der katalytischen Region der PK's interagieren. PK's besitzen üblicherweise eine bilobäre Struktur,
wobei es scheint, dass ATP in der Spalte zwischen den beiden Loben
in einen Bereich bindet, in dem die Aminosäuren unter den PK's konserviert sind.
Man glaubt, dass Inhibitoren von PK's durch nichtkovalente Wechselwirkung,
wie zum Beispiel einer Wasserstoffbrückenbindung, Van-der-Waals-Kräften und
ionischen Wechselwirkungen im gleichen allgemeinen Bereich, in dem
das vorgenannte ATP an die PK's
bindet, binden. Es wird insbesondere angenommen, dass die 2-Indolinon-Komponente
der Verbindungen dieser Erfindung im allgemeinen Raum, der normalerweise
durch den Adeninring des ATP besetzt wird, bindet. Die Spezifität eines
bestimmten Moleküls
für eine
bestimmte PK kann sich dann als ein Ergebnis aus der zusätzlichen Wechselwirkung
zwischen den verschiedenen Substituenten am 2-Indolinonkern und
den Aminosäuredomänen, die
für bestimmte
PK's spezifisch
sind, ergeben. Demnach können
verschiedene Indolinonsubstituenten zur bevorzugten Bindung bestimmter
PK's beitragen.
Die Fähigkeit,
Verbindungen aktiv an verschiedenen ATP (oder anderen Nukleotid)-Bindungsstellen
auszuwählen,
macht die Verbindungen dieser Erfindung für das Ansteuern irgendeines
Proteins mit solch einer Stelle verwendbar. Die hierin offenbarten
Verbindungen weisen daher eine Verwendbarkeit in in vitro Assays
für solche
Proteine auf und zeigen auch in vivo therapeutische Wirkungen durch
die Wechselwirkung mit solchen Proteinen.
-
Zusätzlich stellen
die Verbindungen der vorliegenden Erfindung einen therapeutischen
Ansatz zur Behandlung vieler Arten von festen Tumoren bereit, die
einschließen,
jedoch nicht begrenzt sind auf Karzinome, Sarkome, einschließlich Kaposi's Sarkom, Erythroblastom,
Glioblastom, Meningioma, Astrocytom, Melanom und Myoblastom. Die
Verwendung dieser Verbindungen in einer pharmazeutischen Zusammensetzung
für die Herstellung
eines Arzneimittels zur Behandlung oder zum Verhindern von nicht
festen Tumorkrebsen, wie zum Beispiel Leukämie, wird ebenso von dieser
Erfindung umfasst. Indikationen können einschließen, sind
jedoch nicht begrenzt auf Gehirnkrebs, Blasenkrebs, Ovarialkrebs,
Magenkrebs, Bauchspeicheldrüsenkrebs,
Dickdarmkrebs, Blutkrebs, Lungenkrebs und Knochenkrebs.
-
Weitere
Beispiele, ohne Begrenzung, der Typen von Störungen die mit einer unpassenden
PK-Aktivität
im Zusammenhang stehen, für
die die hierin beschriebenen Verbindungen beim Verhindern, Behandeln
und Studieren verwendet werden könnten,
sind proliferative Störungen
der Zelle, fibrotische Störungen
und metabolische Störungen.
-
Proliferative
Störungen
der Zelle, die man durch die Verwendung der Verbindungen der vorliegenden Erfindung
für die
Herstellung eines Arzneimittels, das gegen diese Störungen gerichtet
ist, verhindern, behandeln oder weiter studieren kann, schließen Krebs,
Störungen
der Blutgefäßproliferation
und mesangiale proliferative Störungen
der Zelle ein.
-
Störungen der
Blutgefäßproliferation
betreffen Störungen,
die mit einer abnormalen Vaskulogenese (Blutgefäßbildung) und Angiogenese (Ausbreitung
von Blutgefäßen) im
Zusammenhang stehen. Während
die Vaskulogenese und die Angiogenese wichtige Rollen bei einer
Vielzahl von normalen physiologischen Prozessen, wie zum Beispiel
der embryonalen Entwicklung, der Corpus Luteum-Bildung, der Wundheilung und der Organregeneration,
spielen, spielen sie auch eine entscheidende Rolle bei der Krebsentwicklung,
bei der sie die Bildung von neuen Kapillaren, die für das Überleben
des Tumors erforderlich sind, zur Folge haben. Andere Beispiele
für Störungen der
Blutgefäßproliferation
schließen
die Arthritis, bei der neue kapillare Blutgefäße in das Gelenk eindringen
und den Knorpel zerstören,
und Augenerkrankungen, wie die diabetische Retinopathie, bei der
neue Kapillaren in der Retina in den Glaskörper eindringen, ausbluten
und Blindheit verursachen, ein.
-
Man
hat zwei strukturell miteinander im Zusammenhang stehende RTK's identifiziert,
die VEGF mit hoher Affinität
binden: der fms-ähnliche
Tyrosin 1 (flt-1)-Rezeptor (Shibuya et al., 1990, Oncogene, 5: 519–524; De
Vries et al., 1992, Science, 255: 989–991) und der KDR/FLK-1-Rezeptor,
auch als VEGF-R2 bekannt. Es wurde berichtet, dass der vaskuläre Endothelwachstumsfaktor
(VEGF) ein Endothelzellenspezifisches Mitogen mit einer Endothelzellenwachstumsfördernden
Aktivität
in vitro ist. Ferrara & Henzel,
1989, Biochein. Biophys. Res. Comm., 161: 851–858; Vaisman et al., 1990,
J. Biol. Chem., 265: 19461–19566.
Die Informationen, die in den U.S. Anmeldungen mit der Ser. Nr.
08/193,829, 08/038,596 und 07/975,750 dargestellt werden, liegen
deutlich nahe, dass VEGF nicht nur für die Endothelzellenproliferation
verantwortlich ist, sondern auch der Hauptregulator für die normale
und pathologische Angiogenese ist. Siehe im Allgemeinen, Klagsburn & Soker, 1993,
Current Biology, 3 (10) 699–702;
Houck, et al., 1992, J. Biol. Chem., 267: 26031–26037.
-
Die
normale Vaskulogenese und Angiogenese spielen wichtige Rollen in
einer Vielzahl von physiologischen Prozessen, wie zum Beispiel der
embryonalen Entwicklung, der Wundheilung, der Organregeneration und
den weiblichen reproduktiven Prozessen, wie zum Beispiel der Follikelentwicklung
im Corpus Luteum während
des Eisprungs und des plazentalen Wachstums nach der Schwangerschaft.
Folkman & Shing,
1992, J. Biological Chem., 267 (16): 10931–34. Die unkontrollierte Vaskulogenese
und/oder Angiogenese ist mit Erkrankungen, wie zum Beispiel Diabetes
als auch mit malignen festen Tumoren, die für das Wachstum von der Vaskularisierung
abhängen,
in Zusammenhang gebracht worden. Klagsburn & Soker, 1993, Current Biology, 3
(10): 699–702;
Folkham, 1991, J. Natl. Cancer Inst., 82: 4–6; Weidner, et al., 1991,
New Engl. J. Med., 324: 1–5.
-
Die
vermutete Rolle des VEGF bei der Endothelzellenproliferation und
Migration während
der Angiogenese und Vaskulogenese, deuten eine wichtige Rolle für den KDR/FLK-1-Rezeptor
in diesen Prozessen an. Erkrankungen wie zum Beispiel Diabetes Mellitus
(Folkman, 198, in XIth Congress of Thrombosis
and Haemostasis (Verstraeta, et al., Hrsg.), S. 583–596, Leuven
University Press, Leuven) und Arthritis als auch das maligne Tumorwachstum
können
sich aus einer unkontrollierten Angiogenese ergeben. Siehe z.B.,
Folkman, 1971, N. Engl. J. Med., 285: 1182–1186. Die Rezeptoren, an die
VEGF spezifisch bindet, sind ein wichtiges und starkes therapeutisches
Ziel für
die Regulation und Modulation der Vaskulogenese und/oder Angiogenese
und einer Vielzahl von ernsten Erkrankungen, die ein abnormales
zelluläres
Wachstum, dass durch solche Prozesse verursacht wird, einschließen. Plowman,
et al., 1994, DN&P,
7(6): 334–339.
Insbesondere die hochspezifische Rolle des KDR/FLK-1-Rezeptors bei der
Gefäßneubildung
machen ihn zu einem Wahlziel für
therapeutische Ansätze
zur Behandlung von Krebs und anderen Erkrankungen, die die unkontrollierte
Bildung von Blutgefäßen einschließen.
-
Daher
stellt die vorliegende Erfindung Verbindungen bereit, die die Tyrosinkinase-Signaltransduktion, die
die KDR/FLK-1-Rezeptor Signaltransduktion einschließt, regulieren
und/oder modulieren können,
um die Angiogenese und/oder Vaskulogenese, das heißt Verbindungen,
die mit dem durch KDR/FLK-1 transduzierten Signal interferieren,
wenn sie durch Liganden, wie zum Beispiel VEGF, aktiviert werden,
zu inhibieren oder zu fördern.
Obwohl man glaubt, dass die Verbindungen der vorliegenden Erfindung
auf einen Rezeptor oder eine andere Komponente entlang des Tyrosinkinase-Signaltransduktionsweges
wirken, so können
sie auch direkt auf die Tumorzellen, die sich aus einer unkontrollierten
Angiogenese ergeben, wirken.
-
Obwohl
sich die Nomenklatur der menschlichen und murinen Gegenstücke des
generischen „flk-I"-Rezeptors unterscheiden,
sind sie in vielen Beziehungen austauschbar. Der murine Rezeptor,
Flk-1, und sein menschliches Gegenstück, KDR, teilen eine Sequenzhomologie
von 93,4% innerhalb der intrazellulären Domäne. Das murine FLK-I bindet
menschliches VEGF ebenfalls mit der gleichen Affinität wie das
Mäuse VEGF, und
wird entsprechend durch den Liganden, der von beiden Spezies abstammt,
aktiviert. Millauer et al., 1993, Cell, 72: 835–846; Quinn et al., 1993, Proc.
Natl. Acad. Sci. USA, 90: 7533–7537.
FLK-1 verbindet sich auch mit und phosphoryliert anschließend Tyrosin
von menschlichen RTK-Substraten
(z.B., PLC-γ oder
p85), wenn es in 293 Zellen (humane embryonale Nierenfibroblasten)
coexprimiert wird.
-
Modelle,
die vom FLK-1-Rezeptor abhängen,
sind daher direkt für
das Verständnis
des KDR-Rezeptors maßgeblich.
Zum Beispiel sind die Verwendung des murinen FLK-1-Rezeptors in
Verfahren, die Verbindungen identifizieren, die den murinen Signaltransduktionsweg
regulieren, direkt bei der Identifikation von Verbindungen, die
verwendet werden können,
um den menschlichen Signaltransduktionsweg zu regulieren, d.h., die
die Aktivität
regulieren, die mit dem KDR-Rezeptor zusammenhängt, anwendbar. Daher können chemische Verbindungen,
die als Inhibitoren für
KDR/FLK-1 in vitro identifiziert worden sind, in geeigneten in vivo-Modellen
bestätigt
werden. Sowohl in vivo Mäuse-
als auch Rattentiermodelle haben gezeigt, dass sie einen außerordentlichen
Wert für
die Untersuchung des klinischen Potenzials von Agenzien, die auf
den KDR/FLK-1 induzierten Signaltransduktionsweg wirken, haben.
-
Demnach
stellt die vorliegende Erfindung Verbindungen bereit, die die Vaskulogenese
und/oder Angiogenese durch Beeinflussen der enzymatischen Aktivität des KDR/FLK-1-Rezeptors und interferieren
mit dem Signal, dass durch KDR/FLK-1 transduziert wird, regulieren,
modulieren und/oder inhibieren. Daher stellt die vorliegende Erfindung
die Verwendung von Zusammensetzungen bereit, die die Verbindungen
der Erfindung für
die Herstellung eines Arzneimittels zur Behandlung von vielen Arten
an festen Tumoren, die einschließen, jedoch nicht begrenzt
sind auf ein Glioblastom, Melanom und Kaposi's Sarkom, und ein Ovarial-, Lungen-, Brust-,
Prostata-, Pankreas-, Dickdarm- und Epidermoidkarzinom. Zusätzlich legen
die Daten die Verwendung von Verbindungen, die den KDR/Flk-1-vermittelten
Signaltransduktionsweg inhibieren, für die Herstellung eines Arzneimittels
zur Behandlung von Hämangiom,
Restenose und diabetische Retinopathie nahe.
-
Darüber hinaus
betrifft diese Erfindung die Inhibierung der Vaskulogenese und Angiogenese
durch andere Rezeptorvermittelte Wege, einschließlich des Weges, der den flt-1-Rezeptor umfasst.
-
Die
Rezeptor-Tyrosinkinase vermittelte Signaltransduktion wird durch
eine extrazelluläre
Wechselwirkung mit einem spezifischen Wachstumsfaktor (Ligand) gefolgt
von einer Rezeptordimerisierung, transienten Stimulation der intrinsischen
Protein-Tyrosinkinaseaktivität
und Autophosphorylierung initiiert. Dadurch werden Bindungsstellen
für intrazellulären Signaltransduktionsmoleküle erzeugt,
die zur Bildung von Komplexen mit einem Spektrum an cytoplasmatischen Signalmolekülen führen, die
die geeignete zelluläre
Reaktion, z.B. Zellteilung und metabolische Wirkungen auf die extrazelluläre Mikroumgebung,
erleichtern. Siehe Schlessinger und Ullrich, 1992, Neuron, 9: 1–20.
-
Die
enge Homologie der intrazellulären
Bereiche des KDR/FLK-1 mit denen des PDGF-β-Rezeptors (50,3% Homologie)
und/oder dem verwandten flt-1-Rezeptor lassen die Induktion der überlappenden
Signaltransduktionswege erkennen. Zum Beispiel ist für den PDGF-β-Rezeptor,
Mitgliedern der src-Familie
(Twamley et al., 1993, Proc. Natl. Acad. Sci. USA, 90: 7696–7700),
der Phosphatidylinositol-3'-Kinase
(Hu et al., 1992, Mol. Cell. Biol., 12: 981–990), der Phospholipase cγ (Kashishian & Cooper, 1993,
Mol. Cell. Biol., 4: 49–51), dem
ras-GTPase-aktivierendem Protein (Kashishian et al., 1992, EMBO
J., 11: 1373–1382),
dem PTP-ID/syp (Kazlauskas et al., 1993, Proc. Natl. Acad. Sci.
USA, 10 90: 6939–6943),
dem Grb2 (Arvidsson et al., 1994, Mol. Cell. Biol., 14: 6715–6726),
und den Adaptermolekülen
Shc und Nck (Nishimura et al., 1993, Mol. Cell. Biol., 13: 6889–6896) gezeigt
worden, dass sie an Bereiche binden, die unterschiedliche Autophosphorylierungsstellen
betreffen. Allgemein siehe Claesson-Welsh, 1994, Prog. Growth Factor
Res., 5: 37–54.
Daher ist es wahrscheinlich, dass die Signaltransduktionswege, die
durch KDR/FLK-1 aktiviert werden, den ras-Weg (Rozakis et al., 1992,
Nature, 360: 689–692),
den PI-3'-Kinase-,
den src vermittelten und den plcγ vermittelten Weg
einschließen.
Jeder dieser Wege kann eine kritische Rolle bei der angiogenen und/oder
vaskulogenen Wirkung von KDR/FLK-1 in Endothelzellen spielen. Folglich
betrifft ein noch weiterer Aspekt dieser Erfindung die Verwendung
der hierin beschriebenen organischen Verbindungen für die Herstellung
eines Arzneimittels, das die Angiogenese und Vaskulogenese moduliert,
da diese Prozesse durch diese Wege kontrolliert werden.
-
Umgekehrt
sind Störungen,
die mit dem Zurückziehen,
der Kontraktion oder dem Verschließen von Blutgefäßen zusammenhängen, wie
zum Beispiel der Restenose, ebenfalls eingeschlossen und können durch die
Verwendung der Verbindungen dieser Erfindung für die Herstellung eines Arzneimittels
daraus behandelt oder verhindert werden.
-
Fibrotische
Störungen
betreffen die abnormale Bildung von extrazellulären Matrizes. Beispiele für fibrotische
Störungen
schließen
die Leberzirrhose und proliferative Störungen mesangialer Zellen ein.
Die Leberzirrhose ist durch die Zunahme an extrazellulären Matrixbestandteilen
gekennzeichnet, die zur Bildung einer Lebernarbe führen. Eine
gesteigerte extrazelluläre
Matrix, die zu einer Lebernarbe führt, kann auch durch eine virale
Infektion, wie zum Beispiel Hepatitis, verursacht werden. Lipocyten
scheinen eine Hauptrolle bei der Leberzirrhose zu spielen. Andere
fibrotische Störungen,
die eingeschlossen sind, schließen
Atherosklerose ein.
-
Proliferative
Störungen
mesangialer Zellen betreffen Störungen,
die durch eine abnormale Proliferation von Mesangialzellen bewirkt
werden. Proliferative Störungen
mesangialer Zellen schließen
verschiedene humane Nierenerkrankungen, wie zum Beispiel Glomerulonephritis,
diabetische Nephropathie und maligne Nephrosklerose als auch solche
Störungen,
wie das thrombotische Mikroangiopathie-Syndrom, die Transplantatabstoßung und
Glomerulopathien, ein. Die RTK PDGFR ist mit der Beibehaltung der
Proliferation mesangialer Zellen in Verbindung gebracht worden.
Floege et al., 1993, Kidney International 43: 47S–54S.
-
Viele
Krebsarten sind proliferative Störungen
mesangialer Zellen und, wie bereits vorher angemerkt, sind PK's mit proliferativen
Störungen
mesangialer Zellen in Verbindung gebracht worden. Daher ist es nicht verwunderlich,
dass PK's, wie zum
Beispiel Mitglieder der RTK-Familie, mit der Entwicklung von Krebs
in Verbindung gebracht worden sind. Einige dieser Rezeptoren, wie
zum Beispiel EGFR (Tuzi et al., 1991, Br. J. Cancer 63: 227–233, Torp
et al., 1992, APMIS 100: 713–719),
HER2/neu (Slamon et al., 1989, Science 244: 707–712) und PDGF-R (Kumabe et
al., 1992, Oncogene, 7: 627–633)
sind in vielen Tumoren überexprimiert und/oder
durch autokrine Schleifen beharrlich aktiviert worden. Tatsächlich sind
bei den üblichsten
und schwerwiegendsten Krebsarten diese Rezeptorüberexpressionen (Akbasak und
Suner-Akbasak et al., 1992, J. Neurol. Sci., 111: 119–133, Dickson
et al., 1992, Cancer Treatment Res. 61: 249–273, Korc et al., 1992, J. Clin.
Invest. 90: 1352–1360)
und autokrinen Schleifen (Lee und Donoghue, 1992, J. Cell. Biol.,
118: 1057–1070,
Korc et al., siehe oben, Akbasak und Suner-Akbasak et al., siehe
oben) gezeigt worden. Zum Beispiel hat man EGFR mit dem glatten
Epithelzellkarzinom, Astrocytom, Glioblastom, Kopf- und Halskrebs,
Lungenkrebs und Blasenkrebs in Verbindung gebracht. HER2 ist mit
Brust-, Ovarial-, Lungen-, Pankreas- und Blasenkrebs in Verbindung gebracht
wurden. PDGFR ist mit Glioblastom und Melanom als auch Lungen-,
Ovarial- und Prostatakrebs in Verbindung gebracht wurden. Die RTK
c-met ist auch mit der malignen Tumorbildung in Verbindung gebracht
worden. Zum Beispiel ist c-met mit, neben anderen Krebsarten, colorektalen,
Thyroid-, Pankreas-, Magen- und hepatozellulären Karzinomen und Lymphomen
in Verbindung gebracht worden. Zusätzlich steht c-met im direkten
Zusammenhang mit Leukämie.
Die Überexpression
des c-met-Gens ist auch in Patienten mit der Hodgkin-Erkrankung
und der Burkitt-Erkrankung detektiert worden.
-
IGF-IR
ist, zusätzlich
dazu, dass es mit der Nahrungsunterstützung und mit Typ II-Diabetes
in Verbindung steht, auch mit zahlreichen Krebstypen in Zusammenhang
gebracht worden. Zum Beispiel hat man IGF-I als einen autokrinen
Wachstumsstimulator mit zahlreichen Tumortypen in Verbindung gebracht,
z.B. menschliche Brustkrebskarzinomzellen (Arteaga et al., 1989,
J. Clin. Invest. 84: 1418–1423)
und kleinen Lungentumorzellen (Macauley et al., 1990, Cancer Res.,
50: 2511–2517).
Zusätzlich
scheint IGF-I, obwohl wesentlich in das normale Wachstum und die
Differenzierung des Nervensystems involviert, auch ein autokriner
Stimulator menschlicher Gliome zu sein. Sandberg-Nordqvist et al., 1993, Cancer Res.
53: 2475–2478.
Die Wichtigkeit von IGF-IR und seiner Liganden bei der Zellproliferation
wird weiterhin durch die Tatsache unterstützt, dass viele Zelltypen in
Kultur (Fibroblasten, Epithelzellen, glatte Muskelzellen, T-Lymphozyten,
Myeloidzellen, Chondrocyten und Osteoblasten (die Stammzellen des
Knochenmarks)) durch IGF-I zum Wachstum stimuliert werden. Goldring
und Goldring, 1991, Eukaryotic Gene Expression, 1: 301–326. Baserga
und Coppola behaupten, dass IGF-IR eine zentrale Rolle im Transformationsmechanismus
spielt und als solcher ein bevorzugtes Ziel für therapeutische Interventionen
für ein
breites Spektrum an bösartigen
Tumoren sein könnte.
Baserga, 1995, Cancer Res., 55: 249–252, Baserga, 1994, Cell 79:
927–930,
Coppola et al., 1994, Mol. Cell. Biol., 14: 4588–4595.
-
STK's sind mit vielen
Krebstypen, einschließlich
und im besonderen Maße
mit Brustkrebs (Cance, et al., Int. J. Cancer, 54: 571–77 (1993))
in Verbindung gebracht wurden.
-
Der
Zusammenhang zwischen der abnormalen PK-Aktivität und einer Erkrankung ist
nicht auf Krebs beschränkt.
Zum Beispiel stehen RTK's
mit Erkrankungen, wie zum Beispiel Psoriasis, Diabetes Mellitus,
Endometriosis, Angiogenese, atheromatöser Beet-Entwicklung, der Alzheimer-Erkrankung,
Restenose, von Hippel-Lindau-Erkrankung, epidermaler Hyperproliferation,
neurodegenerativen Erkrankungen, beschleunigter Makuladegeneration
und Hämangiomen
in Verbindung. Zum Beispiel EGFR bei der kornealen und dermalen Wundheilung
aufgeführt
worden. Defekte beim Insulin-R und IGF-1R weisen auf den Typ II
Diabetes Mellitus hin. Eine vollständigere Zuordnung zwischen
spezifischen RTK's
und ihren therapeutischen Indikationen ist von Plowman et al., 1994,
DN&P 7: 334–339 dargestellt
worden.
-
Wie
zuvor bereits erwähnt,
sind nicht nur RTK's
sondern auch CTK's,
die einschließen,
jedoch nicht begrenzt sind auf src, abl, fps, yes, fyn, lyn, lck,
blk, hck, fgr und yrk (zusammengefasst von Bolen et al., 1992, FASEB
J., 6: 3403–3409)
bei der Proliferation und in metabolischen Signaltransduktionsweg
involviert, und man kann daher erwarten und es ist gezeigt worden,
dass sie in vielen PTK vermittelten Störungen, auf die die vorliegende
Erfindung gerichtet ist, involviert sind. Zum Beispiel wurde gezeigt,
dass mutiertes src (v-src) ein Onkoprotein (pp60v-src)
in Hühnern
ist. Darüber
hinaus überträgt sein
zelluläres
Homolog, das Proto-Onkogen pp60c-src, onkogene
Signale von vielen Rezeptoren. Die Überexpression von EGFR oder
HER2/neu in Tumoren führt
zur konstitutiven Aktivierung von pp60c-src,
das für
maligne Zellen charakteristisch ist, jedoch in normalen Zellen nicht
vorhanden ist. Auf der anderen Seite zeigen Mäuse, die keine Expression von
c-src zeigen, einen osteopetrotischen Phänotyp, was auf eine wichtige
Teilnahme von c-src bei der Osteoklastenfunktion und eine mögliche Beteilung
an verwandten Störungen
hindeutet.
-
Auf
die gleiche Weise wird Zap70 mit der T-Zell-Signalgebung, die mit Autoimmunstörungen in
Verbindung stehen könnte,
in Verbindung gebracht.
-
STK's sind mit Entzündungen,
Autoimmunerkrankungen, Immunantworten und hyperproliferativen Störungen,
wie zum Beispiel Restenose, Fibrose, Psoriasis, Osteoarthritis und
rheumatoider Arthritis in Verbindung gebracht worden.
-
PK's werden auch mit
der Embryoimplantation in Verbindung gebracht. Daher können die
Verbindungen dieser Erfindung ein wirksames Verfahren für das Verhindern
einer solchen Embryoimplantation bereitstellen und dadurch als Geburtskontrollagenzien
nützlich
sein. Zusätzliche
Störungen,
die mittels der Verbindungen dieser Erfindung behandelt oder verhindert
werden können,
sind immunologische Störungen,
wie zum Beispiel eine Autoimmunerkrankung, AIDS und kardiovaskuläre Störungen,
wie zum Beispiel Atherosklerose.
-
Zu
guter Letzt vermutet man derzeit sowohl bei RTK's als auch bei CTK's, dass sie in Hyperimmunstörungen involviert
sind.
-
Verabreichung und pharmazeutische
Zusammensetzung
-
Eine
Verbindung der vorliegenden Erfindung oder ein pharmazeutisch annehmbares
Salz davon kann als solches an einen menschlichen Patienten verabreicht
werden oder kann in pharmazeutischen Zusammensetzungen, in die die
vorgenannten Materialien mit geeigneten Trägern oder einem Hilfsstoff(en)
eingemischt werden, verabreicht werden. Techniken zur Formulierung
und Verabreichung von Arzneimittel können bei „Remington's Pharmacological Sciences", Mack Publishing
Co., Easton, PA., letzte Ausgabe, gefunden werden.
-
Wie
hierin verwendet, betrifft „verabreichen" oder „Verabreichung" die Abgabe einer
Verbindung der Formel (I) oder eines pharmazeutisch geeigneten Salzes
davon oder einer pharmazeutischen Zusammensetzung, die eine Verbindung
der Formel (I) oder ein pharmazeutisch geeignetes Salz davon enthält, diese
Erfindung an einen Organismus zum Zwecke des Verhinderns oder Behandelns
einer mit PK im Zusammenhang stehende Störung.
-
Geeignete
Verabreichungswege, können,
ohne Begrenzung, die orale, rektale, transmukosale, oder intestinale
Verabreichung, oder die intramuskuläre, subkutane, intramedulläre, intrathekale,
direkt intraventrikuläre,
intravenöse,
intravitreale, intraperitoneale, intranasale oder intraokulare Injektion
einschließen.
Die bevorzugten Verabreichungswege sind der orale und der parenterale.
-
Alternativ
dazu kann man die Verbindung eher noch auf lokale als auf systemische
Art und Weise, zum Beispiel durch direkte Injektion der Verbindung
in einen festen Tumor, häufig
in einem Depot oder in einer Formulierung zur langsamen Freisetzung,
verabreichen.
-
Darüber hinaus
kann man das Arzneimittel in einem gezielten Arzneimittelabgabesystem,
zum Beispiel in einem mit einem tumorspezifischen Antikörper beschichtetem
Liposom, verabreichen. Die Liposomen werden auf den Tumor gerichtet
sein und vom Tumor selektiv aufgenommen.
-
Pharmazeutische
Zusammensetzungen der vorliegenden Erfindung können durch im Stand der Technik
gut bekannte Verfahren, z.B. mittels konventioneller Misch-, Auflösungs-,
Granulations-, Drageeherstellungs-, Verreibungs-, Emulsifikations-,
Einkapselungs-, Einschluss- oder Lyophilisierungsverfahren, hergestellt werden.
-
Pharmazeutische
Zusammensetzungen für
die Verwendung gemäß der vorliegenden
Erfindung können
auf konventionelle Art und Weise mittels eines oder mehrerer physiologisch
geeigneter Träger,
die Hilfsstoffe und Zusatzstoffe umfassen, die das Verarbeiten der
aktiven Verbindungen in Zusammensetzungen, die pharmazeutisch verwendet
werden können,
erleichtern, formuliert werden. Die geeignete Formulierung hängt vom
gewählten
Verabreichungsweg ab.
-
Für die Injektion
können
die Verbindungen der Erfindung in wässrigen Lösungen, bevorzugt in physiologisch
kompatiblen Puffern, wie zum Beispiel Hanks'-Lösung,
Ringer-Lösung
oder physiologischer Kochsalzlösung
formuliert werden. Für
die transmukosale Verabreichung können für die zu durchdringende Barriere geeignete
Eindringmittel in der Formulierung verwendet werden. Solche Eindringmittel
sind im Stand der Technik normalerweise gut bekannt.
-
Für die orale
Verabreichung können
die Verbindungen durch das Kombinieren der aktiven Verbindungen
mit pharmazeutisch annehmbaren Trägern, die im Stand der Technik
gut bekannt sind, formuliert werden. Solche Träger erlauben es, die Verbindungen
der Erfindung als Tabletten, Pillen, Pastillen, Dragees, Kapseln, Flüssigkeiten,
Gele, Sirup, Brei, Suspensionen und ähnliches für die orale Nahrungsaufnahme
durch einen Patienten zu formulieren. Pharmazeutische Zubereitungen
für die
orale Verwendung können
mittels eines festen Hilfsstoffs, ggf. Zermahlen der sich ergebenen
Mischung und Verarbeiten der Granulamischung nachdem andere geeignete
Zusatzstoffe, falls gewünscht,
zugegeben wurden, hergestellt werden, um Tabletten oder Drageekerne
zu erhalten. Verwendbare Hilfsstoffe sind besonders Füllmittel,
wie zum Beispiel Zucker, einschließlich Lactose, Sucrose, Manitol
oder Sorbitol, Zellulose-Zubereitungen,
wie zum Beispiel Maisstärke,
Weizenstärke,
Reisstärke
und Kartoffelstärke,
und andere Materialien, wie zum Beispiel Gelatine, Tragantgummi,
Methylzellulose, Hydroxypropylmethylzellulose, Natriumcarboxymethylzellulose
und/oder Polyvinylpyrrolidon (PVP). Falls gewünscht können sich auflösende Agenzien
zugegeben werden, wie zum Beispiel quervernetztes Polyvinylpyrrolidon,
Agar oder Alginsäure.
Ein Salz, wie zum Beispiel Natriumalginat, kann ebenfalls verwendet
werden.
-
Drageekerne
werden mit geeigneten Beschichtungen bereitgestellt. Für diesen
Zweck können
konzentrierte Zuckerlösungen
verwendet werden, die ggf. Gummiarabikum, Talk, Polyvinylpyrrolidon,
Carbopolgel, Polyethylenglycol, und/oder Titandioxid, Lacklösungen,
und geeignete organische Lösungsmittel
oder Lösungsmittelmischungen
enthalten können.
Färbemittel
oder Pigmente können
zu den Tabletten oder Drageebeschichtungen zur Identifikation oder
zum Adressieren verschiedener Kombinationen von aktiven Verbindungsdosen
zugegeben werden.
-
Pharmazeutische
Zusammensetzungen, die oral verwendet werden können, schließen Push-fit-Kapseln,
die aus Gelatine hergestellt werden, als auch weiche, versiegelte
Kapseln, die aus Gelatine und einem Weichmacher, wie zum Beispiel
Glycerol oder Sorbitol, gemacht werden, ein. Die Push-fit-Kapseln
können
die aktiven Inhaltsstoffe als Zusatz zu einem Füllmittel, wie zum Beispiel
Lactose, einem Bindemittel, wie zum Beispiel Stärke, und/oder einem Gleitmittel,
wie zum Beispiel Talk oder Magnesiumstearat und ggf. Stabilisatoren enthalten.
In weichen Kapseln können
die aktiven Verbindungen in geeigneten Flüssigkeiten, wie zum Beispiel fettigen Ölen, flüssigem Paraffin
oder flüssigen
Polyethylenglycolen gelöst
oder suspendiert werden. Stabilisatoren können diesen Formulierungen
ebenfalls zugegeben werden.
-
Pharmazeutische
Zusammensetzungen, die ebenfalls verwendet werden können, schließen harte
Gelatinekapseln ein. Als nicht begrenzendes Beispiel kann die aktive
Verbindungskapsel als orale Arzneimittelproduktformulierung eine
Dosisstärke
von 50 und 200 mg aufweisen. Die beiden Dosisstärken werden aus den gleichen
Granula durch Einführen in
unterschiedlich große
harte Gelatinekapseln der Größe 3 für die 50
mg Kapsel und der Größe 0 für die 200
mg Kapsel hergestellt. Die Zusammensetzung der Formulierung könnte zum
Beispiel so aussehen, wie in Tabelle 2 dargestellt.
-
-
Die
Kapseln können
in braunem Glas oder in Kunststoffflaschen verpackt sein, um die
aktive Verbindung vor dem Licht zu schützen. Die Behälter, die
die Kapsel mit der aktiven Verbindungsformulierung enthalten, müssen bei
geregelter Raumtemperatur (15–30°C) gelagert
werden.
-
Für die Verabreichung
durch Inhalation werden die Verbindungen für die Verwendung gemäß der vorliegenden
Erfindung auf geeignete Weise in Form eines Aerosol-Sprays mittels
eines unter Druck stehenden Behälters
oder eines Zerstäubers
und eines geeigneten Treibmittels, z.B., ohne Begrenzung, Dichlordifluormethan,
Trichlorfluormethan, Dichlortetrafluorethan oder Kohlendioxid, zugeführt. Im
Falle eines unter Druck stehenden Aerosols kann die Dosiseinheit
durch das Bereitstellen eines Ventils zur Abgabe einer abgemessenen Menge
geregelt werden. Kapseln und Patronen aus, zum Beispiel, Gelatine
für die
Verwendung in einem Inhalator oder Insufflator können so formuliert werden,
dass sie eine Pulvermischung der Verbindung und eine geeignete Pulverbasis,
wie zum Beispiel Lactose oder Stärke,
enthalten.
-
Die
Verbindungen können
auch für
die parenterale Verabreichung, z.B. durch Bolus-Injektion oder fortwährende Infusion,
formuliert werden. Formulierungen für die Injektion können in
Dosiseinheitsform, zum Beispiel in Ampullen oder in Multi-Dosis-Behältern, mit
einem zusätzlichen
Konservierungsmittel dargeboten werden. Die Zusammensetzungen können solche
Formeln als Suspensionen, Lösungen
oder Emulsionen in öligen
oder wässrigen
Trägern
aufnehmen und können
Formulierungsmaterialien, wie zum Beispiel Suspensions-, Stabilisierungs-
und/oder Dispersionsagenzien, enthalten.
-
Pharmazeutische
Zusammensetzungen zur parenteralen Verabreichung schließen wässrige Lösung in
einer wasserlöslichen
Form, wie zum Beispiel, ohne Begrenzung, ein Salz, der aktiven Verbindung
ein. Zusätzlich
können
Suspensionen der aktiven Verbindungen in einem lipophilen Vehikel
hergestellt werden. Geeignete lipophile Vehikel schließen fettige Öle, wie
zum Beispiel Sesamöl,
synthetische Fettsäureester,
wie zum Beispiel Ethyloleat und Triglyceride, oder Materialien,
wie zum Beispiel Liposomen, ein. Wässrige Suspensionen für die Injektion
können
Substanzen enthalten, die die Viskosität der Suspension erhöhen, wie
zum Beispiel Natriumcarboxymethylzellulose, Sorbitol oder Dextran. Wahlweise
kann die Suspension auch geeignete Stabilisatoren und/oder Agenzien
enthalten, die die Löslichkeit
der Verbindungen erhöhen,
um die Herstellung von stark konzentrierten Lösungen zu ermöglichen.
-
Alternativ
dazu kann der aktive Inhaltsstoff für die Anordnung mit einem geeigneten
Vehikel, z.B. steriles, pyrogenfreies Wasser, vor der Verwendung
in Pulverform vorliegen.
-
Die
Verbindungen können
auch als rektale Zusammensetzungen, wie zum Beispiel Suppositorien
oder Retentionseinläufe,
mittels, z.B., konventioneller Suppositoriumbasen, wie zum Beispiel
Kakaobutter oder andere Glyceride, formuliert werden.
-
Zusätzlich zu
den zuvor beschriebenen Formulierungen können die Verbindungen auch
als Depotzubereitungen formuliert werden. Solche lang wirkenden
Formulierungen können
durch Implantation (zum Beispiel subkutan oder intramuskulär) oder
durch intramuskuläre
Injektion verabreicht werden. Eine Verbindung dieser Erfindung kann
für diesen
Verabreichungsweg mit geeigneten Polymeren oder hydrophoben Materialien (zum
Beispiel in einer Emulsion mit einem pharmakologisch geeigneten Öl), mit
Ionenaustauschharzen oder als schwer lösliches Derivat, wie zum Beispiel,
ohne Begrenzung, ein schwer lösliches
Salz, formuliert werden.
-
Ein
nicht zur Begrenzung gedachtes Beispiel eines pharmazeutischen Trägers für die hydrophoben Verbindungen
der Erfindung ist ein Verschnittmittelsystem (cosolvent system),
das Benzylalkohol, einen unpolaren oberflächenaktiven Stoff, ein wassermischbares
organisches Polymer und eine wässrige
Phase, wie zum Beispiel das VPD Co-Solvent-System, umfasst. VPD
ist eine Lösung
aus 3% w/v Benzylalkohol, 8% w/v des unpolaren oberflächenaktiven
Stoffes Polysorbat 80 und 65% w/v Polyethylenglycol 300, das mit
absoluten Ethanol auf das Endvolumen aufgefüllt wird. Das VPD Co-Solvent-System
(VPD:D5W) besteht aus VPD, das mit einer 5% Dextrose in Wasser-Lösung auf
1:1 verdünnt
wird. Dieses Co-Solvent-System löst
hydrophobe Verbindungen gut auf und entwickelt selber nach der systemischen
Verabreichung eine geringe Toxizität. Natürlich können die Verhältnisse
eines solchen Co-Solvent-Systems
beträchtlich
variiert werden, ohne seine Löslichkeits-
und Toxizitätscharakteristika
zu zerstören.
Darüber
hinaus kann die Identität
der Co-Solvent-Komponenten variiert werden: Zum Beispiel können andere
gering toxische, unpolare oberflächenaktive Stoffe
anstelle von Polysorbat 80 verwendet werden, die Fraktionsgröße des Polyethylenglycols
kann variiert werden, andere biokompatible Polymere können Polyethylenglycol
ersetzen, z.B. Polyvinylpyrrolidon, und andere Zucker oder Polysaccharide
können
Dextrose ersetzen.
-
Alternativ
dazu können
andere Abgabesystem für
hydrophobe pharmazeutische Verbindungen verwendet werden. Liposomen
und Emulsionen sind gut bekannte Beispiele für Abgabevehikel oder Träger von hydrophoben
Arzneimitteln. Zusätzlich
können
auch bestimmte organische Lösungsmittel,
wie zum Beispiel Dimethylsulfoxid, verwendet werden, obwohl häufig auf
Kosten einer höheren
Toxizität.
-
Zusätzlich können die
Verbindungen mittels eines verzögerten
Freisetzungs-Systems, wie zum Beispiel semipermeable Matrizen aus
festen hydrophoben Polymeren, die das therapeutische Agens enthalten, zugeführt werden.
Verschiedene Materialien zur verzögerten Freisetzung sind etabliert
worden und sind dem Fachmann gut bekannt. Kapseln zur verzögerten Freisetzung
können,
abhängig
von ihrer chemischen Natur die Verbindungen für ein paar Wochen bis zu über 100
Tagen freisetzen. Abhängig
von der chemischen Natur und der biologischen Stabilität des therapeutischen Reagenzes,
können
zusätzliche
Strategien für
die Proteinstabilisierung angewendet werden.
-
Die
pharmazeutischen Zusammensetzungen hierin können auch geeignete Feste oder
Gelphasenträger
oder Hilfsstoffe umfassen. Beispiele für solche Träger oder Hilfsstoffe schließen ein,
sind jedoch nicht begrenzt auf Calciumcarbonat, Calciumphosphat,
verschiedene Zucker, Stärken,
Zellulosederivate, Gelatine und Polymere, wie zum Beispiel Polyethylenglycole.
-
Viele
der PK-modulierenden Verbindungen der Erfindung können als
physiologisch annehmbare Salze bereitgestellt werden, wobei die
beanspruchte Verbindung die negativ oder positiv geladenen Spezies
bilden kann. Beispiele für
Salze, in denen die Verbindung den positiv geladenen Rest bildet,
schließen,
ohne Begrenzung, quaternäres
Ammonium (an anderer Stelle hierin definiert), Salze, wie zum Beispiel
das Hydrochlorid, Sulfat, Carbonat, Lactat, Tartart, Malat, Maleat,
Succinat, ein, wobei das Stickstoffatom der quaternären Ammonium-Gruppe
ein Stickstoff der ausgewählten
Verbindung dieser Erfindung ist, die mit der geeigneten Säure reagiert
hat. Salze, in denen eine Verbindung dieser Erfindung die negativ
geladene Spezies bildet, schließen, ohne
Begrenzung, die Natrium-, Kalium-, Calcium- und Magnesiumsalze ein,
die durch die Reaktion einer Carbonsäure-Gruppe in der Verbindung mit einer geeigneten
Base (z.B. Natriumhydroxid (NaOH), Kaliumhydroxid (KOH), Calciumhydroxid
(Ca(OH)2), etc.) gebildet werden.
-
Pharmazeutische
Zusammensetzungen, die für
die Verwendung in der vorliegenden Erfindung geeignet sind, schließen Zusammensetzungen
ein, in denen die aktiven Inhaltsstoffe in einer Menge enthalten
sind, die ausreichend ist, um den beabsichtigten Zweck, z.B. die
Modulation der PK- Aktivität oder der
Behandlung oder das Verhindern einer mit PK zusammenhängenden
Störung,
enthalten sind.
-
Eine
therapeutisch wirksame Menge bedeutet ganz besonders eine Menge
einer Verbindung, die die Symptome einer Erkrankung verhindern,
sie lindern oder besser werden lässt,
oder das Überleben
des zu behandelnden Subjektes verlängert.
-
Das
Bestimmen einer therapeutisch wirksamen Menge liegt im Rahmen der
Fähigkeiten
eines Fachmanns, besonders im Hinblick auf die hierin bereitgestellte
detaillierte Offenbarung.
-
Für jede Verbindung,
die in dem Verfahren der Erfindung verwendet wird, kann die therapeutisch
wirksame Menge oder Dosis am Anfang aus Zellkulturassays abgeschätzt werden.
Dann kann die Dosis für
die Verwendung in Tiermodellen formuliert werden, um einen Konzentrationsbereich
im Kreislauf zu erhalten, der den in Zellkultur bestimmten IC50 einschließt (d.h. die Konzentration
der Testverbindung, die die Hälfte
der maximalen Inhibierung der PK-Aktivität erzielt). Solche Informationen
können
dann verwendet werden, um eine verwendbare Dosierung in Menschen
genauer bestimmen zu können.
-
Die
Toxizität
und die therapeutische Wirksamkeit der hierin beschriebenen Verbindungen
kann durch pharmazeutische Standardverfahren in Zellkulturen oder
Versuchstieren, z.B., durch Bestimmen des IC50 und des
LD50 (beide werden an anderer Stelle hierin
diskutiert) für
eine betreffende Verbindung bestimmt werden. Die Daten, die von
diesen Zellkulturassays und Tierstudien erhalten werden, können zur
Formulierung eines Dosisbereiches für die Verwendung in Menschen
verwendet werden. Die Dosierung kann abhängig von der angewandten Dosierung
und dem verwendeten Verabreichungsweg variiert werden. Die genaue
Formulierung, der Verabreichungsweg und die Dosis kann durch den
einzelnen Arzt in Hinblick auf den Zustand des Patienten ausgewählt werden.
(Siehe z.B., Fingl, et al., 1975, in „The Pharmacological Basis
of Therapeutics", Kap.
1, S. 1).
-
Die
Dosierungsmenge und das Intervall können individuell angepasst
werden, um die Plasmaniveaus der aktiven Spezies bereitzustellen,
die ausreichend sind, um die Kinasemodulierenden Wirkungen zu erhalten.
Diese Plasmaniveaus werden als minimal wirksame Konzentrationen
(MEC's) bezeichnet.
Die MEC werden für
jede Verbindung variieren, können
jedoch aus in vitro Daten abgeschätzt werden, z.B. kann die Konzentration,
die erforderlich ist, um 50–90%
Inhibierung bei einer Kinase zu erzielen mittels des hierin beschriebenen
Assays bestimmt werden. Dosierungen, die für das Erzielen der MEC notwendig
sind, werden von individuellen Charakteristika und dem Verabreichungsweg
abhängen.
HPLC-Assays oder
Bioassays können
verwendet werden, um die Plasmakonzentrationen zu bestimmen.
-
Dosierungsintervalle
können
ebenfalls mittels des MEC-Wertes
bestimmt werden. Verbindungen sollten unter Verwendung eines Systems
verabreicht werden, dass die Plasmaniveaus für 10–90% der Zeit, bevorzugt zwischen
30–90%
und am meisten bevorzugt zwischen 50–90% über dem MEC hält.
-
Zurzeit
können
die therapeutisch wirksamen Mengen der Verbindungen der Formel I,
Ia oder II von etwa 25 mg/m2 bis 1500 mg/m2 pro Tag, bevorzugt etwa 3 mg/m2/Tag
variieren. Noch bevorzugter von 50 mg/qm qd bis 400 mg/qd.
-
Im
Falle der lokalen Verabreichung oder der selektiven Aufnahme kann
die wirksame lokale Konzentration des Arzneimittels nicht mit der
Plasmakonzentration in Verbindung gebracht werden und andere im Stand
der Technik bekannte Verfahren können
angewendet werden, um die korrekte Dosierungsmenge und das Intervall
zu bestimmen.
-
Die
Menge einer verabreichten Zusammensetzung wird natürlich vom
zu behandelnden Subjekt, der Schwere der Krankheit, der Art und
Weise der Verabreichung, des Urteils des verschreibenden Arztes,
etc. abhängen.
-
Die
Zusammensetzungen können,
falls erwünscht,
in einem Paket oder einer Dispenservorrichtung, wie zum Beispiel
einem durch das FDA anerkannten Kit, das eine oder mehrere Dosiseinheitsformen,
die den aktiven Inhaltsstoff enthalten, enthalten können, dargeboten
werden. Das Paket kann zum Beispiel eine Metall- oder Kunststofffolie,
wie zum Beispiel eine Blisterpackung, umfassen. Dem Paket oder der
Dispenservorrichtung können
Instruktionen zur Verabreichung beiliegen.
-
Dem
Paket oder dem Dispenser kann auch eine Notiz beiliegen, die mit
dem Behälter
in einer Form zusammenliegt, die durch eine Regierungsorganisation,
die die Herstellung, Verwendung oder den Verkauf von Arzneimitteln
reguliert, vorgeschrieben wird, wobei die Notiz die Zulassung durch
die Organisation, die Form der Zusammensetzungen, oder ob zur menschlichen
oder veterinären
Verabreichung widerspiegelt. Eine solche Notiz kann zum Beispiel
ein Schild sein, genehmigt durch die U.S. Food and Drug Administration
für verschreibungspflichtige
Arzneimittel oder eines genehmigten Produktinserts. Zusammensetzungen,
die eine Verbindung der Erfindung umfassen, die in einem kompatiblen
pharmazeutischen Träger
formuliert wurden, können
ebenfalls hergestellt werden, in einem geeigneten Behälter angeordnet
werden und für
die Behandlung eines angegebenen Zustandes ausgezeichnet werden.
Geeignete Zustände
auf die auf dem Schild hingewiesen wird, können die Behandlung eines Tumors,
die Inhibition der Angiogenese, die Behandlung der Fibrose, Diabetes
und ähnliches
einschließen.
-
Die
vorliegende Erfindung kann mit einem CMC-Suspensionsvehikel verabreicht werden.
Eine beispielhafte CMC-Suspension ist unten in Tabelle 3 aufgelistet. Tabelle
3
- * abhängig
von der erforderlichen Konzentration (Datum)
-
Ein
Protokoll für
1,0 l des CMC-Suspensionsvehikels sieht wie folgt aus. Man berechne
die geeignete Menge an Hilfsstoffen, die für das Herstellen der Vehikelformulierung
erforderlich sind, unter Verwendung der Tabelle, die die Zusammensetzung
der Vehikelformulierung und der Batch-Größe zeigt. Man wiege einen geeigneten
leeren Behälter,
wie zum Beispiel eine saubere weithalsige Glasflasche oder eine
Polyethylenflasche, ab. Man gebe etwa 600 ml Wasser in den Behälter. Man
wiege Carboxymethylzellulose-Natrium (5 g) ab und übertrage
sie in den Behälter.
Man rühre
mittels eines magnetischen Rührfisches
oder eines Laborrührers
mit Propeller bis zur Homogenität
(etwa 2–3
Stunden). Man wiege NaCl ab und gebe in den Behälter. Man setze das Mischen
fort bis es aufgelöst
ist (etwa 10 min). Man gebe Polysorbat-80 zu. Mische bis die Lösung homogen
ist (etwa 20 min). Man gebe Benzylalkohol zu. Mische bis die Lösung homogen
ist (etwa 10 min). Man gebe das verbleibende Wasser zu, um das Gewicht
der Lösung
auf die erforderliche Batch-Größe zu bringen, entweder nach
Gewicht oder Volumen (1010 g oder 1000 ml, Dichte bei 22°C ist 1,01).
Man lagere sie bei 2–8°C (unter
Kühlung).
-
Die
Suspensionsformulierung kann wie folgt hergestellt werden. Man zerreibe
die API mittels eines Mörsers
und eines Pistills, um ein homogen aussehendes Pulver mit kleiner
Teilchengröße (keine
großen
Stücke
oder große
Teilchen – idealer
weise sollte es durch ein US-Standardsieb > 80, d.h. < 180 μm Größe passen) zu erhalten. Man
wiege die berechnete Menge an API in den Behälter. Man gebe etwa 90% der
insgesamt erforderlichen Menge an (CMC-Suspensionsvehikel) in den
Behälter.
Man suspendiere die Verbindungen mittels eines Laborrührers mit
Propeller oder einem Äquivalent
in das Vehikel. Der Durchmesser der Propellerblätter sollte dem Durchmesser
des Bodens des Behälters
entsprechen, um ein effizientes Vermischen sicherzustellen. Man
rühre bei
50 rpm für
30 min oder bis das Arzneimittel gut suspendiert ist. Man gebe die
Vehikelformulierung bis „qs" zu (mit Wasser auffüllen) (Qualität ausreichend
(quality sufficient)), bis zum geeigneten Gewicht entsprechend der
Batch-Größe. Man
rühre bei
50 rpm für
zusätzliche
30 min und aliquotiere die Suspension sofort in Bernsteinfarben
gefärbtes
Glas oder in Polypropylenbehälter.
Die Behälter
sollten vor dem Licht geschützt
werden. Man rühre
bei 2–8°C (unter
Kühlung,
nicht einfrieren).
-
Es
ist auch ein Aspekt dieser Erfindung, dass eine hierin beschriebene
Verbindung oder ihr Salz oder Arzneimittelvorstufe mit anderen chemotherapeutischen
Agenzien für
die Behandlung von weiter oben diskutierten Erkrankungen und Störungen kombiniert
werden kann. Zum Beispiel kann eine Verbindung, ein Salz oder eine
Arzneimittelvorstufe dieser Erfindung mit alkylierenden Agenzien,
wie zum Beispiel Fluoruracil (5-FU) alleine oder in weiterer Kombination
mit Leukovorin, oder anderen alkylierenden Agenzien, wie zum Beispiel,
ohne Begrenzung, andere Pyrimidinanaloga, wie zum Beispiel UFT,
Capecitabin, Gemcitabin und Cytarabin, den Alkylsulfonaten, z.B.
Busulfan (wird bei der Behandlung von chronischer granulocytärer Leukämie verwendet),
Improsulfan und Piposulfan; Aziridine, z.B. Benzodepa, Carboquone,
Meturedepa und Uredepa; Ethyleniminen and Methylmelaminen, z.B.
Altretamin, Triethylenmelamin, Triethylenphosphoramid, Triethylenthiophosphoramid
und Trimethylolmelamin; und den Stickstoff-Lost, z.B., Chlorambucil
(wird zur Behandlung von chronischer lymphocytischer Leukämie, primärer Makroglobulinämie und
Non-Hodgkin-Lymphom verwendet), Cyclophosphamid (wird zur Behandlung
der Hodgkin-Erkrankung, eines multiplen Myeloms, eines Neuroblastom,
von Brustkrebs, Ovarialkrebs, Lungenkrebs, Wilm's-Tumor und Rhabdomyosarkom verwendet),
Estramustin, Ifosfamid, Novembrichin, Prednimustin und Uracil-Lost
(wird zur Behandlung von primärer Thrombocytose,
Non-Hodgkin-Lymphom, Hodgkin-Erkrankung
und Ovarialkrebs verwendet), und Triazine, z.B. Dacarbazin (wird
bei der Behandlung eines Weichgewebesarkoms verwendet), kombiniert
werden.
-
Eine
Verbindung, ein Salz oder eine Arzneimittelvorstufe dieser Erfindung
kann auch in Kombination mit anderen antimetabolischen chemotherapeutischen
Agenzien, wie zum Beispiel, ohne Begrenzung, Folsäureanaloga,
z.B. Methotrexat (wird bei der Behandlung von akuter lymphocytischer
Leukämie,
Choriokarzinom, Mykose-Brustkrebs, Kopf- und Halskrebs und osteogenem
Sarkom verwendet) und Pteropterin; und den Purinanaloga, wie zum
Beispiel Mercaptopurin und Thioguanin, die eine Verwendung bei der
Behandlung von akuter granulocytärer,
akuter lymphocytischer und chronisch granulocytärer Leukämie finden, verwendet werden.
-
Es
wird in Erwägung
gezogen, dass eine Verbindung, ein Salz oder eine Arzneimittelvorstufe
dieser Erfindung auch in Kombination mit auf natürlichen Produkten basierenden
chemotherapeutischen Agenzien, wie zum Beispiel, ohne Begrenzung,
Vinca-rosea-Alkaloide, z.B. Vinblastin (wird bei der Behandlung
von Brust- und Hodenkrebs verwendet), Vincristin und Videsin; den
Epipodophylotoxinen, z.B. Etoposid und Teniposid, beide sind bei
der Behandlung von Hodenkrebs und Kaposi-Sarkom verwendbar; die
antibiotischen, chemotherapeutischen Agenzien, z.B. Daunorubicin,
Doxorubicin, Epirubicin, Mitomycin (wird zum Behandeln von Magen-,
Cervix-, Dickdarm-, Brust-, Blasen- und Pankreaskrebs verwendet),
Dactinomycin, Temozolomid, Plicamycin, Bleomycin (wird bei der Behandlung
von Haut-, Speiseröhren-
und Urugenitaltraktkrebs verwendet); und den enzymatischen, chemotherapeutischen
Agenzien, wie zum Beispiel L-Asparaginase,
verwendet werden kann.
-
Zusätzlich zum
oben genannten, könnte
eine Verbindung, ein Salz oder eine Arzneimittelvorstufe dieser
Erfindung auch in Kombination mit Platin koordinierten Komplexen
(Cisplatin, etc.), substituierten Harnstoffe, wie zum Beispiel Hydroxyharnstoff;
Methylhydrazinderivaten, z.B., Procarbazin; Adrenokortikal-Suppressoren,
z.B., Mitotan, Aminoglutethimid; und einem Hormon und Hormonantagonisten,
wie zum Beispiel dem Adrenocorticosteriod (z.B., Prednison), Progestine
(z.B. Hydroxyprogesteroncaproat), Östrogene (z.B. Diethylstilbesterol),
Antiöstrogene,
wie zum Beispiel Tamoxifen; Androgene, z.B. Testosteronpropionat;
und Aromataseinhibitoren, wie zum Beispiel Anastrozol, verwendet
werden.
-
Es
wird letztlich auch in Erwägung
gezogen, dass die Kombination einer Verbindung dieser Erfindung mit
Mitoxantron, Paclitaxel, Cyclooxygenase-2-Inhibitoren, die im Stand
der Technik bekannt sind, besonders Celebrex®, Paracoxib®,
Vioxx®,
Abbott's Cox-189,
das in der PCT-Veröffentlichung
Nr. WO 99/11605 offenbart ist, Topoiosmeraseinhibitoren, wie zum
Beispiel Camptosar®, einem Her-2-Rezeptorantagonisten,
wie zum Beispiel Herceptin®, Endostatin, Gleevac®,
einem ImClone VEGF-Rezeptorantagonisten IMC C225® für die Behandlung
von festen Tumoren oder Leukämien,
wie zum Beispiel, ohne Begrenzung, akuter myelogener (nicht-lymphocytischer)
Leukämie,
wirksam sein wird.
-
Allgemeines Syntheseverfahren
-
Die
folgende allgemeine Methodik kann angewendet werden, um die Verbindungen
dieser Erfindung herzustellen:
Das entsprechend substituierte
2-Oxindol (1 Äquiv.),
das entsprechend substituierte 3-Carboxy-5-formylpyrrol (1,2 Äquiv.) und
eine Base (0,1 Äquiv.)
werden in einem Lösungsmittel
(1–2 ml/mmol
2-Oxindol) zusammengemischt, und die Mischung wird dann von etwa
2 bis etwa 12 Stunden erhitzt. Nach dem Abkühlen wird das Präzipitat,
das sich bildet, gefiltert, mit kaltem Ethanol oder Ether gewaschen
und vakuumgetrocknet, um das entsprechende 5-(2-Oxo-1,2-dihydroindol-(3Z)-ylidenmethyl)-1-H-pyrrol-3-carbonsäure zu bekommen.
Wenn sich kein Präzipitat
bildet, wird die Reaktionsmischung auf konzentriert und der Rest
wird mit Dichlormethan/Ether zerrieben, der sich daraus ergebende
Feststoff wird durch Filtration gesammelt und dann getrocknet. Das
Produkt kann wahlweise durch Chromatographie weiter gereinigt werden.
-
Die
Base kann eine organische oder anorganische Base sein. Wenn eine
organische Base verwendet wird, ist es bevorzugt eine Stickstoffbase.
Beispiele für
organische Stickstoffbasen schließen ein, sind jedoch nicht
begrenzt auf Diisopropylamin, Trimethylamin, Triethylamin, Anilin,
Pyridine, 1,8-Diazabicyclo[5.4.1]undec-7-en, Pyrrolidin und Piperidin.
-
Beispiele
für anorganische
Basen sind, ohne Begrenzung, Ammoniak, Alkalimetall oder Erdalkalihydroxide,
Phosphate, Carbonate, Bicarbonate, Bisulfate und Amide. Die Alkalimetalle
schließen
Lithium, Natrium und Kalium ein, während die Erdalkalien, Calcium,
Magnesium und Barium einschließen.
-
In
einer derzeit bevorzugten Ausführungsform
dieser Erfindung ist, wenn das Lösungsmittel
ein protisches Lösungsmittel
ist, wie zum Beispiel Wasser oder Alkohol, die Base ein Alkalimetall
oder eine anorganische Erdalkalibase, bevorzugt ein Alkalimetall
oder ein Erdalkalihydroxid.
-
Für den Fachmann
wird deutlich sein, welche Base, basierend sowohl auf den bekannten
allgemeinen Prinzipien der organischen Synthese als auch den Offenbarungen
hierin, für
die eingehend betrachtete Reaktion die geeignetste sein würde.
-
Das
Lösungsmittel,
in dem die Reaktion durchgeführt
wird, kann ein protisches oder ein aprotisches Lösungsmittel sein, bevorzugt
ist es ein protisches Lösungsmittel.
Ein „protisches
Lösungsmittel" ist ein Lösungsmittel,
das ein Wasserstoffatom(e) aufweist, das/die kovalent an Sauerstoff- oder Stickstoffatome
gebunden ist/sind, die die Wasserstoffatome zusehends sauer machen
und daher in die Lage versetzen, mit einer gelösten Substanz durch Wasserstoffbrückenbindung „geteilt
zu werden". Beispiele
für protische
Lösungsmittel
schließen,
ohne Begrenzung, Wasser und Alkohol ein.
-
Ein „aprotisches
Lösungsmittel" kann polar oder
nichtpolar sein, enthält
jedoch in beiden Fällen
keine sauren Wasserstoffe und kann daher keine Wasserstoffbrückenbindung mit
gelösten
Substanzen eingehen. Beispiele, ohne Begrenzung, von nichtpolaren
aprotischen Lösungsmitteln
sind Pentan, Hexan, Benzen, Toluen, Methylenchlorid und Kohlenstofftetrachlorid.
Beispiele für
polare aprotische Lösungsmittel
sind Chloroform, Tetrahydrofuran, Dimethylsulfoxid und Dimethylformamid.
-
In
einer derzeit bevorzugten Ausführungsform
dieser Erfindung ist das Lösungsmittel
ein protisches Lösungsmittel,
bevorzugt Wasser oder ein Alkohol, wie zum Beispiel Ethanol.
-
Die
Reaktion wird bei einer Temperatur von größer als Raumtemperatur durchgeführt. Die
Temperatur liegt im Allgemeinen bei etwa 30°C bis etwa 150°C, bevorzugt
bei etwa 80°C
bis etwa 100°C,
am meisten bevorzugt etwa 60°C
bis etwa 85°C,
was über
dem Siedepunkt von Ethanol liegt. Mit „etwa" ist gemeint, dass der Temperaturbereich
bevorzugt innerhalb von 10 Grad Celsius zur angegebenen Temperatur,
noch bevorzugter innerhalb von 5 Grad Celsius zur angegebenen Temperatur
und am meisten bevorzugt innerhalb von 2 Grad Celsius zur angegebenen
Temperatur liegt. Daher ist zum Beispiel mit „etwa 75°C" 75°C ± 10°C, bevorzugt 75°C ± 5°C und am
meisten bevorzugt 75°C ± 2°C gemeint.
-
2-Oxindole
und 3-Carboxy-5-formylpyrrol kann einfach mittels im Stand der chemischen
Technik gut bekannter Verfahren unter Verwendung von einfach erhältlichen
Ausgangsmaterialien synthetisiert werden.
-
Das
Verkuppeln einer 5-(2-Oxo-1,2-dihydroindol-(3Z)-ylidenmethyl)-1-H-pyrrol-3-carbonsäure mit
einem Amin der Formel ZCH(R5)-CR4(OH)-CHR3NH2 in einem organischen Lösungsmittel, wie zum Beispiel
Dimethylformamid, Tetrahydrofuran und ähnlichen und in Gegenwart eines
geeigneten Verkopplungsagens, wie zum Beispiel Dicyclohexylcarbodiimid,
DEAD, EDC und HOBt, stellt dann eine Verbindung der Formel (I) bereit.
Amine der Formel ZCH(R5)- CR4(OH)-CHR3NH2 sind kommerziell
erhältlich
oder sie können
durch im Stand der Technik bekannte Verfahren hergestellt werden.
Einige solcher Prozeduren werden hierin weiter unten beschrieben.
-
Der
Fachmann wird erkennen, dass andere synthetische Wege zum Bilden
der Verbindungen der Erfindung verfügbar sind und dass das nachfolgende
als Beispiel und nicht zur Begrenzung dargeboten wird.
-
BEISPIELE
-
Die
folgenden Zubereitungen und Beispiele werden dargelegt, um den Fachmann
in die Lage zu versetzen, die vorliegende Erfindung einfacher zu
verstehen und auszuführen.
Sie sollten. nicht zur Begrenzung der Erfindung angesehen werden,
sondern lediglich zur Illustration und Darstellung davon.
-
Synthesebeispiele
-
Beispiel 1
-
Synthese von 5-[5-Fluor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure
-
Schritt 1
-
Dimethylformamid
(25 ml, 3 Äq.)
wurde unter Rühren
in einem Eisbad abgekühlt.
Dazu wurde POCl3 (1,1 Äq., 10,8 ml) gegeben. Nach
30 Minuten wurde eine Lösung
aus 3,5-Dimethyl-4-ethylesterpyrrol
(17,7 g, 105,8 mmol) in DMF (2 M, 40 ml) zum Reaktionsansatz gegeben
und das Rühren
fortgesetzt. Nach 2 Stunden wurde der Reaktionsansatz mit Wasser
(250 ml) verdünnt
und mit 1 N wässriger
NaOH auf pH = 11 basisch eingestellt. Der weiße Feststoff wurde durch Filtration
entfernt, mit Wasser und dann Hexanen gewaschen und getrocknet,
um 5-Formyl-2,4-dimethyl-1H-pyrrol-3- carbonsäureethylester (19,75 g, 95%)
als einen gelbbraunen Feststoff hervorzubringen. 1H
NMR (360 MHz, DMSO-d6) δ 12,11
(br s, 1H, NH), 9,59 (s, 1H,
CHO), 4,17 (q, J = 6,7 Hz,
2H, OCH 2CH3), 2,44 (s, 3H, CH 3), 2,40 (s, 3H,
CH 3),
1,26 (d, J = 6,7 Hz, 3H, OCH2CH 3).
-
Schritt 2
-
5-Formyl-2,4-dimethyl-1H-pyrrol-3-carbonsäureethylester
(2 g, 10 mmol) wurde zu einer Lösung
aus Kaliumhydroxyd (3 g, 53 mmol), die in Methanol (3 ml) und Wasser
(10 ml) aufgelöst
wurde, gegeben. Man ließ die
Mischung für
3 Stunden refluxieren, auf Raumtemperatur abkühlen und säuerte sie mit 6 N Salzsäure auf pH
3 an. Der Feststoff wurde durch Filtration gesammelt, mit Wasser
gewaschen und in einem Vakuumofen über Nacht getrocknet, um 5-Formyl-2,4-dimethyl-1H-pyrrol-3-carbonsäure (1,6
g, 93%) zu erhalten. 1H NMR (300 MHz, DMSO-d6) δ 12,09 (s,
br, 2H, NH & COOH),
9,59 (s, 1H, CHO), 2,44 (s, 3H, CH3), 2,40
(s, 3H, CH3).
-
Schritt 3
-
5-Fluorisatin
(8,2 g, 49,7 mmol) wurde in 50 ml Hydrazinhydrat gelöst und für 1 Stunde
refluxiert. Die Reaktionsmischungen wurden dann in Eiswasser gegossen.
Das Präzipitat
wurde dann gefiltert, mit Wasser gewaschen und in einem Vakuumofen
getrocknet, um 5-Fluor-2-oxindol (7,5 g) zu erhalten.
-
Schritt 4
-
Die
Reaktionsmischung aus 5-Fluoroxindol (100 mg, 0,66 mmol), 5-Formyl-2,4-dimethyl-1H-pyrrol-3-carbonsäure (133
mg, 0,79 mmol) und 10 Tropfen Piperidin in Ethanol (3 ml) wurde
bei 60°C über Nacht gerührt und
gefiltert. Der Feststoff wurde mit 1 M wässriger Hydrochloridlösung und
Wasser gewaschen und getrocknet, um 5-(5-Fluor-2-oxo-1,2-dihydroindol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (201 mg,
quantitativ) als einen gelben Feststoff, zu erhalten. MS m/z (relative
Intensität,
%) 299 ([M – 1]+, 100).
-
Beispiel 2
-
Synthese von 5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure(3-Diethylamino-2-hydroxy-propyl)-amid
-
Schritt 1
-
Zu
2-Chlormethyloxiran (95 g, 1,03 mol) wurde bei 30°C eine Mischung
aus Wasser (3,08 g, 0,17 mol) und Diethylamin (106,2 ml, 1,03 mol)
gegeben. Die Reaktionsmischung wurde dann bei 28–35°C für 6 Stunden gerührt und
auf 20–25°C abgekühlt, um
1-Chlor-3-diethylamino-propan-2-ol zu erhalten.
-
Schritt 2
-
Zu
einer Lösung
aus Natriumhydroxid (47,9 g, 1,2 mol) in 78 ml Wasser wurde 1-Chlor-3-diethylamino-propan-2-ol
gegeben. Das Endprodukt daraus wurde bei 20–25°C für 1 Stunde gerührt, mit
178 ml Wasser verdünnt
und zweimal mit Ether extrahiert. Die kombinierte Etherlösung wurde
mit festem Kaliumhydroxid getrocknet und verdampft, um 135 g des
Rohproduktes zu erhalten, das durch fraktionierte Destillation gereinigt wurde,
um reines Glycidyldiethylamin (98 g, 76%) als Öl zu erhalten.
-
Schritt 3
-
Zur
eiskalten Lösung
aus Ammoniumhydroxid (25 ml, 159 mmol) aus 25% (w/w) wurde Glycidyldiethylamin
tropfenweise (3,2 g, 24,8 mmol) über
10 Minuten zugegeben. Die Reaktionsmischung wurde bei 0–5°C für 1 Stunde
und dann bei Raumtemperatur für
14 Stunden gerührt.
Die sich daraus ergebende Reaktionsmischung wurde verdampft und
destilliert (84–90°C bei 500–600 mT),
um 1-Amino-3-diethylamino-propan-2-ol (3,3 g, 92%) zu erhalten. MS m/z
147 ([M + 1]+).
-
Schritt 4
-
Zur
Lösung
aus 5-Formyl-2,4-dimethyl-1H-pyrrol-3-carbonsäure (100 mg, 0,43 mmol), EDC
(122,7 mg, 0,64 mmol) und HOBt (86,5 mg, 0,64 mmol) in 1,0 ml DMF
wurden 1-Amino-3-diethylamino-propan-2-ol (93,2
mg, 0,64 mmol) gegeben. Die sich daraus ergebende Reaktionslösung wurde
bei Raumtemperatur über Nacht
gerührt
und verdampft. Der Rückstand
wurde in 10 ml Wasser suspendiert und filtriert. Der Feststoff wurde
mit gesättigtem
Natriumbicarbonat und Wasser gewaschen und in einem Vakuumofen Übernacht
getrocknet, um das Rohprodukt zu erhalten, das mittels Säulenchromatographie,
wobei es mit 6% Methanol-Dichlormethan,
das Triethylamin (2 Tropfen/100 ml an 6% Methanol-Dichlormethan)
enthält,
eluiert wurde, gereinigt wurde, um 5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure(3-diethylamino-2-hydroxy-propyl)-amid
(62 mg, 34%) als einen gelben Feststoff zu erhalten. 1H
NMR (400 MHz, DMSO-d6) δ 13,70
(s, 1H, NH-1'),
10,90 (s, 1H, NH-1), 7,76 (dd, J = 2,38, 9,33 Hz, 1H, H-4), 7,72
(s, 1H, vinyl-H), 7,60 (m, br., 1H, CONHCH2CH(OH)CH2N(C2H5)2-4'),
6,93 (dt, J = 2,38, 8,99 Hz, 1H, H-5), 6,85 (dd, J = 4,55, 8,99
Hz, 1H, H-6), 3,83 (m, br, 1H, OH), 3,33 (m, 4H), 2,67 (m, br, 5H),
2,46 (s, 3H, CH3), 2,44 (s, 3H, CH3), 1,04 (m, br, 6H, CH3 × 2). MS
m/z (relative Intensität,
%) 427 ([M + 1]+, 100).
-
Beispiel 3
-
Synthese von 5-[5-Fluor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
-
Schritt 1
-
Eine
Mischung aus Morpholin (2,6 ml, 30 mmol) und Epichlorhydrin (2,35
ml, 30 mmol) in Ethanol (50 ml) wurde Übernacht bei 70°C gerührt. Nach
dem Entfernen des Lösungsmittels
wurde der Rückstand
mit Methylenchlorid (50 ml) verdünnt.
Der klare präzipitierte
Feststoff wurde durch Vakuumfiltration gesammelt, um 1-Chlor-3-morpholin-4-yl-propan-2-ol (2,0
g, 37%) zu erhalten. 1H NMR (DMSO-d6) δ 3,49
(t, J = 4,8 Hz, 2H), 3,60 (t, J = 4,6 Hz, 2H), 3,75 (m, 4H, 2 × CH2), 4,20 (dd, J = 5,2, 12 Hz, 2H), 4,54 (m,
2H), 4,62 (m, 1H, CH), 6,64 (d, J = 6,4 Hz, 1H, OH). MS (m/z) 180,2
(M + 1).
-
Schritt 2
-
1-Chlor-3-morpholin-4-yl-propan-2-ol
(2,0 g, 11 mmol) wurde mit der Lösung
aus NH3 in Methanol (25 Gew.-%, 20 ml) bei
Raumtemperatur behandelt. Stickstoff wurde in die Reaktionsmischung
bombiert, um den Ammoniak zu entfernen. Das Verdampfen des Lösungsmittels
ergab das Hydrogenchloridsalz 1-Amino-3-morpholin-4-yl-propan-2-ol
(2,0 g, 91%). 1H NMR (DMSO-d6) δ 2,30 (d,
J = 6,0 Hz, 2H), 2,36 (m, 4H, NCH2), 2,65 (dd,
J = 8,4, 12,8 Hz, 1H), 2,91 (dd, J = 3,6, 12,8 Hz, 1H), 3,52 (m,
4H, OCH2), 3,87 (m, 1H, CH), 5,32 (s, 1H, OH),
8,02 (brs., 3H, NH3 +).
MS (m/z) 161,1 (M + 1).
-
Schritt 3
-
5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (120
mg, 0,4 mmol) wurde mit 1-Amino-3-morpholin-4-yl-propan-2-ol (74
mg, 0,48 mmol) kondensiert, um 5-[5-Fluor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
(65 mg, 36%) zu präzipitieren.
Die Ursprungsflüssigkeit
wurde bis zur Trockne verdampft und der Rückstand wurde durch Schnellchromatographie
gereinigt, um zusätzliche
2 N (70 mg, 39%) zu erhalten. 1H NMR (DMSO-d6) δ 2,28
(m, 1H), 2,32 (m, 1H), 2,40 (m, 4H), 2,40, 2,42 (2 × s, 6H,
2 × CH3), 3,15 (s, 1H), 3,31 (m, 1H), 3,55 (m,
4H), 3,78 (m, 1H), 4,73 (brs, 1H, OH), 6,82 (dd, J = 4,5, 8,4 Hz,
1H), 6,90 (td, 2J = 2,8, 3J
= 10,0 Hz, 1H), 7,53 (m, 1H), 7,70 (s, 1H), 7,74 (dd, J = 2,0, 9,6
Hz, 1H) (aromatisch und Vinyl), 10,87 (s, 1H, CONH), 13,66 (s, 1H,
NH). LC-MS (m/z) 441,4 (M – 1).
-
Synthese
von 2-Hydroxy-7-oxa-4-azoniaspiro[3,5]nonanchlorid
-
In
einen 1 l 3-halsigen, rundbödigen
Kolben, dem ein Thermoelement, ein Stickstoffeinlass und ein zusätzlicher
250 ml Trichter eingesetzt wurde, wurde Morpholin (91,5 g, 91,5
ml, 1,05 mol, 1,0 Äq.)
und 100 ml Ethanol eingebracht. Die Lösung wurde schnell gerührt, während Epichlorhydrin
(100 g, 84,5 ml, 1,08 mol, 1,03 Äq.) über den
zusätzlichen
Trichter für über 30 Minuten
zugegeben wurde. Die Temperatur wurde überwacht und wenn die Gefäßtemperatur
27°C erreichte,
wurde die Reaktion in einem Eiswasserbad gekühlt. Die klare Lösung wurde
für 18
Stunden gerührt.
Die Reaktion wurde durch GC (verdünne 5 Tropfen der Reaktionsmischung
in 1 ml Ethanol und injiziere es auf eine 15 m DB-5 GC-Kapillarsäule mit
den folgenden Laufparametern, Injektor 250°C, Detektor 250°C, anfängliche
Ofentemperatur 28°C,
Erwärmen
auf 250°C
bei 10°C
pro Minute) untersucht. Der Reaktionsansatz wurde mit weniger als
3% verbleibendem Morpholin komplettiert. Der Reaktionsansatz wurde
durch Rotationsverdampfen bei 50°C
unter einem Vollvakuum konzentriert, bis kein Destillat mehr kondensiert
werden konnte. Das verbleibende Öl
wurde bei Raumtemperatur für
24–48
Stunden oder bis eine signifikante Masse an Kristallen beobachtet
wurde (Animpfen wird den Prozess beschleunigen) gelagert. Der Brei
wurde mit 250 ml Aceton verdünnt
und gefiltert. Die Feststoffe wurden im Vakuumofen bei 60°C für 18–24 Stunden
getrocknet. Dies ergab 84 g des kristallinen Produktes. Die ursprüngliche
wässrige Lösung könnte konzentriert
werden und der Kristallisationsprozess mit zunehmender Rückgewinnung
wiederholt werden. 1H NMR (400 MHz, DMSO-d6) δ 6,55
(d, 1H), 4,64 (m, 1H), 4,53 (m, 2H), 4,18 (m, 2H), 3,74 (m, 4H),
3,60 (m, 2H), 3,48 (m, 2H). 13C NMR (100
MHz, DMSO-d6) δ 70,9, 61,39, 61,04, 60,25,
58,54, 57,80.
-
Synthese
von 1-Amino-3-(4-morpholinyl)-2-propanol (racemisch)
-
In
einen 3 l 1-halsigen rundbödigen
Kolben mit einem Magnetrührstab
wurden 2-Hydroxy-7-oxa-4-azoniaspiro[3,5]nonanchlorid
(150 g, 835 mmol), gefolgt von 23 Gew.-% wasserfreiem Ammoniak in
Methanol (2120 ml) eingebracht. Der Kolben wurde zugestöpselt und
die sich ergebende klare Lösung
wurde bei 20–23°C für 18 Stunden
gerührt.
Eine GC unter den oben dargestellten Bedingungen zeigte kein verbleibendes
Ausgangsmaterial. Der Stopfen wurde entfernt und man ließ den Ammoniak
für 30
Minuten aus der Lösung ausgasen.
Der Kolben wurde dann in einen Rotationsverdampfer übertragen
und in einem 45°C
Bad und Vollvakuum zu einem weißen
Feststoff konzentriert. 1H NMR (400 MHz,
DMSO-d6) δ 3,57
(dd, 2H), 3,3–3,5
(m, 6H), 2,59 (m, 2H), 2,2–2,4
(m, 6H); 13C NMR (100 MHz DMSO-d6) δ 70,8,
67,1, 60,1, 53,8, 48,1.
-
Dem
oben in Beispiel 3 beschriebenen Verfahren folgend, jedoch 2-(RS)-1-Amino-3-morpholin-4-yl-propan-2-ol
durch 2-(S)-1-Amino-3-morpholin-4-yl-propan-2-ol
ersetzend, dass wie weiter unter beschrieben hergestellt wurde,
wurde die gewünschte
Verbindung 5-[5-Fluor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-(S)-hydroxy-3-morpholin-4-yl-propyl)-amid
erhalten.
-
Synthese
von 1-Amino-3-(4-morpholinyl)-2-propanol (nicht-razemisch)
-
In
einen 1 l 3-halsigen, rundbödigen
Kolben, der mit einem mechanischen Rührer, einem Thermoelement und
einem zusätzlichen
Trichter ausgerüstet
wurde, wurden Morpholin (91,5 g, 91,5 ml, 1,05 mol, 1,0 Äq.) und
45 ml t-Butanol eingebracht. Die Lösung wurde schnell gerührt, während R-Epichlorhydrin
(100 g, 84,5 ml, 1,08 mol, 1,03 Äq.) über den
zusätzlichen
Trichter über
etwa 30 Minuten zugegeben wurde. Die Temperatur wurde überwacht
und wenn die Gefäßtemperatur
27°C erreichte,
wurde die Reaktion in einem Eiswasserbad abgekühlt. Die klare Lösung wurde
für 18
Stunden gerührt.
Die Reaktion wurde mittels GC (verdünne 5 Tropfen der Reaktionsmischung
in 1 ml Ethanol und injiziere es auf eine 15 m DB-5 GC-Kapillarsäule mit
den folgenden Laufparametern, Injektor 250°C, Detektor 250°C, anfängliche
Ofentemperatur 28°C,
Aufwärmen
auf 250°C
bei 10°C
pro Minute) untersucht. Der Reaktionsansatz wurde mit weniger als
3% verbleibendem Morpholin komplettiert. Die Lösung wurde auf 10°C abgekühlt und
eine 20 Gew.-% Lösung
aus Kalium-t-butoxid in THF (576 g) wurde tropfenweise zugegeben,
wobei die Temperatur bei weniger als 15°C gehalten wurde. Der sich daraus
ergebende weiße
Brei wurde bei 10–15°C für 2 Stunden
gerührt
und durch GC unter Verwendung der oben angegebenen Bedingungen überprüft. Es konnte
kein Chlorhydrin beobachtet werden. Die Mischung wurde auf dem Rotationsverdampfer
mit einem 50°C
Bad und Vollvakuum auf konzentriert. Die sich daraus ergebende Mischung
wurde mit Wasser (500 ml) und Methylenchlorid verdünnt. Die
Phasen wurden aufgetrennt und die wässrigen Phasen mit Methylenchlorid
(500 ml) gewaschen. Die kombinierten organischen Schichten wurden über Natriumsulfat
getrocknet und zu einem klaren, farblosen Öl auf konzentriert. Dies ergab
145 g, bei 97% Ausbeute für
das Epoxid. 1H NMR (400 MHz, DMSO-d6) δ 3,3
(dd, 4H), 3,1 (m, 1H), 2,6 (dd, 1H), 2,5 (dd, 1H), 2,4 (m, 4H),
2,2 (dd, 2H); 13C NMR (100 MHz, DMSO-d6) δ 65,4,
60,1, 53,1, 48,9, 43,4.
-
Das
obige Rohepoxid wurde in einen 3 l 1-halsigen rundbödigen Kolben
mit einem magnetischen Rührstab
eingebracht. Wasserfreies Ammoniak in Methanol (24% w/w 2,5 l) wurden
zugegeben, der Kolben wurde zugestöpselt und die Mischung bei
Raumtemperatur für
24 Stunden gerührt.
Unter den obigen Bedingungen zeigte die GC kein zurückgebliebenes
Ausgangsmaterial. Der Stopfen wurde entfernt und man ließ den Ammoniak
für 30
Minuten aus der Lösung
ausdampfen. Der Kolben wurde dann auf einen Rotationsverdampfer übertragen
und in einem 45°C
Wasserbad und Vollvakuum zu einer klaren, farblosen Öl auf konzentriert.
Dies ergab 124 g des Produktes. 1H NMR (400
MHz, DMSO-d6) δ 3,57 (dd, 2H), 3,3–3,5 (m,
6H), 2,59 (m, 2H), 2,2–2,4
(m, 6H); 13C NMR (100 MHz, DMSO-d6) δ 70,8,
67,1, 60,1, 53,8, 48,1.
-
Synthese von 1-Amino-3-(4-morpholinyl)-2-(S)-propanol
-
In
einen 1 l 3-halsigen rundbödigen
Kolben, der mit einem mechanischen Rührer, einem Thermoelement und
einem zusätzlichen
Trichter ausgerüstet
wurde, wurden Morpholin (91,5 g, 91,5 ml, 1,05 mol, 1,0 Äq.) und
200 ml Methanol eingebracht. Die Lösung wurde schnell gerührt, während R-Epichlorhydrin
(100 g, 84,5 ml, 1,08 mol, 1,03 Äq.) über den
zusätzlichen
Trichter über
etwa 30 Minuten zugegeben wurde. Die Temperatur wurde überwacht
und wenn die Gefäßtemperatur
27°C erreichte,
wurde der Reaktionsansatz mit einem Eiswasserbad abgekühlt. Die
klare Lösung
wurde für
18 Stunden gerührt.
Der Reaktionsansatz wurde mittels GC (verdünne 5 Tropfen der Reaktionsmischung
in 1 ml Ethanol und injiziere es auf eine 15 m DB-5 GC-Kapillarsäule, mit
den folgenden Laufparametern, Injektor 250°C, Detektor 250°C, anfängliche
Ofentemperatur 28°C, Aufwärmen auf
250°C bei
10°C pro
Minute) untersucht. Der Reaktionsansatz wurde mit weniger als 3%
verbleibendem Morpholin komplettiert. Die Lösung wurde auf 10°C abgekühlt und
25 Gew.-% einer Lösung
aus Natriummethoxid in Methanol (233 g, 1,08 mol, 247 ml) wurden
tropfenweise zugegeben, wobei die Temperatur bei weniger als 15°C gehalten
wurde. Der sich daraus ergebende weiße Brei wurde bei 10–15°C für 2 Stunden
gerührt
und durch GC unter den oben angegebenen Bedingungen überprüft. Es konnte
kein Chlorhydrin beobachtet werden. Die Mischung wurde in einem
Rotationsverdampfer mit einem 50°C
Bad und Vollvakuum auf konzentriert. Die sich daraus ergebende Mischung
wurde mit Wasser (500 ml) und Methylenchlorid verdünnt. Die
Phasen wurden getrennt und die wässrige
Phase mit Methylenchlorid (500 ml) gewaschen. Die kombinierten organischen
Schichten wurden über
Natriumsulfat getrocknet und zu einem klaren, farblosen Öl auf konzentriert.
Dies ergab 145 g, bei 97% Ausbeute an 1,2-Epoxy-3-morpholin-4-ylpropan. 1H NMR (400 MHz, DMSO-d6) δ 3,3 (dd,
4H), 3,1 (m, 1H), 2,6 (dd, 1H), 2,5 (dd, 1H), 2,4 (m, 4H), 2,2 (dd,
2H); 13C NMR (100 MHz, DMSO-d6) δ 65,4, 60,1,
53,1, 48,9, 43,4.
-
Das
obige Rohprodukt 1,2-Epoxy-3-morpholin-4-ylpropan wurde in einen
3 l 1-halsigen rundbödigen Kolben
mit einem magnetischen Rührstab
eingebracht. Wasserfreier Ammoniak in Methanol (24% w/w 2,5 l) wurden
zugegeben, der Kolben wurde zugestöpselt und die Mischung bei
Raumtemperatur für
24 Stunden gerührt.
Eine GC unter den obigen Bedingungen zeigte kein zurückgebliebenes
Ausgangsmaterial. Der Stopfen wurde entfernt und man lies den Ammoniak
für 30
Minuten aus der Lösung
ausdampfen. Der Kolben wurde dann auf einen Rotationsverdampfer übertragen
und zu einem klaren, farblosen Öl
in einem 45°C
Wasserbad und Vollvakuum auf konzentriert. Dies ergab 124 g an 1-Amino-3-(4-morpholinyl)-2-(S)-propanol. 1H NMR (400 MHz, DMSO-d6) δ 3,57 (dd,
2H), 3,3–3,5
(m, 6H), 2,59 (m, 2H), 2,2–2,4
(m, 6H); 13C NMR (100 MHz, DMSO-d6) δ 70,8,
67,1, 60,1, 53,8, 48,1.
-
-
Imidazolamid
(7,0 g, 32,3 mmol), Amin (15,0 g, 64,6 mmol), 5-Fluoroxindol (4,93
g, 32,6 mmol), Triethylamin (9,79 g, 96,9 mmol) und THF (88 ml)
wurden vermischt und auf 60°C
erhitzt. Es bildete sich eine braune Lösung. Nach dem Rühren für 24 h bei
60°C wurde
der gelbe Brei auf RT (Raumtemperatur) abgekühlt und gefiltert. Der Filterrückstand
wurde mit 80 ml THF gewaschen und Übernacht bei 50°C unter Vollvakuum
getrocknet. Ein brauner Feststoff (23,2 g) wurde erhalten. Der Feststoff
wurde in 350 ml Wasser für
5 h bei RT aufgeschlemmt und gefiltert. Der Filterrückstand
wurde mit 100 ml Wasser gewaschen und bei 50°C unter Vollvakuum Übernacht
getrocknet. 8,31 g wurden mit einer chemischen Ausbeute von 56%
erhalten.
-
-
In
einen 0,25 l Kolben, der mit einem Thermometer, einem Kondensator,
einem magnetischen Rührer und
einem Stickstoffeinlass ausgerüstet
wurde, wurden 4,92 g 5-Fluoroxindol, 7,0 g Imidazolamid, 15,5 g (R)-1-Amino-3-(4-morpholinyl)-2-propanol,
9,78 g Triethylamin und 88 ml Tetrahydrofuran eingebracht. Die Mischung
wurde für
16,5 Stunden auf 60°C
erhitzt. Der Reaktionsansatz wurde auf Umgebungstemperatur abgekühlt und
gefiltert. Die erhaltenen Feststoffe werden (3) drei aufeinander
folgende Male in Acetonitril bei 11 ml/g aufgeschlemmt, in Vakuum
für 3,6
g (25,25%) getrocknet. [HPLC, Hypersil BDS, C-18, 5μ, (6:4),
Acetonitril: 0,1 M Ammoniumchlorid, PHA-571437 = 4,05 min] H1 NMR (DMSO): δ 10,86 (1H, bs); 7,75 (1H, d);
7,70 (1H, s); 7,50 (1H, m); 6,88 (2H, m); 4,72 (1H, bs); 3,78 (1H,
bs); 3,56 (4H, m); 3,32 (6H, m); 3,15 (1H, m); 2,43 (8H, bm).
-
Beispiel 4
-
Synthese von 2,4-Dimethyl-5-[2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
-
5-(2-Oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (113
mg, 0,4 mmol) wurde mit 1-Amino-3-morpholin-4-yl-propan-2-ol
(74 mg, 0,48 mmol) kondensiert, um 2,4-Dimethyl-5-[2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
(77 mg, 45,3%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,27 (m,
1H), 2,32 (m, 1H), 2,40 (m, 4H), 2,40, 2,42 (2 × s, 6H, 2 × CH3),
3,15 (s, 1H), 3,32 (m, 1H), 3,55 (m, 4H), 3,77 (m, 1H), 4,74 (d,
J = 4,8 Hz, 1H, OH), 6,86 (d, J = 7,6 Hz, 1H), 6,96 (t, J = 7,2
Hz, 1H), 7,10 (t, J = 7,6 Hz, 1H), 7,49 (t, J = 5,6 Hz, 1H), 7,61
(s, 1H), 7,77 (d, J = 8,0 Hz, 1H) (aromatisch und Vinyl), 10,88
(s, 1H, CONH), 13,62 (s, 1H, NH). LC-MS (m/z) 425,4 (M + 1).
-
Beispiel 5
-
Synthese von 5-[5-Chlor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
-
5-(5-Chlor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (126,6
mg, 0,4 mmol) wurde mit 1-Amino-3-morpholin-4-yl-propan-2-ol (74
mg, 0,48 mmol) kondensiert, um 5-[5-Chlor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
(107 mg, 58%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,29 (m,
1H), 2,33 (m, 1H), 2,39 (m, 4H), 2,40, 2,42 (2 × s, 6H, 2 × CH3),
3,15 (s, 1H), 3,37 (m, 1H), 3,55 (m, 4H), 3,77 (m, 1H), 4,74 (d,
J = 4,8 Hz, 1H, OH), 6,85 (d, J = 8,4 Hz, 1H), 7,11 (dd, J = 2,0,
8,0 Hz, 1H), 7,53 (t, J = 5,6 Hz, 1H), 7,75 (s, 1H), 7,97 (d, J
= 2,0 Hz, 1H) (aromatisch und Vinyl), 10,99 (s, 1H, CONH), 13,62
(s, 1H, NH). LC-MS (m/z) 457,4 (M – 1).
-
Die
R- und S-Stereoisomere können
wie folgt hergestellt werden.
-
-
Imidazolamid
(7,0 g, 32,3 mmol), Amin (15,5 g, 96,9 mmol), 5-Chloroxindol (5,48
g, 32,6 mmol), Triethylamin (14 ml) und THF (88 ml) wurden vermischt
und auf 60°C
erhitzt. Es bildete sich eine rote Lösung. Nach dem Rühren für 16 h bei
60°C wurde
der gelbe Brei auf RT abgekühlt
und gefiltert. Der Filterrückstand
wurde mit 2 × 50
ml THF gewaschen und Übernacht
bei 50°C
unter Vakuum getrocknet. 4,36 g wurden mit einer chemischen Ausbeute
von 29% erhalten.
-
-
Imidazolamid
(6,8 g, 31,3 mmol), Amin (10,0 g, 62,5 mmol), 5-Chloroxindol (5,3
g, 31,6 mmol) und THF (100 ml) wurden vermischt und auf 60°C erhitzt.
Es bildete sich eine rote Lösung.
Nach dem Rühren
für 68
h bei 60°C
wurde Triethylamin (14 ml) zugegeben und für 5 h bei 60°C gerührt. Die
Reaktion war nicht vollständig.
Man gebe 4,6 g der Amin-Seitenkette
zu und rühre
für 20
h bei 60°C.
Der gelbe Brei wurde auf RT abgekühlt und gefiltert. Der Filterrückstand
wurde mit 2 × 50
ml THF gewaschen und Übernacht
bei 50°C
unter Vollvakuum getrocknet. 5,48 g wurden mit einer chemischen
Ausbeute von 38% erhalten.
-
Beispiel 6
-
Synthese von 5-[5-Brom-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
-
5-(5-Brom-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (72,2
mg, 0,2 mmol) wurde mit 1-Amino-3-morpholin-4-yl-propan-2-ol (38
mg, 0,24 mmol) kondensiert, um 5-[5-Brom-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-amid
(55 mg, 55%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,27 (m,
1H), 2,32 (m, 1H), 2,39 (m, 4H), 2,41, 2,42 (2 × s, 6H, 2 × CH3),
3,13 (s, 1H), 3,35 (m, 1H), 3,55 (m, 4H), 3,77 (m, 1H), 4,74 (d,
J = 4,4 Hz, 1H, OH), 6,80 (d, J = 8,4 Hz, 1H), 7,24 (dd, J = 2,0,
8,0 Hz, 1H), 7,51 (t, J = 5,6 Hz, 1H), 7,76 (s, 1H), 8,09 (d, J
= 2,0 Hz, 1H) (aromatisch und Vinyl), 10,99 (s, 1H, CONH), 13,62
(s, 1H, NH). LC-MS (m/z) 503,4 (M – 1).
-
Beispiel 7
-
Synthese von 2,4-Dimethyl-5-[2-oxo-1,2-dihydro-indol-(3Z)-yliden-methyl]-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
-
Schritt 1
-
Eine
Mischung aus 3-[1,2,3]triazol (2,0 g, 29 mmol), Epichlorhydrin (3,4
ml, 43,5 mmol) und N,N-Diisopropylethylamin
(2,6 ml, 15 mmol) in Ethanol (50 ml) wurde bei Raumtemperatur Übernacht
gerührt.
Nach dem Entfernen der Lösungsmittel
wurde der Rest durch Schnellchromatographie (CH2Cl2/CH3OH = 100/1–100/2–100/4)
gereinigt, um 1-Chlor-3-(1,2,3)-triazol-2-ylpropan-2-ol (2,1 g,
45%) zu erhalten. 1H NMR (CDCl3) δ 3,52 (m,
2H, OH und CH2), 3,60 (dd, J = 5,2, 11,2
Hz, 1H), 4,36 (m, 1H, CH), 4,68 (m, 2H), 7,67 (s, 2H). MS (m/z)
162,1 (M + 1) und 1-Chlor-3-(1,2,3)triazol-1-ylpropan-2-ol
(2,3 g, 49%). 1H NMR (CDCl3) δ 3,56 (s,
1H), 3,57 (s, 1H), 4,35 (m, 1H), 4,53 (dd, J = 7,2, 14 Hz, 1H),
4,67 (dd, J = 3,8, 14 Hz, 1H), 7,67 (s, 1H), 7,71 (s, 1H). MS (m/z)
162,1 (M + 1).
-
Schritt 2
-
1-Chlor-3(1,2,3)triazol-1-ylpropan-2-ol
(2,3 g, 13 mmol) wurde mit der Lösung
aus NH3 in Methanol (25 Gew.-%, 20 ml) bei
60°C Übernacht
in einem versiegelten Druckbehälter
behandelt. Nach dem Abkühlen
auf Raumtemperatur wurde Stickstoff in die Reaktionsmischung bombiert,
um den Ammoniak zu entfernen. Das Verdampfen des Lösungsmittels
ergab das Hydrogenchloridsalz von 1-Amino-3-(1,2,3)triazol-1-ylpropan-2-ol (2,57 g, 100%). 1H NMR (DMSO-d6) δ 2,68 (dd,
J = 8,8, 12,8 Hz, 1H), 2,97 (dd, J = 3,6, 12,8 Hz, 1H), 4,15 (m, 1H),
4,44 (dd, J = 6,4, 14 Hz, 1H), 4,57 (dd, J = 4,6, 14 Hz, 1H), 5,95
(d, J = 5,2 Hz, 1H, OH), 7,77 (s, 1H), 8,01 (brs., 3H, NH3 +), 8,12 (s, 1H).
MS (m/z) 143,1 (M + 1).
-
Schritt 3
-
5-(2-Oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (113
mg, 0,4 mmol) wurde mit 1-Amino-3(1,2,3)triazol-1-yl-propan-2-ol
(85 mg, 0,48 mmol) kondensiert, um 2,4-dimethyl-5-[2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-1H-pyrrol-3-carbonsäure(2-hydroxy-3- [1,2,3]triazol-1-yl-propyl)-amid
(70 mg, 41%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,45, 2,48
(2 × s,
6H, 2 × CH3), 3,35 (m, 2H), 4,02 (m, 1H), 4,32 (dd,
J = 7,6, 14 Hz, 1H), 4,53 (dd, J = 3,4, 14 Hz, 1H), 5,43 (d, J =
5,6 Hz, 1H, OH), 6,91 (d, J = 7,6 Hz, 1H), 7,01 (t, J = 7,6 Hz,
1H), 7,15 (t, J = 8,0 Hz, 1H), 7,66 (s, 1H), 7,12 (t, J = 5,6 Hz,
1H), 7,74 (s, 1H), 7,77 (d, J = 7,6 Hz, 1H), 8,11 (s, 1H), 10,93
(s, 1H, CONH), 13,68 (s, 1H, NH). LC-MS (m/z) 405,4 (M – 1).
-
Beispiel 8
-
Synthese von 5-[5-Fluor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
-
5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (120
mg, 0,4 mmol) wurden mit 1-Amino-3(1,2,3)triazol-1-yl-propan-2-ol
(85 mg, 0,48 mmol) kondensiert, um 5-[5-Fluor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
(100 mg, 62%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,42, 2,44
(2 × s,
6H, 2 × CH3), 3,27 (m, 2H), 3,98 (m, 1H), 4,27 (dd,
J = 7,6, 14 Hz, 1H), 4,50 (dd, J = 3,4, 13,6 Hz, 1H), 5,38 (d, J
= 5,6 Hz, 1H, OH), 6,82 (dd, J = 4,4, 8,4 Hz, 1H), 6,91 (td, 2J = 2,4, 3J = 9,0
Hz, 1H), 7,70 (m, 3H), 7,75 (dd, J = 2,4, 9,2 Hz, 1H), 8,11 (s.
1H), 10,93 (s, 1H, CONH), 13,73 (s, 1H, NH). LC-MS (m/z) 423,4 (M – 1).
-
Beispiel 9
-
Synthese von 5-[5-Chlor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
-
5-(5-Chlor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (126,6
mg, 0,4 mmol) wurde mit 1-Amino-3(1,2,3)triazol-1-yl-propan-2-ol
(85 mg, 0,48 mmol) kondensiert, um 5-[5-Chlor-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
(48 mg, 27%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,42, 2,44
(2 × s,
6H, 2 × CH3), 3,27 (m, 2H), 3,99 (m, 1H), 4,28 (dd,
J = 7,8, 14 Hz, 1H), 4,51 (dd, J = 3,2, 14 Hz, 1H), 5,39 (d, J =
6,0 Hz, 1H, OH), 6,85 (d, J = 8,4 Hz, 1H), 7,12 (dd, J = 2,0, 8,2
Hz, 1H), 7,70 (m, 2H), 7,74 (s, 1H), 7,97 (d, J = 2,0 Hz, 1H), 8,07
(s, 1H), 10,99 (s, 1H, CONH), 13,65 (s, 1H, NH). LC-MS (m/z) 439,4
(M – 1).
-
Beispiel 10
-
Synthese von 5-[5-Brom-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
-
5-(5-Brom-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure (144,4
mg, 0,4 mmol) wurden mit 1-Amino-3(1,2,3)triazol-1-yl-propan-2-ol
(85 mg, 0,48 mmol) kondensiert, um 5-[5-Brom-2-oxo-1,2-dihydro-indol-(3Z)-ylidenmethyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-[1,2,3]triazol-1-yl-propyl)-amid
(130 mg, 67%) zu präzipitieren. 1H NMR (DMSO-d6) δ 2,41, 2,44
(2 × s,
6H, 2 × CH3), 3,27 (m, 2H), 3,99 (m, 1H), 4,28 (dd,
J = 7,6, 14 Hz, 1H), 4,50 (dd, J = 3,6, 14 Hz, 1H), 5,40 (d, J =
5,6 Hz, 1H, OH), 6,81 (d, J = 8,4 Hz, 1H), 7,24 (dd, J = 2,0, 8,0
Hz, 1H), 7,70 (m, 2H), 7,77 (s, 1H), 8,07 (s, 1H), 8,10 (d, J =
1,6 Hz, 1H), 11,0 (s, 1H, CONH), 13,64 (s, 1H, NH). LC-MS (m/z)
485,4 (M – 1).
-
Die
Synthese von 5-(5-Brom-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure, 5-(5-Chlor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure, 5-(2-Oxo-1,2-dihydroindol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure wurde
in der vom Anmelder gleichzeitig mit der vorliegenden Anmeldung
am 14. Februar 2001 unter dem Titel "PYRROLE SUBSTITUTED 2-INDOLINONE – PROTEIN
KINASE INHIBITORS",
Seriennr. 09/783,264, angemeldeten Anmeldung, beschrieben, wobei
deren Offenbarung hierin in ihrer Gesamtheit aufgenommen wird.
-
Beispiel
11 Synthese
von 1-Amino-3-(1,1-dioxo-λ
6-thiomorpholin-4-yl)-propan-2-ol
-
Zur
Lösung
aus Thiomorpholin (5,0 g, 48,7 mmol) in HOCH3 (200
ml) wurde die Lösung
aus Oxon (36,0 g, 58,5 mmol) in H2O (100
ml) gegeben. Die Mischung wurde bei 40°C für 48 h gut gerührt und
dann bei 0°C
gekühlt.
Wässriges
NaOH wurde tropfenweise zugegeben, um auf pH = 12 einzustellen.
Der Feststoff wurde herausgefiltert und mit HOCH3 (3 × 40 ml)
gewaschen. Die kombinierte Flüssigkeit
wurde kondensiert und durch Schnellchromatographie auf Silicagel
(CHCl3/CH3OH/NH3·H2O = 3/1/0,1–2/1/0,1) gereinigt, um Thiomorpholin-1,1-dioxid
(6,2 g) mit einer Ausbeute von 93% zu erhalten. 1H
NMR (DMSO-d6) δ 2,97 (m, 4H), 3,07 (m, 4H),
3,42 (brs, 1H), MS (m/z) 136 (M + 1).
-
Zur
Mischung aus Thiomorpholin-1,1-dioxid (2,5 g, 18,5 mmol) und (R)-(–)Epichlorhydrin
(1,55 ml, 20 mmol) wurde das Lösungsmittel
Ethanol (50 ml) und H2O (5 ml) zugegeben
und dann bei 25°C
für 24
h gerührt. Nach
dem Entfernen des Lösungsmittels
wurde der Rest durch Schnellchromatographie gereinigt, um (R)-1-Chlor-3-(1,1-dioxo-λ6–-thiomorpholin-4-yl)-propan-2-ol (4,0
g, 96%) zu erhalten. 1H NMR (DMSO-d6) δ 2,50
(m, 2H), 2,94 (m, 4H), 305 (m; 4H), 3,54 (dd, J = 5,8, 11,2, Hz,
1H), 3,63 (dd, J = 4,4, 11,2 Hz, 1H), 3,78 (m, 'H, CH), 5,10 (d, J = 5,2 Hz, 1H, OH),
MS (m/z) 228,2 (M + 1).
-
(R)-1-Chlor-3-(1,1-dioxo-λ
6-thiomorpholin-4-yl)-propan-2-ol (2,27 g, 10
mmol) wurde mit der Lösung aus
NH
3 in Methanol (25 Gew.-%, 20 ml) bei 50°C für 12 h behandelt.
Nach dem Verdampfen der Lösungsmittel wurde
der Rest mit einem anionischen Austauschharz (AG1x8, OH-Form) in
Wasser behandelt, um das Rohprodukt (S)-1-Amino-3-(1,1-dioxo-λ
6-thiomorpholin-4-yl)-propan-2-ol
(2,0 g) zu erhalten. Es war zu etwa 30% mit seinem Dimer kontaminiert
und konnte durch Säulenchromatographie
kaum gereinigt werden. MS (m/z) 209,2 (M + 1). Die Kondensation
von (S)-1-Amino-3-(1,1-dioxo-λ
6-thiomorpholin-4-yl)-propan-2-ol
mit Oxindolen ergab die gewünschten
Indolinone (Ausbeute 50–80%
nach der Reinigung). (R)-5-(2-Oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure[3-(1,1-dioxo-λ
6-thiomorpholin-4-yl)-2-hydroxy-propyl]-amid
- 1H NMR (DMSO-d6) δ 2,39,
2,42 (2 × s,
6H, 2 × CH3), 2,49 (m, 1H), 2,56 (m, 1H), 2,97 (m,
4H), 3,07 (m, 4H), 3,16 (m, 1H), 3,34 (m, 1H), 3,74 (m, 1H), 4,83
(d, J = 4,8 Hz, IH, OH), 6,86 (d, J = 7,6 Hz, 1H), 6,97 (t, J =
7,4 Hz, 1H), 7,11 (t, J = 7,5 Hz, 1H), 7,50 (t, J = 5,6 Hz, 1H),
7,61 (s, 1H), 7,76 (d, J = 7,6 Hz, 1H) (aromatisch und Vinyl), 10,88
(s, 1H, CONH), 13,62 (s, 1H, NH), LC-MS (m/z) 473,4 (M + 1).
(R)-5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure[3-(1,1-dioxo-λ6-thiomorpholin-4-yl)-2-hydroxy-propyl]-amid - 1H NMR (DMSO-d6) δ 2,40,
2,42 (2 × s,
6H, 2 × CH3), 2,47 (m, 1H), 2,54 (m, 1H), 2,97 (m,
4H), 3,06 (m, 4H), 3,17 (m, 1H), 3,30 (m, 1H), 3,74 (m, 1H), 4,83
(d, J = 4,4 Hz, 1H), 6,82 (t, J = 4,0 Hz, 1H), 6,91 (td, 2J = 2,8, 3J = 9,0
Hz, 1H), 7,53 (t, J = 5,8 Hz, 1H), 7,70 (s, 1H), 7,75 (dd, J = 2,4,
9,2 Hz, 1H), 10,88 (s, 1H), 13,67 (s, 1H). LC-MS (m/z) 491,4 (M
+ 1).
(R)-5-(5-Chlor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure[3-(1,1-dioxo-λ6-thiomorpholin-4-yl)-2-hydroxy-propyl]-amid - 1H NMR (DMSO-d6) δ 2,40,
2,42 (2 × s,
6H, 2 × CH3), 2,45 (m, 1H), 2,53 (m, 1H), 2,96 (m,
4H), 3,06 (m, 4H), 3,17 (m, 1H), 3,33 (m, 1H), 3,75 (m, 1H), 4,83
(d, J = 4,4 Hz, 1H, OH), 6,85 (t, J = 8,4 Hz, 1H), 7,11 (dd, J = 2,2,
8,2 Hz, 1H), 7,53 (t, J = 5,5 Hz, 1H), 7,75 (s, 1H), 7,97 (d, J
= 2,0 Hz, 1H), 10,98 (s, 1H), 13,62 (s, 1H), LC-MS (m/z) 507,2 (M
+ 1). (R)-5-(5-Brom-2-oxo-1,2-dihydro-indol-3-ylidenmethyl),
2,4-dimethyl-1H-pyrrol-3-carbonsäure[3-(1,1-dioxo-λ6-thiomorpholin-4-yl)-2-hydroxy-propyl]-amid
- 1H NMR (DMSO-d6) δ 2,41,
2,42 (2 × s,
6H, 2 × CH3), 2,47 (m, 1H), 2,54 (m, 1H), 2,97 (m,
4H), 3,06 (m, 4H), 3,18 (m, 1H), 3,30 (m, 1H), 3,74 (m, 1H), 4,83
(d, J = 4,8 Hz, 1H), 6,81 (d, J = 8,4 Hz, 1H), 7,24 (dd, J = 1,8, 8,2
Hz, 1H), 7,53 (t, J = 5,8, 1H), 7,76 (s, 1H), 8,09 (d, J = 2,0 Hz,
1H), 10,98 (s, 1H) 13,62 (s, 1H), LC-MS (m/z) 553,6 (M + 1).
-
Beispiel
12 Synthese
von (S)- oder (R)-1-methylamino-3-morpholin-4-yl-propan-2-ol
-
Die
Mischung aus Morpholin (1,74 ml, 20 mmol) und (R)-Epichlorhydrin (1,56
ml, 20 mmol) in Ethanol (10 ml) wurde bei R. T. für 48 h gerührt. Nach
dem Entfernen des Lösungsmittels
wurde der Reststoff mit der Lösung
aus CH3NH2 in Wasser
(40 Gew.-%, 20 ml) bei R. T. für
14 h behandelt. Das Entfernen der Lösungsmittel ergab das Rohprodukt
(S)-1-Methylamino-3-morpholin-4-yl-propan-2-ol,
das durch Vakuumdestillation oder Säulenchromatographie gereinigt
werden konnte (2,4 g, 70%). (R)-1-Methylamino-3-morpholin-4-yl-propan-2-ol wurde
aus (S)-Epichlorhydrin mit einer Ausbeute von 76% hergestellt. 1H NMR (CDCl3) δ 2,33 (dd,
J = 3,6, 12,4 Hz, 1H), 2,42 (m, 1H), 2,44 (dd, J = 2,8, 9,8 Hz,
2H), 2,45 (s, 3H), 2,53 (dd, J = 7,6, 11,8 Hz, 1H), 2,62 (m, 2H),
2,65 (dd, J = 3,6, 12,0 Hz, 1H), 3,71 (m, 4H), 3,85 (m, 1H), 13CNMR (CDCl3) δ 67,06, 65,58,
62,80, 55,87, 53,94, 36,72, MS (m/z) 175 (M + 1).
-
(S)-1-Methylamino-3-morpholin-4-yl-propan-2-ol
wurde mit 5-Fluoroxindol, dass mit (R)-5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-methyl-amid versehen
ist, kondensiert.
1H
NMR (DMSO-d
6) δ 2,0 (s, 3H), 2,15 (m, 1H),
2,25 (m, 6H), 2,28 (m, 2H), 2,42 (s, 1H), 2,95 (s, 1H), 3,0 (s, 3H),
3,25 (m, 2H), 3,57 (m, 2H), 3,97 & 3,68
(2 × brs,
1H), 4,80 & 4,74
(2 × brs,
1H), 6,82 (dd, J = 4,0, 8,0 Hz, 1H), 6,90 (td,
2J
= 2,3,
3J = 8,7 Hz, 1H), 7,67 (s, 1H), 7,71
(dd, J = 2,2, 9,0 Hz, 1H), 10,86 (s, 1H), 13,57 (s, 1H), LC-MS (m/z)
457,2 (M + 1).
-
(R)-1-Amino-3-morpholin-4-yl-propan-2-ol
versehen mit (S)-5-(5-Fluor-2-oxo-1,2-dihydro-indol-3-ylidenmethyl)-2,4-dimethyl-1H-pyrrol-3-carbonsäure(2-hydroxy-3-morpholin-4-yl-propyl)-methyl-amid
-
- 1H NMR (DMSO-d6) δ 2,0 (m,
3H), 2,10 (m, 1H), 2,22 (m, 6H), 2,25 (m, 2H), 2,38 (m, 1H), 2,90
(s, 1H), 2,96 (s, 3H), 3,27 (m, 2H), 3,52 (m, 2H), 3,93 & 3,64 (2 × brs, 1H),
4,75 & 4,70 (2 × brs, 1H),
6,77 (dd, J = 4,6, 8,2 Hz, 1H), 6,85 (td, 2J
= 2,5, 3J = 8,8 Hz, 1H), 7,62 (s, 1H), 767
(dd, J = 2,0, 9,6 Hz, 1H), 10,81 (s, 1H), 13,52 (s, 1H), LC-MS (m/z)
457,2 (M + 1).
-
Beispiel 13
-
Amin-Seitenkettenherstellung
-
3-(1-H-Tetrazol-1-yl)]-2-hydroxy-1-chlorpropan
und 3-(2-H-Tetrazol-2-yl)-2-hydroxy-1-chlorpropan
-
6,905
g Tetrazol (100 mmol), und 1,75 ml Diisopropylethylamin (10 mmol)
und 11,73 Epichlorhydrin (150 mmol) in wasserfreiem Acetonitril
(30 ml) wurden bei 60°C
für 4 Stunden
gerührt.
Die erhaltene Lösung wurde
verdampft, unter einem Hochvakuum getrocknet und auf einer Säule aus
Silica in Chloroform-Methanol 100:8 gereinigt. Die erste Fraktion
stellte reines 3-(2-H-Tetrazol-2-yl)-2-hydroxy-1-chlorpropan, 6,215 g (farbloses Öl, 38% A.
(A., Ausbeute: engl. Y, yield)) bereit, die zweite Fraktion ergab
9,208 g reines 3-(1-H-Tetrazol-1-yl)]-2-hydroxyl-1-chlorpropan (klebriges
Gummi; 57% A.).
-
3-(1-H-Tetrazol-1-yl)]-2-hydroxy-1-aminopropan
-
9,110
g an 3-(1-H-Tetrazol-1-yl)]-2-hydroxy-1-chlorpropan, 15 g Kaliumcarbonat und
130 ml an gesättigtem
methanolischem Ammoniak wurden für
21 Stunden gerührt,
dann gefiltert und verdampft. Der auf einer Säule aus Silica in Chloroform-Methanol-wässrigem
Ammoniak 80:35:4 gereinigte Reststoff ergab A. = 7,326 g eines weißen klebrigen
Gummis (91,5% th).
-
3-(2-H-Tetrazol-2-yl)]-2-hydroxy-1-aminopropan
-
6,105
g an 3-(2-H-Tetrazol-2-yl)]-2-hydroxy-1-chlorpropan, 10 g Kaliumcarbonat und
95 ml an gesättigtem
methanolischen Ammoniak wurden für
21 Stunden gerührt,
dann gefiltert und verdampft. Der auf einer Säule aus Silica in Chloroform-Methanol-wässrigem
Ammoniak 60:25:2 gereinigte Reststoff ergab A. = 3,726 g eines weißen kristallinen
Feststoffes (69,5% th).
-
3-[(2R,6S)-2,6-Dimethylmorpholin-4-yl]-2-hydroxy-1-aminopropan
-
4,7
ml Epichlorhydrin (60 mmol) wurden zu einer eisgekühlten Lösung aus
cis-2,6-Dimethylmorpholin (4,607 g, 40 mmol) in Trifluorethanol
(5 ml) gegeben. Die Lösung
wurde bei 0–5°C für 1 h gerührt, dann
wurde das Bad zum Abkühlen
entfernt und es wurde für
zusätzliche
5 h bei RT gerührt.
Die Mischung wurde unter Hochvakuum verdampft, der erhaltene ölige Reststoff
wurde in wasserfreiem Ethanol (50 ml) aufgelöst, die Lösung wurde in einem Eisbad
gekühlt,
festes Natriummethoxid (2,27 g) wurde in zwei Portionen zugegeben
und die Mischung wurde bei 0–5°C für 2 h gerührt. Die
Reaktionsmischung wurde dann gefiltert, die Salze mit Ethanol (30
ml) gewaschen und die kombinierten Filtrate zu eisgekühltem konzentrierten
flüssigen
Ammoniak (200 ml) gegeben. Die Mischung wurde bei RT für 12 h gerührt und
dann unter einem Hochvakuum verdampft. Der Rest wurde auf einer
Säule aus
Silica in einer Mischung aus Chloroform-Methanol-7 M methanolischem
Ammoniak 80:15:3 gereinigt. A. = 5,75 g eines weißen, kristallinen,
hygroskopischen Feststoffes (76,3% th).
-
(2S)-3-(3-Methyl-2,5-dioxoimidazolidin-1-yl)-2-hydroxy-1-chlorpropan und (2S)-3-(3-Methyl-2,5-dioxoimidazolidin-1-yl)-2-hydroxy-1-aminopropan
-
3,423
g an 3-Methyl-2,5-dioxoimidazolidin (3,423 g), und 3,60 ml R-Epichlorphydrin
(–) (99%
ee) und 0,30 ml der Barton-Base (1,5 mmol) in wasserfreiem Acetonitril
wurden bei 60°C
für 20
h gerührt.
Die erhaltene Lösung
wurde unter einem Hochvakuum verdampft und auf einer Säule aus
Silica in einer Mischung aus Chloroform-Methanol (einem Gradienten
von 5 bis 20% Methanol) gereinigt, um 5,572 g der Chlorverbindung
als weißen,
amorphen Feststoff (90% A.) zu erhalten. Das Chlorid wurde wie folgt
in ein Amin umgewandelt. Das erhaltene Hydroxy-Chlor-Zwischenprodukt
wurde in methanolischem Ammoniak (gesättigt mit Ammoniakgas) gelöst, Kaliumcarbonat
wurde zugegeben und die Mischung wurde in einem geschlossenen Kolben
für 2 ½ Tage
gerührt.
Die Reaktionsmischung wurde gefiltert und die Filtrate verdampft.
Der Reststoff wurde auf einer Silicasäule in einer Mischung aus Chloroform-Methanolkonzentriertem,
wässrigen
Ammoniak 80:15:1,5 gereinigt.
-
Beispiel 14
-
5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(2H-tetraazol-2-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 22) (allgemeines Verfahren)
-
72
mg an 3-(2-H-Tetrazol-2-yl)]-2-hydroxy-1-aminopropan wurden zum
Brei aus 105 mg (0,25 mmol) 5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure-1-oxy-7-azabenztriazolester
[hergestellt durch Aktivieren von (3Z)-3-({3,3-Dimethyl-4-carboxy-1-H-pyrrol-2-yl}methylen)-5-fluor-1,3-dihydro-2H-indol-2-on
(480 mg; 1,6 mmol) mit dem HATU-Reagenz (570 mg; 1,5 mmol) in Gegenwart
der Hunig-Base (3,0 mol; 0,525 ml) in DMF (5 ml), und isolieren
durch Präzipitation
mit Chloroform (5 ml) und trocknen unter einem Hochvakuum mit einer
Ausbeute von 92% (579 mg) in reiner Form] in wasserfreiem Dimethylacetamid
(1,5 ml) gegeben. Die Mischung wurde für 30 Minuten gerührt und
im Hochvakuum verdampft. Der Reststoff wurde in einer Mischung aus
Methanol-Diethylamin 20:1 (3 ml) suspendiert, man ließ es im
Kühlschrank
(5°C) für 1 h kristallisieren,
es wurde gefiltert und das Präzipitat
wurde mit eiskaltem Methanol gewaschen und im Hochvakuum getrocknet.
A. = 106 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 15
-
5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(2H-tetraazol-2-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 23) (allgemeines Verfahren)
-
72
mg an 3-(2-H-tetrazol-2-yl)]-2-hydroxy-1-aminopropan wurden zum
Brei aus 109 mg (0,25 mmol) 5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure-1-oxy-7-azabenztriazolester
[hergestellt durch Aktivieren von (3Z)-3-([3,3-dimethyl-4-carboxy-1-H-pyrrol-2-yl)methylen)-5-chlor-1,3-dihydro-2H-indol-2-on
(1,520 g; 4,8 mmol) mit dem HATU-Reagenz (1,768 g; 4,65 mmol) in
Gegenwart der Hunig-Base (9,0 mmol; 1,58 ml) in DMF (20 ml), und
isolieren durch Präzipitation mit
Chloroform (20 ml) und trocknen unter einem Hochvakuum mit einer
Ausbeute von 94% (1,907 g) in reiner Form] in wasserfreiem Dimethylacetamid
(1,5 ml) gegeben. Die Mischung wurde für 30 Minuten gerührt und im
Hochvakuum verdampft. Der Reststoff wurde in einer Mischung aus
Methanol-Diethylamin 20:1 (3 ml) suspendiert, man ließ es im
Kühlschrank
(5°C) für 1 h kristallisieren,
es wurde gefiltert und das Präzipitat
wurde in eiskaltem Methanol gewaschen und im Hochvakuum getrocknet.
A. = 109 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 16
-
N-[2-hydroxy-3-(2H-tetraazol-2-yl)propyl]-2,4-dimethyl-5-[(Z)-[2-oxo-5-(trifluormethoxy)-1,2-dihydro-3H-indol-3-yliden]methyl)-1H-pyrrol-3-carboxamid
(Verbindung 24) (allgemeines Verfahren)
-
72
mg an 3-(2-H-Tetraazol-2-yl)]-2-hydroxy-1-aminopropan wurden zum
Brei aus 121,5 mg (0,25 mmol) 5-[(Z)-(5-Trifluormethoxy-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure-1-oxy-7-azabenztriazolester
[hergestellt durch Aktivieren von (3Z)-3- ((3,3-dimethyl-4-carboxy-1-H-pyrrol-2-yl)methylen)-5-trifluormethoxy-1,3-dihydro-2H-indol-2-on
(1,768 g; 4,8 mmol) mit dem HATU-Reagenz (1,758 g; 4,8 mmol) in
Gegenwart der Hunig-Base (9,0 mmol; 1,58 ml) in DMF (25 ml) und
isolieren durch Verdampfung und Präzipitation mit wasserfreiem
Acetonitril und Trocknen unter einem Hochvakuum mit einer Ausbeute
von 85,5% (1,929 g) in reiner Form] in wasserfreiem Dimethylacetamid
(1,5 ml) gegeben. Die Mischung wurde für 30 Minuten gerührt und
im Hochvakuum verdampft. Der Reststoff wurde in einer Mischung aus
Methanol-Diethylamin 20:1 (3 ml) suspendiert, man ließ im Kühlschrank
(5°C) für 1 h kristallisieren,
es wurde gefiltert und das Präzipitat
wurde in eiskaltem Methanol gewaschen und im Hochvakuum getrocknet.
A. = 113 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 17
-
5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(1H-tetraazol-1-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 25)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 14 aus 72 mg des entsprechenden Amins hergestellt. A.
= 113 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 18
-
5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(1H-tetraazol-1-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 26)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 15 aus 72 mg des entsprechenden Amins hergestellt. A.
= 122 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 19
-
N-[2-hydroxy-3-(1H-tetraazol-1-yl)propyl]-2,4-dimethyl-5-[(Z)-[2-oxo-5-(trifluormethoxy)-1,2-dihydro-3H-indol-3-yliden]methyl]-1H-pyrrol-3-carboxamid
(Verbindung 27)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 16 aus 72 mg des entsprechenden Amins hergestellt. A.
= 118 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 20
-
N-[3-[(2R,6S)-2,6-Dimethylmorpholin-4-yl]-2-hydroxypropyl)-5-[(Z)-(5-fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 28)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 14 aus 95 mg des entsprechenden Amins hergestellt. A.
= 99 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 21
-
5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[3-[(2R,6S)-2,6-dimethylmorpholin-4-yl]-2-hydroxypropyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 29)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 15 aus 95 mg des entsprechenden Amins hergestellt. A.
= 101 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 22
-
N-[3-[(2R,6S)-2,6-dimethylmorpholin-4-yl]-2-hydroxypropyl]-2,4-dimethyl-5-[(Z)-[2-oxo-5-(trifluormethoxy)-1,2-dihydro-3H-indol-3-yliden]methyl]-1H-pyrrol-3-carboxamid
(Verbindung 30)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 16 aus 95 mg des entsprechenden Amins hergestellt. A.
= 89 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 23
-
5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[(2S)-2-hydroxy-3-(3-methyl-2,5-dioxoimidazolidin-1-yl)]2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 34)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 14 aus 95 mg des entsprechenden Amins hergestellt. A.
= 109 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 24
-
5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[(2S)-2-hydroxy-3-(3-methyl-2,5-dioxoimidazolidin-1-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 36)
-
Dies
wurde gemäß dem Verfahren
aus Beispiel 15 aus 95 mg des entsprechenden Amins hergestellt. A.
= 107 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 25
-
N-[(2S)-2-Hydroxy-3-(3-methyl-2,5-dioxoimidazolidin-1-yl)propyl]-2,4-dimethyl-5-{(Z)-[2-oxo-5-(trifluormethoxy)-1,2-dihydro-3H-indol-3-yliden]methyl}-1H-pyrrol-3-carboxamid
(Verbindung 35)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 16 aus 95 mg des entsprechenden Amins hergestellt. A.
= 123 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 26
-
5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[(2R)-2-hydroxy-3-(3-methyl-2,5-dioxoimidazolidin-1-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 31)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 14 aus 95 mg des entsprechenden Amins hergestellt. A.
= 110 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 27
-
5[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[(2R)-2-hydroxy-3-(3-methyl-2,5-dioxoimidazolidin-1-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
(Verbindung 32)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 15 aus 95 mg des entsprechenden Amins hergestellt. A.
= 103 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 28
-
N-[(2R)-2-hydroxy-3-(3-methyl-2,5-dioxoimidazolidin-1-yl)propyl]-2,4-dimethyl-5-{(Z)-[2-oxo-5-(trifluormethoxy)-1,2-dihydro-3H-indol-3-ylidenmethyl}-1H-pyrrol-3-carboxamid
(Verbindung 33)
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 16 aus 95 mg des entsprechenden Amins hergestellt. A.
= 120 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel
29 5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäureethylester
-
DMF
(4 ml, 3 Äq.)
wurde unter Rühren
in einem Eisbad gekühlt.
Dazu wurde POCl3 (1,1 Äq., 1,8 ml) gegeben. Nach 30
Minuten wurde eine Lösung
des 3,5-Dimethyl-4- Ethylesterpyrrols
(4 g, 17,4 mmol) in DMF (2 M, 9 ml) zum Reaktionsansatz gegeben
und das Rühren
fortgesetzt. Nach 10 min verfestigte sich die Reaktionsmischung.
Diese wurde mit 5 ml DMF verdünnt
und in einem 90°C Ölbad erhitzt.
Nach 1 h wurde die Reaktion auf Raumtemperatur abgekühlt, und
mit Wasser (100 ml) verdünnt
und mit 1 N NaOH auf pH = 11 basisch eingestellt. Das Produkt wurde
in Methylenchlorid (3 × 200
ml) extrahiert und die organischen Schichten wurden mit einer Salzlösung (200
ml) gewaschen, getrocknet (MgSO4) und auf
konzentriert, um 4,3 g (95%) an 5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäureethylester
als einen brauen Feststoff zu erhalten. 1H
NMR (360 MHz, DMSO-d6) δ 12,5
(br s, 1H, NH), 9,11 (s, 1H,
CHO), 7,35 (s, 5H, ArH), 3,98 (q, J = 6,8 und 7,2
Hz, 2H, OCH 2CH3), 2,48 (s, 3H, CH 3), 0,98 (t, J
= 7 Hz, 3H, OCH2CH 3)
-
5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäure
-
5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäureethylester
wurde in Wasser (100 ml) und Methanol (45 ml) unter Rühren gelöst. Es wurden
KOH (2 Äq.,
1,9 g) zugegeben und bei 100°C
erhitzt. Nach 2,5 h wurde sie auf Raumtemperatur abgekühlt und
der verbleibende Ester wurde durch Extrahieren in Ethylacetat (200
ml) entfernt, getrocknet und konzentriert. Die wässrige Schicht wurde unter
Verwendung von 2 N HCl auf pH = 3 sauer eingestellt. Der weiße Feststoff
wurde durch Filtration und Waschen mit Wasser entfernt. Der Feststoff
wurde aus Toluen rekonzentriert, mit Hexan zermahlen und getrocknet,
um 2 g (52%) eines cremefarbenen Feststoffes zu erhalten. 1H NMR (360 MHz, DMSO-d6) δ 12,46
(br s, 1H, CO2H), 11,95 (s, 1H, NH), 9,08 (s, 1H, CHO), 7,36 (s, 5H, ArH), 2,49 (s, 3H, CH 3). MS m/z (relative
Intensität
%, Ion) gemessen 229 (100, M+); berechnet
229,2.
-
5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäure(3-diethylamino-2-hydroxy-propyl)-amid
-
Eine
Mischung aus 5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäure (1,0
mg, 4,36 mmol), 1-Amino-3-diethylamino-2-propanol (950 mg, 6,54 mmol), DDC (900
mg, 4,36 mmol) und HOBt (884 mg, 6,54 mmol) in Chloroform (60 ml)
wurde bei RT für
12 h gerührt.
Der Reaktionsansatz wurde in gesättigtes
Natriumbicarbonat (60 ml) gerührt,
und dazu wurden 1 N NaOH (8 ml) gegeben. Er wurde dann mit EtOAc
(3 × 100
ml) extrahiert, mit Wasser und Salzlösung gewaschen, getrocknet
und konzentriert, um 400 mg an 5-Formyl-2-methyl-4-phenyl-1H-pyrrol-3-carbonsäure(3-diethylamino-2-hydroxy-propyl)-amid
zu erhalten.
-
Beispiel 30
-
Verfahren zur Synthese
der Verbindungen 11–21
-
Es
wurde eine 0,36 M Lösung
jedes Oxindols in DMSO als auch eine 0,576 M Lösung jedes Aldehyds hergestellt.
300 μl des
passenden Oxindols wurden mit 300 μl des passenden Aldehyds in
Gegenwart von 200 μl
DMSO vermischt. Dann werden 40 mg des Diethylentriamin-Radikalfängerharzes
zugegeben. Die Mischung wird in einem Robbins-Block angeordnet und
der Block wird versiegelt und in einem 60°C-Ofen angeordnet, in dem er
für 18
Stunden geschüttelt
wird.
-
Nach
18 Stunden wird der Robbins-Block aus dem Ofen entfernt. Das obere
Siegel des Blocks wird entfernt und 800 μl DMSO werden zur Mischung gegeben.
Dann wird der Block wieder versiegelt und abermals im 60°C-Ofen angeordnet,
in dem er sich fortwährend
für eine
Stunde dreht.
-
Nachdem
die 1 Stunde abgelaufen ist, wird der Robbins-Block aus dem Ofen entfernt, und dann
lässt man
ihn abkühlen.
Das untere Siegel des Robbins-Block wird vorsichtig entfernt und
der gesamte Block wird in die Filtrationsvorrichtung eingesetzt,
wodurch die neu synthetisierten Verbindungen vom Harz abgefiltert werden
können.
-
Beispiel 31
-
3-[1-H-(7-Azabenztriazolyl)-oxy]-2-hydroxy-1-aminopropan
-
4,083
g 1-Hydroxy-7-azabenztriazol (30 mmol) und 0,53 ml Diisopropylamin
(3 mmol) und 4,70 ml Epichlorhydrin in wasserfreiem Chloroform wurden
bei 60°C
für 2 Stunden
gerührt.
Die Reaktionsmischung wurde auf eine Säule aus Silica gegossen und
mit einer Mischung aus Chloroform-Methanol 100:3 eluiert. Das dabei erhaltene
Hydroxy-Chlor-Zwischenprodukt
(4,83 g, blassgelbes Öl,
70% A.) wurde in methanolischem Ammoniak (100 ml, gesättigt mit
Ammoniakgas) gelöst,
8,3 g Kaliumcarbonat wurde zugegeben und die Mischung wurde in einem
geschlossenen Kolben für
2 ½ Tagen
gerührt.
Die Reaktionsmischung wurde gefiltert und die Filtrate verdampft.
Der Rest wurde auf einer Silicasäule
in einer Mischung aus Chloroform-Methanol-konz. wässrigen
Ammoniak 80:15:1,5 gereinigt. A. = 2,793 g eines weißen kristallinen
Feststoffes (63% d. Th. des Chlorids).
-
3-[1-H-(Benztriazolyl)-oxy]-2-hydroxy-1-chlorpropan
und 3-[1-H-(Benztriazolyl-3-N-oxido)]-2-hydroxy-1-chlorpropan
-
12,162
g Hydroxyazabenztriazol (90 mmol), 1,59 ml Diisopropylethylamin
(9 mmol) und 14,1 ml Epichlorhydrin (180 mmol) in wasserfreiem Chloroform
wurden bei 55°C
für 2 Stunden
gerührt.
Die Reaktionsmischung wurde verdampft, der Rest wurde im Hochvakuum
getrocknet, dann auf einer Silicasäule in einer Mischung aus Chloroform-Methanol
100:5 gereinigt. Die ersten Fraktionen ergaben 3-[1-H-(Benztriazolyl)-oxy]-2-hydroxy-1-chlorpropan
10,570 g (blassgelber Honig; 51,5% A.), gefolgt von einer Fraktion
an 3-[1-H-(Benztriazolyl-3-N-oxido)]-2-hydroxy-1-chlorpropan 9,990
g (weißer,
kristalliner Feststoff, 48,5% A.).
-
3-[1-H-(Benztriazolyl-3-N-oxido)]-2-hydroxy-1-aminopropan
-
Wurde
durch Aminolyse von 3-[1-H-(Benztriazolyl-3-N-oxido)]-2-hydroxy-1-chlorpropan in Analogie zur
Synthese von 3-[1-H-(7-Azabenztriazolyl)-oxy]-2-hydroxy-1-aminopropan
hergestellt.
-
Beispiel 32
-
5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(3H-[1,2,3]triazolo[4,5-b]pyridin-3-yloxy)propyl]-2,4-dimenthyl-1H-pyrrol-3-carboxamid
(allgemeines Verfahren)
-
105
mg an 3-[1-H-(7-Azabenztriazolyl)-oxy]-2-hydroxy-1-aminopropan wurden
zum Brei aus 105 mg (0,25 mmol) an 5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4- dimenthyl-1H-pyrrol-3-carbonsäure-1-oxy-7-azabenztriazolester
[hergestellt durch Aktivieren von (3Z)-3-({3,3-dimethyl-4-carboxy-1-H-pyrrol-2-yl}methylen)-5-fluor-1,3-dihydro-2H-indol-2-on (480 mg;
1,6 mmol) mmol; 0,525 ml) in DMF (5 ml) und Isolieren durch Präzipitation
mit Chloroform (5 ml) und Trocknen im Hochvakuum mit einer Ausbeute
von 92% (579 mg) in reiner Form] in wasserfreiem Dimethylacetamid
(1,5 ml) gegeben. Die Mischung wurde für 30 min gerührt und
im Hochvakuum verdampft. Der Reststoff wurde in einer Mischung aus
Methanol-Diethylamin 20:1 (3 ml) suspendiert, man ließ ihn im
Kühlschrank
(5°C) für 1 h kristallisieren,
filterte ihn und das Präzipitat
wurde im eisgekühlten
Methanol gewaschen und im Hochvakuum getrocknet. A. = 121 mg eines
orangenen, kristallinen Feststoffes.
-
Beispiel 33
-
5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(3H-[1,2,3]triazolo[4,5-b]pyridin-3-yloxy)propyl-2,4-dimenthyl-1H-pyrrol-3-carboxamid
(allgemeines Verfahren)
-
105
mg an 3-[1-H-(7-Azabenztriazolyl)-oxy]-2-hydroxy-1-aminopropan wurden
zum Brei aus 109 mg (0,25 mmol) an 5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure-1-oxy-7-azabenztriazolester
[hergestellt durch Aktivieren von (3Z)-3-({3,3-dimethyl-4-carboxy-1-H-pyrrol-2-yl}methylen)-5-chlor-1,3-dihydro-2H-indol-2-on (1,520
g; 4,8 mmol) mit dem HATU-Reagenz (1,768 g; 4,65 mmol) in Gegenwart
der Hunig-Base (9,0 mmol; 1,58 ml) in DMF (20 ml) und isolieren
durch Präzipitation mit
Chloroform (20 ml) und Trocknen im Hochvakuum mit einer Ausbeute
von 94% (1,907 g) in reiner Form] in wasserfreiem Dimethylacetamid
(1,5 ml) gegeben. Die Mischung wurde für 30 Minuten gerührt und
im Hochvakuum verdampft. Der Reststoff wurde in einer Mischung aus
Methanol-Diethylamin 20:1 (3 ml) suspendiert, man ließ ihn im
Kühlschrank
(5°C) für 1 h kristallisieren,
er wurde gefiltert und das Präzipitat
wurde im eiskalten Methanol gewaschen und im Hochvakuum getrocknet.
A. = 130 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 34
-
5-[(Z)-(5-Trifluormethoxy-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(3H-[1,2,3]triazol[4,5-b]pyridin-3-yloxy)propyl]-2,4-dimenthyl-1H-pyrrol-3-carboxamid (allgemeines
Verfahren)
-
105
mg 3-[1-H-(7-Azabenztriazolyl)-oxy]-2-hydroxy-1-aminopropan wurden zum Brei aus 121,5
mg (0,25 mmol) an 5-[(Z)-(5-Trifluormethoxy-2-oxol-1,2-dihydro-3H-indol-3-yliden)methyl]-2,4-dimethyl-1H-pyrrol-3-carbonsäure-1-oxy-7-azabenztriazolester
[hergestellt durch Aktivieren von (3Z)-3-({3,3-Dimethyl-4-carboxy-1-H-pyrrol-2-yl}methylen)-5-trifluormethoxy-1,3-dihydro-2H-indol-2-on
(1,768 g; 4,8 mmol) mit dem HATU-Reagenz (1,758 g; 4,8 mmol) in
Gegenwart der Hunig-Base (9,0 mmol; 1,58 ml) in DMF (25 ml) und
isolieren durch Verdampfen und Präzipitieren mit wasserfreiem
Acetonitril und Trocknen im Hochvakuum bis zu einer Ausbeute von
85,5% (1,929 g) in reiner Form] in wasserfreiem Dimethylacetamid
(1,5 ml) gegeben. Die Mischung wurde für 30 min gerührt und
im Hochvakuum verdampft. Der Reststoff wurde in einer Mischung aus
Methanol-Diethylamin 20:1 (3 ml) suspendiert, man ließ ihn im
Kühlschrank
(5°C) für 1 h kristallisieren,
er wurde gefiltert und das Präzipitat
wurde in eiskaltem Methanol gewaschen und im Hochvakuum getrocknet.
A. = 142 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 35
-
5-[(Z)-(5-Fluor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(3-oxido-1H-1,2,3-benzotriazol-1-yl)propyl]-2,4-dimethyl-1H-pyrrol-3-carboxamid
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 32 aus 105 mg des entsprechenden Amins hergestellt. A.
= 120 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 36
-
5-[(Z)-(5-Chlor-2-oxo-1,2-dihydro-3H-indol-3-yliden)methyl]-N-[2-hydroxy-3-(3-oxido-1H-1,2,3-benzotriazol-1-yl)propyl-2,4-dimethyl-1H-pyrrol-3-carboxamid
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 33 aus 105 mg des entsprechenden Amins hergestellt. A.
= 127 mg eines orangenen, kristallinen Feststoffes.
-
Beispiel 37
-
N-[2-Hydroxy-3-(3-oxido-1H-1,2,3-benzotriazol-1-yl)propyl-2,4-dimethyl-5-[(Z)-[2-oxo-5-(trifluormethoxy)-1,2-dihydro-3H-indol-3-yliden]methyl)-1H-pyrrol-3-carboxamid
-
Sie
wurde gemäß dem Verfahren
aus Beispiel 34 aus 105 mg des entsprechenden Amins hergestellt. A.
= 141 mg eines orangenen, kristallinen Feststoffes.
-
Biologische Beispiele
-
Die
folgenden Assays werden angewendet, um solche Verbindungen zu finden,
welche den gewünschten,
optimalen Aktivitätsgrad
zeigen.
-
A. Assay-Verfahren.
-
Die
folgenden Assays können
verwendet werden, um das Aktivitätsniveau
und die Wirkung der verschiedenen Verbindungen der vorliegenden
Erfindung auf eine oder mehrere PK's zu bestimmen. Vergleichbare Assays
können
auf gleiche Art und Weise für
jede PK mittels im Stand der Technik gut bekannter Verfahren entworfen
werden.
-
Mehrere
der hierin beschriebenen Assays werden in einem ELISA (Enzyme-Linked
Immunosorbent Sandwich Assay, Festphasen-Enzymimmunoassay)-Format
durchgeführt
(Voller, et al., 1980, „Enzyme-Linked Immunosorbent
Assay," Manual of
Clinical Immunology, 2. Ausgabe, Rose und Friedman, Am. Soc. of
Microbiology, Washington, D. C., S. 359–371). Das allgemeine Verfahren
sieht wie folgt aus: Eine Verbindung wird in Zellen eingeführt, die
die Testkinase entweder auf natürliche
Weise oder rekombinant für
einen ausgewählten
Zeitraum exprimieren, wonach, wenn die Testkinase ein Rezeptor ist,
ein Ligand zugegeben wird, der bekanntermaßen den Rezeptor aktiviert.
Die Zellen werden lysiert und das Lysat wird in die Kammern einer
ELISA-Platte, die zuvor mit einem spezifischen Antikörper, der
das Substrat der enzymatischen Phosphorylierungsreaktion erkennt,
beschichtet wurde, übertragen.
Nichtsubstratkomponenten des Zelllysats werden weggewaschen und
die Phosphorylierungsmenge am Substrat wird mit einem Antikörper, der
Phosphotyrosin im Vergleich zu Kontrollzellen, die mit keiner Testverbindung
in Kontakt gebracht wurden, spezifisch erkennt, detektiert.
-
Die
derzeit bevorzugten Protokolle zum Durchführen der ELISA-Experimente
für spezifische
PK's werden weiter
unten bereitgestellt. Jedoch liegt die Anpassung dieser Protokolle
zum Bestimmen der Aktivität
der Verbindungen gegen andere RTK's als auch CTK's und STK's innerhalb des Wissensumfangs des Fachmanns.
Andere hierin beschriebene Assays messen die Menge an DNA, die als
Antwort auf die Aktivierung der Testkinase hergestellt wird, was
ein allgemeiner Maßstab
für eine
proliferative Antwort ist. Das allgemeine Verfahren für dieses
Assay sieht wie folgt aus: Eine Verbindung wird in Zellen eingeführt, die
die Testkinase entweder auf natürliche
Weise oder rekombinant für
einen ausgewählten
Zeitraum exprimieren, wonach, wenn die Testkinase ein Rezeptor ist,
ein Ligand zugegeben wird, der bekanntermaßen den Rezeptor aktiviert.
Nach zumindest einer Inkubation übernacht
wird ein DNA-markierendes Reagenz, wie zum Beispiel 5-Bromdesoxyuridin
(BrdU) oder H3-Thymidin zugegeben. Die Menge
der markierten DNA wird entweder mit einem Anti-BrdU-Antikörper oder
durch Messen der Radioaktivität
detektiert und wird mit Kontrollzellen, die nicht mit einer Testverbindung
in Kontakt gebracht wurden, verglichen.
-
GST-FLK-1 BIOASSAY
-
Dieses
Assay analysiert die Tyrosinkinaseaktivität von GST-Flk1 auf Poly(Glu-Tyr)-Peptide.
-
Materialien und Reagenzien:
-
- 1. Corning 96-Kammer-ELISA-Platten (Corning
Katalog Nr. 5805-96).
- 2. Poly(Glu-Tyr) 4:1, Lyophilisat (Sigma Katalog # P0275).
- 3. Herstellung von Poly(Glu,Tyr)(pEY) beschichteten Assay-Platten:
Beschichte mit 2 μg/Kammer
an Poly(Glu,Tyr)(pEY) in 100 μl
PBS, lagere für
2 Stunden bei Raumtemperatur oder bei 4°C übernacht. Man decke die Platten
gut ab, um ein Verdampfen zu verhindern.
- 4. PBS-Puffer: für
1 l, mische 0,2 g KH2PO4,
1,15 g Na2HPO4,
0,2 g KCl und 8 g NaCl in etwa 900 ml dH2O. Wenn
sich alle Reagenzien aufgelöst
haben, stelle den pH mit HCl auf 7,2 ein. Man stelle das Gesamtvolumen
mit dH2O auf 1 l ein.
- 5. PBST-Puffer: zu 1 l des PBS-Puffers, gebe man 1,0 ml Tween-20.
- 6. TBB-Blockierpuffer: für
1 l, mische man 1,21 g TRIS, 8,77 g NaCl und 1 ml Tween-20 in etwa
900 ml dH2O. Man stelle den pH mit HCl auf
7,2 ein. Man gebe 10 g BSA zu und rühre es zum Auflösen. Man
stelle das Gesamtvolumen mit dH2O auf 1
l ein. Man filtere, um fein verteiltes Material zu entfernen.
- 7. 1% BSA in PBS: um eine 1× Arbeitslösung herzustellen,
gebe man 10 g BSA zu etwa 990 ml PBS-Puffer und rühre es um es aufzulösen. Man
stelle das Gesamtvolumen mit PBS-Puffer auf 1 l ein, und filtere
es, um fein verteiltes Material zu entfernen.
- 8. 50 mM Hepes, pH 7,5.
- 9. GST-Flk1cd, aus einer sf9 rekombinanten Baculovirustransformation
(SUGEN, Inc.) gereinigt.
- 10. 4% DMSO in dH2O.
- 11. 10 mM ATP in dH2O.
- 12. 40 mM MnCl2
- 13. Kinaseverdünnungspuffer
(KDB): Man mische 10 ml Hepes (pH 7,5), 1 ml 5 M NaCl, 40 μl 100 mM
Natriumorthovanadat und 0,4 ml an 5% BSA in dH2O
mit 88,56 ml dH2O.
- 14. NUNC 96-Kammer V-bödige
Polypropylenplatten, Applied Scientific Katalog # AS-72092
- 15. EDTA: man mische 14,12 g Ethylendiamintetraessigsäure (EDTA)
mit etwa 70 ml dH2O. Man gebe 10 N NaOH
zu, bis sich das EDTA auflöst.
Man stelle den pH auf 8,0 ein. Man stelle das Gesamtvolumen mit dH2O auf 100 ml ein.
- 16. 10 Antikörperverdünnungspuffer: man mische 10
ml 5% BSA in PBS-Puffer mit 89,5 ml TBST.
- 17. monoklonaler Antiphosphotyrosinantikörper, der mit einer Meerrettichperoxidase
(PY99 HRP, Santa Cruz Biotech) konjugiert ist.
- 18. 2,2'-Azinobis(3-Ethylbenzthiazolin-6-Sulfonsäure (ABTS,
Moss, Kat. Nr. ABST).
- 19. 10% SDS.
-
Verfahrensablauf:
-
- 1. Man beschichte Corning 96-Kammer-ELISA-Platten
mit 2 μg
des polyEY-Peptids in sterilem PBS, wie in Schritt 3 von Materialien
und Reagenzien beschrieben.
- 2. Man entferne die ungebundene Flüssigkeit durch Umdrehen der
Platte aus den Kammern. Man wasche sie einmal mit TBST. Man klopfe
die Platte auf einem Papiertuch aus, um überschüssige Flüssigkeit zu entfernen.
- 3. Man gebe 100 μl
1% BSA in PBS in jede Kammer. Man inkubiere unter Schütteln für 1 h bei
Raumtemperatur.
- 4. Man wiederhole Schritt 2.
- 5. Man tränke
die Kammern mit 50 mmol HEPES (pH 7,5) (150 μl/Kammer).
- 6. Man verdünne
die Testverbindung mit dH2O/4% DMSO auf
das 4-fache der gewünschten
Assay-Endkonzentration
in 96-Kammer-Polypropylenplatten.
- 7. Man gebe 25 μl
der verdünnten
Testverbindung zur ELISA-Platte. Man gebe 25 μl an dH2O/4%
DMSO in die Kammern mit der Kontrolle.
- 8. Man gebe 25 μl
an 40 mM MnCl2 mit 4× ATP (2 μM) zu jeder Kammer.
- 9. Man gebe 25 μl
an 0,5 M EDTA zu den Kammern mit den Negativkontrollen.
- 10. Man verdünne
GST-Flk1 auf 0,005 μg
(5 ng)/Kammer mit KDB.
- 11. Man gebe 50 μl
des verdünnten
Enzyms zu jeder Kammer.
- 12. Man inkubiere unter Schütteln
für 15
Minuten bei Raumtemperatur.
- 13. Man stoppe die Reaktion durch Zugabe von 50 μl an 250
mM EDTA (pH 8,0).
- 14. Man wasche 3× mit
TBST und klopfe die Platte auf einem Papiertuch aus, um überschüssige Flüssigkeit zu
entfernen.
- 15. Man gebe 100 μl
pro Kammer des Antiphosphotyrosin-HRP-Konjugates zu, 1:5000 Verdünnung im
Antikörperverdünnungspuffer.
Man inkubiere unter Schütteln
für 90
min bei Raumtemperatur.
- 16. Man wasche wie unter Schritt 14.
- 17. Man gebe 100 μl
der auf Raumtemperatur temperierten ABTS-Lösung zu jeder Kammer.
- 18. Man inkubiere unter Schütteln
für 10
bis 15 Minuten. Man entferne alle Blasen.
- 19. Man stoppe die Reaktion durch Zugeben von 20 μl 10% SDS
zu jeder Kammer.
- 20. Man lese die Ergebnisse auf einem Dynatech MR7000 ELISA-Lesegerät mit einem
Testfilter bei 410 nM und einem Referenzfilter bei 630 nM aus.
-
PKY2-BIOASSAY
-
Dieses
Assay wird verwendet, um die in vitro-Kinaseaktivität von mit HA-Epitop markierten
Volllängen pyk2
(FL.pyk2-HA) in einem ELISA-Assay zu messen.
-
Materialien und Reagenzien:
-
- 1. Corning 96-Kammer-ELISA-Platten.
- 2. 12CA5 monoklonaler Anti-HA-Antikörper (SUGEN, Inc.)
- 3. PBS (Dulbecco's
Phosphat gepufferte Salzlösung
(Gibco Katalog # 450-1300EB)
- 4. TBST-Puffer: für
1 l mische man 8,766 g NaCl, 6,057 g TRIS und 1 ml 0,1% Triton X-100
in etwa 900 ml dH2O. Man stelle den pH auf
7,2 ein und stelle das Volumen auf 1 l ein.
- 5. Blockierpuffer: für
1 l mische man 100 g 10% BSA, 12,1 g 100 mM TRIS, 58,44 g 1 M NaCl
und 10 ml 1% TWEEN-20.
- 6. FL.pyk2-HA aus den sf9-Zelllysaten (SUGEN, Inc.).
- 7. 4% DMSO in MilliQue H2O.
- 8. 10 mM ATP in dH2O.
- 9. 1 M MnCl2.
- 10. 1 M MgCl2.
- 11. 1 M Dithiothreitol (DTT).
- 12. 10× Kinasepufferphosphorylierung:
Man mische 5,0 ml 1 M Hepes (pH 7,5), 0,2 ml 1 M MnCl2,
1,0 ml 1 M MgCl2, 1,0 ml 10% Triton X-100
in 2,8 ml dH2O. Man füge kurz vom Verwenden 0,1 ml
1 M DTT zu.
- 13. NUNC 96-Kammer V-bödige
Polypropylenplatten.
- 14. 500 mM EDTA in dH2O.
- 15. Antikörperverdünnungspuffer:
für 100
ml, 1 ml 5% BSA/PBS und 1 ml 10% Tween-20 in 88 ml TBS.
- 16. HRP-konjugiertes Anti-Ptyr PY99, Santa Cruz Biotech Kat.
Nr. SC-7020.
- 17. ABTS, Moss, Kat. Nr. ABST-2000.
- 18. 10% SDS.
-
Verfahrensablauf:
-
- 1. Man beschichte Corning 96-Kammer-ELISA-Platten
mit 0,5 μg
pro Kammer an 12CA5 Anti-HA-Antikörper in 100 μl PBS. Man
lagere sie Übernacht
bei 4°C.
- 2. Man entferne ungebundene HA-Antikörper durch Umdrehen der Platte
aus den Kammern. Man wasche die Platte mit dH2O.
Man klopfe die Platte auf ein Papiertuch aus, um überschüssige Flüssigkeit
zu entfernen.
- 3. Man gebe 150 μl
Blockierpuffer zu jeder Kammer. Man inkubiere unter Schütteln für 30 min
bei Raumtemperatur.
- 4. Man wasche die Platten 4× mit
TBS-T.
- 5. Man verdünne
das Lysat in PBS (1,5 μg
Lysat/100 μl
PBS).
- 6. Man gebe 100 μl
des verdünnten
Lysats zu jeder Kammer. Schüttle
sie bei Raumtemperatur für
1 h.
- 7. Man wasche wie unter Schritt 4.
- 8. Man gebe 50 μl
des 2× Kinase-Puffers
zur ELISA-Platte,
die das Eingefangene pyk2-HA enthält.
- 9. Man gebe 25 μl
der 400 μM
Testverbindung in 4% DMSO zu jeder Kammer. Für Kammern mit Kontrollen werden
nur 4% DMSO verwendet.
- 10. Man gebe 25 μl
an 0,5 M EDTA zu den Kammern mit den Negativkontrollen.
- 11. Man gebe 25 μl
an 20 μM
ATP zu allen Kammern. Man inkubiere unter Schütteln für 10 Minuten.
- 12. Man stoppe die Reaktion durch Zugabe von 25 μl an 500
mM EDTA (pH 8,0) zu allen Kammern.
- 13. Man wasche wie unter Schritt 4.
- 14. Man gebe 100 μl
mit HRP konjugiertes Anti-Ptyr, das auf 1:6000 verdünnt ist,
in Antikörperverdünnungspuffer
zu jeder Kammer. Man inkubiere unter Schütteln für 1 h bei Raumtemperatur.
- 15. Man wasche die Platte 3× mit
TBST und 1× mit
PBS.
- 16. Man gebe 100 μl
an ABST-Lösung
zu jeder Kammer.
- 17. Falls erforderlich, stoppe man die Entwicklungsreaktion
durch Zugabe von 20 μl
an 10% SDS zu jeder Kammer.
- 18. Man lese die Platte auf einem ELISA-Lesegerät mit einem
Testfilter bei 410 nM und einem Referenzfilter bei 630 nM aus.
-
FGFR1 BIOASSAY
-
Dieses
Assay wird verwendet, um die in vitro Kinaseaktivität für FGF1-R
in einem ELISA-Assay zu messen.
-
Materialien und Reagenzien:
-
- 1. Costar 96-Kammer-ELISA-Platten (Corning
Katalog # 3369.
- 2. Poly(Glu-Tyr) (Sigma Katalog # P0275).
- 3. PBS (Gibco Katalog # 450-1300EB)
- 4. 50 mM Hepes Pufferlösung.
- 5. Blockierpuffer (5% BSA/PBS).
- 6. Gereinigtes GST-FGFR1 (SUGEN, Inc.)
- 7. Kinaseverdünnungspuffer.
Man
mische 500 μl
1 M Hepes (GIBCO), 20 μl
5% BSA/PBS, 10 μl
100 mM Natriumorthovanadat und 50 μl 5 M NaCl.
- 8. 10 mM ATP.
- 9. ATP/MnCl2 Phosphorylierungsmischung:
Man mische 20 μl
ATP, 400 μl
1 M MnCl2 und 9,56 ml dH2O.
- 10. NUNC 96-Kammer V-bödige
Polypropylenplatten (Applied Scientific Katalog # AS-72092).
- 11. 0,5 M EDTA.
- 12. 0,05% TBST.
Man gebe 500 μl TWEEN zu einem Liter TBS.
- 13. Polyklonales Anti-Phosphotyrosinserum vom Hasen (SUGEN,
Inc.).
- 14. Anti-Hasen IgG-Peroxidasekonjugat von der Ziege (Biosource,
Katalog # ALI0404).
- 15. ABTS-Lösung.
- 16. ABTS/H2O2-Lösung.
-
Verfahrensablauf:
-
- 1. Man beschichte die Costar 96-Kammer-ELISA-Platten
mit 1 μg
pro Kammer Poly(Glu,Tyr) in 100 μl
PBS.
Man lagere sie über
Nacht bei 4°C.
- 2. Man wasche beschichtete Platten einmal mit PBS.
- 3. Man gebe 150 μl
an 5% BSA/PBS-Blockierpuffer zu jeder Kammer. Man inkubiere unter
Schütteln
für 1 h
bei Raumtemperatur.
- 4. Man wasche die Platte 2× mit
PBS und dann einmal mit 50 mM Hepes.
Man klopfe die Platten
auf einen Papiertuch aus, um überschüssige Flüssigkeit
und Blasen zu entfernen.
- 5. Man gebe 25 μl
an 0,4 mM Testverbindung in 4% DMSO oder 4% DMSO alleine (Kontrolle)
zur Platte.
- 6. Man verdünne
gereinigtes GST-FGFR1 im Kinaseverdünnungspuffer (5 ng Kinase/50 μl KDB/Kammer).
- 7. Man gebe 50 μl
der verdünnten
Kinase zu jeder Kammer.
- 8. Man starte die Kinasereaktion durch Zugabe von 25 μl/Kammer
an frisch hergestelltem ATP/Mn++ (0,4 ml 1 M MnCl2,
40 μl 10
mM ATP, 9,56 ml dH2O), frisch hergestellt).
- 9. Dies ist eine schnelle Kinasereaktion, die man mit 25 μl an 0,5
M EDTA in einer Art und Weise ähnlich der
Zugabe von ATP stoppen muss.
- 10. Man wasche die Platte 4× mit
frischem TBST.
- 11. Herstellen des Antikörperverdünnungspuffers:
pro 50 ml: Man mische 5 ml an 5% BSA, 250 μl an 5% Milch und 50 μl an 100
mM Natriumvanadat und stelle es mit 0,05% TBST auf das Endvolumen
ein.
- 12. Man gebe 100 μl
pro Kammer an Anti-Phosphotyrosin (1:10000 Verdünnung in ADB) zu. Man inkubiere unter
Rühren
für 1 h
bei Raumtemperatur.
- 13. Man wasche wie unter Schritt 10.
- 14. Man gebe 100 μl
pro Kammer an Biosource Anti-Hasen IgG-Peroxidasekonjugat von der
Ziege (1:6000 Verdünnung
in ADB) zu.
Man inkubiere unter Schütteln für 1 h bei Raumtemperatur.
- 15. Man wasche wie unter Schritt 10 und dann mit PBS, um Blasen
und überschüssiges TWEEN
zu entfernen.
- 16. Man gebe 100 μl
ABTS/H2O2-Lösung zu
jeder Kammer.
- 17. Man inkubiere unter Schütteln
für 10
bis 20 Minuten. Man entferne alle Blasen.
- 18. Man lese das Assay auf einem Dynatech MR7000 ELISA-Lesegerät aus: Testfilter
bei 410 nM, Referenzfilter 630 nM.
-
EGFR BIOASSAY
-
Dieses
Assay wird verwendet, um die in vitro Kinaseaktivität von FGF1-R
in einem ELISA-Assay zu messen.
-
Materialien und Reagenzien:
-
- 1. Corning 96-Kammer-ELISA-Platten.
- 2. SUMO1 monoklonaler Anti-EGFR-Antikörper (SUGEN, Inc.)
- 3. PBS.
- 4. TBST-Puffer.
- 5. Blockierpuffer: für
100 ml, mische man 5,0 g rosarote (Carnation) lösliche, fettfreie Milch® mit
100 ml PBS.
- 6. A431 Zelllysat (SUGEN, Inc.).
- 7. TBS-Puffer.
- 8. TBS + 10% DMSO: für
1 l, mische man 1,514 g TRIS, 2,192 g NaCl und 25 ml DMSO; man stelle
das Gesamtvolumen mit dH2O auf 1 Liter ein.
- 9. ATP (Adenosin-5'-Triphosphat
vom Pferdemuskel, Sigma Kat. Nr. A-5394), 1,0 mM Lösung in
dH2O. Dieses Reagenz sollte man kurz vor
der Verwendung herstellen und auf Eis lagern.
- 10. 1,0 mM MnCl2.
- 11. ATP/MnCl2-Phosphorylierungsmischung:
um 10 ml herzustellen, mische man 300 μl an 1 mM ATP, 500 μl MnCl2 und 9,2 ml dH2O.
Man
stelle es kurz vor der Verwendung her und lagere es auf Eis.
- 12. NUNC 96-Kammer V-bödige
Polypropylenplatten.
- 13. EDTA.
- 14. Polyklonales Anti-Phosphotyrosinserum vom Hasen (SUGEN,
Inc.).
- 15. Anti-Hasen IgG-Peroxidasekonjugat von der Ziege (Biosource
Kat. Nr. ALI0404).
- 16. ABTS.
- 17. 30% Wasserstoffperoxid.
- 18. ABTS/H2O2.
- 19. 0,2 M HCl.
-
Verfahrensablauf:
-
- 1. Man beschichte Corning 96-Kammer-ELISA-Platten
mit 0,5 μg
SUMO1 in 100 μl
PBS pro Kammer und lagere sie bei 4°C über Nacht.
- 2. Man entferne ungebundenes SUMO1 durch Umdrehen der Platte,
um überschüssige Flüssigkeit
zu entfernen, aus den Kammern. Man wasche 1× mit dH2O.
Man klopfe die Platte auf einem Papiertuch aus, um überschüssige Flüssigkeit
zu entfernen.
- 3. Man gebe 150 μl
des Blockierpuffers zu jeder Kammer.
Man inkubiere unter Schütteln für 30 min
bei Raumtemperatur.
- 4. Man wasche die Platte 3× mit
deionisiertem Wasser und dann einmal mit TBST. Man klopfe die Platte
auf einem Papiertuch aus, um überschüssige Flüssigkeit
und Blasen zu entfernen.
- 5. Man verdünne
das Lysat in PBS (7 μg
Lysat/100 μl
PBS).
- 6. Man gebe 100 μl
des verdünnten
Lysats zu jeder Kammer. Man schüttle
bei Raumtemperatur für
1 h.
- 7. Man wasche die Platten wie weiter oben unter 4.
- 8. Man gebe 120 μl
TBS zur ELISA-Platte, die das eingefangene EGFR enthält.
- 9. Man verdünne
die Testverbindung 1:10 in TBS und gebe sie in die Kammer.
- 10. Man gebe 13,5 μl
der verdünnten
Testverbindung zur ELISA-Platte. Man gebe 13,5 μl TBS in 10% DMSO zu den Kammern
mit den Kontrollen.
- 11. Man inkubiere unter Schütteln
für 30
Minuten bei Raumtemperatur.
- 12. Man gebe 15 μl
Phosphorylierungsmischung zu allen Kammern, mit Ausnahme der Kammer
mit der Negativkontrolle. Das Kammerendvolumen sollte bei etwa 150 μl mit 3 μM ATP/5 mM
MnCl2 Endkonzentration in jeder Kammer liegen.
Man inkubiere unter Schütteln
für 5 Minuten.
- 13. Man stoppe die Reaktion durch Zugabe von 16,5 μl EDTA-Lösung, während geschüttelt wird.
Man schüttle
für eine
zusätzliche
Minute.
- 14. Man wasche 4× mit
deionisiertem Wasser, 2× mit
TBST.
- 15. Man gebe 100 μl
Anti-Phosphotyrosin (1:3000 Verdünnung
in TBST) pro Kammer zu. Man inkubiere unter Schütteln für 30–45 min bei Raumtemperatur.
- 16. Man wasche wie weiter oben unter 4.
- 17. Man gebe 100 μl
Biosource Anti-Hasen IgG-Peroxidasekonjugat
von der Ziege (1:2000 Verdünnung
in TBST) zu jeder Kammer. Man inkubiere unter Schütteln für 30 min
bei Raumtemperatur.
- 18. Man wasche wie weiter oben unter 4.
- 19. Man gebe 100 μl
ABTS/H2O2-Lösung zu
jeder Kammer.
- 20. Man inkubiere 5 bis 10 Minuten unter Schütteln. Man entferne alle Blasen.
- 21. Falls erforderlich, stoppe man die Reaktion durch Zugabe
von 100 μl
0,2 M HCl pro Kammer.
- 22. Man lese das Assay auf einem Dynatech MR7000 ELISA-Lesegerät aus: Testfilter
bei 410 nM, Referenzfilter bei 630 nM.
-
PDGFR BIOASSAY
-
Dieses
Assay wird verwendet, um die in vitro Kinaseaktivität von FGF1-R
in einem ELISA-Assay zu messen.
-
Materialien und Reagenzien:
-
- 1. Corning 96-Kammer-ELISA-Platten.
- 2. 28D4C10 monoklonaler Anti-PDGFR-Antikörper (SUGEN, Inc.)
- 3. PBS.
- 4. TBST-Puffer.
- 5. Blockierpuffer (der gleiche wie für das EGFR-Bioassay).
- 6. PDGFR-β exprimierendes
NIH 3T3-Zelllysat (SUGEN, Inc.).
- 7. TBS-Puffer.
- 8. TBS + 10% DMSO.
- 9. ATP.
- 10. MnCl2.
- 11. Kinasepufferphosphorylierungsmischung: für 10 ml, mische man 250 μl 1 M TRIS,
200 μl 5
M NaCl, 100 μl
1 M MnCl2 und 50 μl 100 mM Triton X-100 in genügend dH2O, um 10 ml herzustellen.
- 12. NUNC 96-Kammer V-bödige
Polypropylenplatten.
- 13. EDTA.
- 14. Polyklonales Anti-Phosphotyrosinserum vom Hasen (SUGEN,
Inc.).
- 15. Anti-Hasen IgG-Peroxidasekonjugat von der Ziege (Biosource
Kat. Nr. ALI0404).
- 16. ABTS.
- 17. Wasserstoffperoxid, 30%-Lösung.
- 18. ABTS/H2O2.
- 19. 0,2 M HCl.
-
Verfahrensablauf:
-
- 1. Man beschichte Corning 96-Kammer-ELISA-Platten
mit 0,5 μg
28D4C10 in 100 μl
PBS pro Kammer und lagere sie über
Nacht bei 4°C.
- 2. Man entferne ungebundenes 28D4C10 durch Umdrehen der Platten,
um Flüssigkeit
zu entfernen, aus den Kammern. Man wasche 1× mit dH2O.
Man klopfe die Platten auf einem Papiertuch aus, um überschüssige Flüssigkeit
zu entfernen.
- 3. Man gebe 150 μl
des Blockierpuffers zu jeder Kammer. Man inkubiere unter Schütteln für 30 min
bei Raumtemperatur.
- 4. Man wasche die Platte 3× mit
deionisiertem Wasser und dann einmal mit TBST. Man klopfe die Platte
auf einem Papiertuch aus, um überschüssige Flüssigkeit
und Blasen zu entfernen.
- 5. Man verdünne
das Lysat in HNTG (10 μg
Lysat/100 μl
HNTG).
- 6. Man gebe 100 μl
des verdünnten
Lysats zu jeder Kammer. Man schüttle
sie bei Raumtemperatur für
60 min.
- 7. Man wasche die Platten wie unter Schritt 4 beschrieben.
- 8. Man gebe 80 μl
der Kinasepufferarbeitsmischung zur ELISA-Platte, die das eingefangene
PDGFR enthält.
- 9. Man verdünne
die Testverbindung 1:10 in TBS in 96-Kammer Polypropylenplatten.
- 10. Man gebe 10 μl
der verdünnten
Testverbindung zur ELISA-Platte. Zu den Kammern mit den Kontrollen gebe
man 10 μl
TBS + 10% DMSO. Man inkubiere unter Schütteln für 30 Minuten bei Raumtemperatur.
- 11. Man gebe 10 μl
ATP direkt zu allen Kammern, mit Ausnahme der Kammer mit der Negativkontrolle
(das Kammerendvolumen sollte bei etwa 100 μl mit 20 μM ATP in jeder Kammer liegen).
Man inkubiere 30 Minuten unter Schütteln.
- 12. Man stoppe die Reaktion durch Zugabe von 10 μl EDTA-Lösung zu
jeder Kammer.
- 13. Man wasche 4× mit
deionisiertem Wasser und zweimal mit TBST.
- 14. Man gebe 100 μl
Anti-Phosphotyrosin (1:3000 Verdünnung
in TBST) pro Kammer zu. Man inkubiere unter Schütteln für 30–45 min bei Raumtemperatur.
- 15. Man wasche wie unter Schritt 4.
- 16. Man gebe 100 μl
Biosource Anti-Hasen IgG-Peroxidasekonjugat
von der Ziege (1:2000 Verdünnung
in TBST) zu jeder Kammer. Man inkubiere unter Schütteln für 30 min
bei Raumtemperatur.
- 17. Man wasche wie unter Schritt 4.
- 18. Man gebe 100 μl
der ABTS/H2O2-Lösung zu
jeder Kammer.
- 19. Man inkubiere für
10 bis 30 Minuten unter Schütteln.
Man entferne alle Blasen.
- 20. Falls erforderlich, stoppe man die Reaktion durch Zugabe
von 100 μl
0,2 M HCl pro Kammer.
- 21. Man lesen das Assay auf einem Dynatech MR7000 ELISA-Lesegerät mit einem
Testfilter bei 410 nM und einem Referenzfilter bei 630 nM aus.
-
ZELLULÄRES HER-2 KINASE-ASSAY
-
Dieses
Assay wird verwendet, um die HER-2 Kinaseaktivität in ganzen Zellen in einem
ELISA-Format zu messen.
-
Materialien und Reagenzien:
-
- 1. DMEM (GIBCO Katalog #11965-092).
- 2. Fötales
Rinderserum (FBS, GIBCO Katalog #16000-044), hitzeinaktiviert für 30 Minuten
bei 56°C
in einem Wasserbad
- 3. Trypsin (GIBCO Katalog #25200-056).
- 4. L-Glutamin (GIBCO Katalog #25030-081)
- 5. HEPES (GIBCO Katalog #15630-080).
- 6. Wachstumsmedium
Man mische 500 ml DMEM, 55 ml hitzeinaktiviertes
FBS, 10 ml HEPES und 5,5 ml L-Glutamin.
- 7. Hungermedium
Man mische 500 ml DMEM, 2,5 ml hitzeinaktiviertes
FBS, 10 ml HEPES und 5,5 ml L-Glutamin.
- 8. PBS.
- 9. Flachbödige
96-Kammer Gewebekultur-Mikrotiter-Platten (Corning Katalog #25860).
- 10. 15 cm Gewebekulturschalen (Corning Katalog #08757148).
- 11. Corning 96-Kammer-ELISA-Platten.
- 12. NUNC 96-Kammer V-bödige
Polypropylenplatten.
- 13. Costar Patronen zum Übertragen
für den
Transtar 96 (Costar Katalog #7610).
- 14. SUMO1: Monoklonaler Anti-EGFR-Antikörper (SUGEN, Inc.).
- 15. TBST-Puffer.
- 16. Blockierpuffer: 5% Carnation lösliche Milch® in
PBS.
- 17. EGF-Ligand: EGF-201, Shinko American, Japan.
Man suspendiere
Pulver in 100 μl
an 10 mM HCl. Man gebe 100 μl
10 mM NaOH zu. Man gebe 800 μl
PBS zu und übertrage
es in ein Eppendorfgefäß und lagere
es bis zum Gebrauch bei –20°C.
- 18. HNTG-Lysepuffer
Für
die Stammlösung
5× HNTG,
mische man 23,83 g Hepes, 43,83 g NaCl, 500 ml Glycerol und 100
ml Triton X-100 und genügend
dH2O, um 1 l der Gesamtlösung herzustellen.
Für 1× HNTG*,
mische man 2 ml HNTG, 100 μl
0,1 M Na3VO4, 250 μl 0,2 M Na4P2O7 und
100 μl EDTA.
- 19. EDTA.
- 20. Na3VO4.
Um eine Stammlösung
herzustellen, mische man 1,84 g Na3VO4 mit 90 ml dH2O.
Man stelle den pH auf 10 ein. Man koche sie erst für 1 Minute
in der Mikrowelle (die Lösung
wird klar). Kühle
sie auf Raumtemperatur ab. Man stelle den pH auf 10 ein.
Man
wiederhole den Erhitzungs/Abkühlungs-Zyklus,
bis der pH bei 10 bleibt.
- 21. 200 mM Na4P2O7.
- 22. Polyklonales Antiserum vom Hasen, das für Phosphotyrosin spezifisch
ist (Anti-Ptyr-Antikörper, SUGEN,
Inc.).
- 23. Affinitätsgereinigtes
Antiserum, Anti-Hasen IgG-Antikörper von
der Ziege, Peroxidasekonjugat (Biosource Kat. # ALI0404).
- 24. ABTS-Lösung.
- 25. 30% Wasserstoffperoxidlösung.
- 26. ABTS/H2O2.
- 27. 0,2 M HCl.
-
Verfahrensablauf:
-
- 1. Man beschichte Corning 96-Kammer-ELISA-Platten
mit SUMO1 bei 1,0 μg
pro Kammer in PBS, 100 μl Endvolumen/Kammer.
Man lagere sie Übernacht
bei 4°C.
- 2. Am Tag des Gebrauchs, entferne man den Beschichtungspuffer
und wasche die Platte 3 mal mit dH2O und
einmal mit TBST-Puffer. Alle Waschungen in diesem Assay sollte man
auf diese Weise durchführen, soweit
nichts anderes angegeben wird.
- 3. Man gebe 100 μl
des Blockierpuffers zu jeder Kammer. Man inkubiere die Platte unter
Schütteln
für 30 min
bei Raumtemperatur. Kurz vorm Gebrauch, wasche man die Platte.
- 4. Man verwende die EGFr/HER-2 chimäre/3T3-C7-Zelllinie für dieses Assay.
- 5. Man wähle
Schalen mit 80–90%
Konfluenz. Man sammle die Zellen durch Trypsinierung und zentrifugiere sie
für 5 min
bei 1000 rpm bei Raumtemperatur.
- 6. Man resuspendiere die Zellen in Hungermedium und zähle sie
mit Trypanblau. Es ist eine Lebensfähigkeit von 90% erforderlich.
Man impfe die Zellen in Hungermedium bei einer Dichte von 2500 Zellen
pro Kammer an, 90 μl
pro Kammer, in einer 96-Kammer Mikrotiterplatte. Man inkubiere die
angeimpften Zellen Übernacht
bei 37° bei
5% CO2.
- 7. Man starte das Assay zwei Tage nach dem Animpfen.
- 8. Man löse
die Testverbindungen in 4% DMSO auf. Man verdünnt die Proben dann direkt
weiter auf Platten mit Hunger-DMEM. Üblicherweise wird diese Verdünnung 1:10
oder größer sein.
Man überträgt dann
alle Kammern mit einer weiteren 1:10-Verdünnung
(10 μl Probe
und Medium in 90 μl
Hungermedium) auf die Zellplatte. Die DMSO-Endkonzentration sollte 1% oder niedriger
sein. Eine Standardserienverdünnung kann
ebenfalls verwendet werden.
- 9. Man inkubiere bei 5% CO2, bei 37°C für 2 Stunden.
- 10. Man stelle den EGF-Liganden durch Verdünnen der Stamm-EGF-Lösung (16,5 μM) in warmem
DMEM auf 150 nM her.
- 11. Man stelle frisches HNTG* her, dass für 100 μl pro Kammer ausreichend ist;
man stelle es auf Eis.
- 12. Nach 2 Stunden Inkubation mit der Testverbindung, gebe man
hergestellten EGF-Liganden zu den Zellen, 50 μl pro Kammer, für eine Endkonzentration
von 50 nM. Die Kammern mit der Positivkontrolle erhalten die gleiche
Menge an EGF. Die Negativkontrollen erhalten kein EGF. Man inkubiere
bei 37°C
für 10
min.
- 13. Man entferne die Testverbindung, EGF und DMEM. Man wasche
die Zellen einmal mit PBS.
- 14. Man gebe HNTG* zu den Zellen, 100 μl pro Kammer. Man stelle es
für 5 Minuten
auf Eis. In der Zwischenzeit entferne man den Blockierpuffer von
der ELISA-Platte und wasche sie.
- 15. Man schabe die Zellen mit einem Mikropipettor von der Platte
und homogenisiere das Zellmaterial durch wiederholtes Aspirieren
und Dispensieren des HNTG*- Lysepuffers.
Man übertrage
das Lysat auf eine beschichtete, blockierte, gewaschene ELISA-Platte
oder man verwendet eine Costar-Patrone zum Übertragen des Lysats auf die
Platte.
- 16. Man inkubiere unter Schütteln
bei Raumtemperatur für
1 h.
- 17. Man entferne das Lysat und wasche. Man gebe frisch verdünnten Anti-Ptyr-Antikörper (1:3000
in TBST) zur ELISA-Platte, 100 μl
pro Kammer.
- 18. Man inkubiere unter Schütteln
bei Raumtemperatur für
30 min.
- 19. Man entferne den Anit-Ptyr-Antikörper und wasche. Man gebe frisch
verdünnten
BIOSOURCE-Antikörper
zur ELISA-Platte (1:8000 in TBST, 100 μl pro Kammer).
- 20. Man inkubiere unter Schütteln
bei Raumtemperatur für
30 min.
- 21. Man entferne den BIOSOURCE-Antikörper und wasche. Man gebe frisch
hergestellte ABTS/H2O2-Lösung zur
ELISA-Platte, 100 μl
pro Kammer.
- 22. Man inkubiere unter Schütteln
für 5–10 Minuten.
Man entferne alle Blasen.
- 23. Man stoppe die Reaktion durch Zugabe von 100 μl an 0,2
M HCl pro Kammer.
- 24. Man lese das Assay auf einen Dynatech MR7000 ELISA-Lesegerät mit einem
Testfiltersatz bei 410 nM und einem Referenzfilter bei 630 nM aus.
-
CDK2/CYCLIN A ASSAY
-
Dieses
Assay wird verwendet, um die in vitro Serin/Threoninkinaseaktivität des humanen
cdk2/Cyclin A in einem Scintillation Proximity Assay (SPA) zu messen.
-
Materialien und Reagenzien:
-
- 1. Wallac 96-Kammer Polyethylenterephthalat
(flexi)-Platten
(Wallac Katalog # 1450-401).
- 2. Amersham Redivue [γ33P] ATP (Amersham Katalog #AH 9968).
- 3. Amersham Streptavidin beschichtete Polyvinyltoluen SPA-Kügelchen
(Amersham Katalog #RPNQ0007). Man sollte die Kügelchen in PBS ohne Magnesium
oder Calcium bei 20 mg/ml rekonstituieren.
- 4. Aktivierter cdk2/Cyclin A-Enzymkomplex, der aus Sf9-Zellen
(SUGEN, Inc.) aufgereinigt wurde.
- 5. Biotinyliertes Peptid-Substrat (Debtide). Das Peptid Biotin-X-PKTPKKAKKL
wird in dH2O bei einer Konzentration von
5 mg/ml aufgelöst.
- 6. Peptid/ATP-Mischung: für
10 ml, mische man 9,979 ml dH2O, 0,00125
ml „kaltes" ATP, 0,010 ml Debtide und
0,010 ml γ33P ATP. Die endgültige Konzentration pro Kammer
wird bei 0,5 μM „kaltem" ATP, 0,1 μg Debtide
und 0,2 μCi γ33P
ATP liegen.
- 7. Kinasepuffer: für
10 ml, mische man 8,85 ml dH2O, 0,625 ml
TRIS (pH 7,4), 0,25 ml 1 M MgCl2, 0,25 ml 10%
NP40 und 0,025 ml 1 M DTT und gebe dies kurz vor der Verarbeitung
zu.
- 8. 10 mM ATP in dH2O.
- 9. 1 M TRIS, pH wird mit HCl auf 7,4 eingestellt.
- 10. 1 M MgCl2.
- 11. 1 M DTT.
- 12. PBS (Gibco Katalog # 14190-144).
- 13. 0,5 M EDTR.
- 14. Stopplösung:
für 10
ml, mische man 9,25 ml PBS, 0,005 ml 100 mM ATP, 0,1 ml 0,5 M EDTA,
0,1 ml 10% Triton X-100 und 1,25 ml an 20 mg/ml SPA Kügelchen.
-
Verfahrensablauf:
-
- 1. Man stelle die Lösungen mit den Testverbindungen
bei 5× der
gewünschten
Endkonzentration in 5% DMSO her. Man gebe 10 μl zu jeder Kammer. Man verwende
10 μl 5%
DMSO alleine in Kammern mit den Negativkontrollen.
- 2. Man verdünne
5 μl der
cdk2/Cyclin A-Lösung
mit 2,1 ml 2× Kinasepuffer.
- 3. Man gebe 20 μl
Enzym zu jeder Kammer.
- 4. Man gebe 10 μl
an 0,5 M EDTA zu den Kammern mit der Negativkontrolle.
- 5. Um die Kinasereaktion zu starten, gebe man 20 μl der Peptid/ATP-Mischung
zu jeder Kammer. Man inkubiere ohne zu schütteln für 1 h.
- 6. Man gebe 200 μl
Stopplösung
zu jeder Kammer.
- 7. Man behalte alles für
wenigstens 10 min bei.
- 8. Man zentrifugiere die Platte bei etwa 2300 rpm für 3–5 min.
- 9. Man zähle
die Platte mittels Trilux oder einem ähnlichen Lesegerät aus.
-
MET TRANSPHOSPHORYLIERUNGSASSAY
-
Dieses
Assay wird verwendet, um die Phosphotyrosinniveaus auf einem Poly(Glutaminsäure:Tyrosin (4:1))-Substrat
als Mittel zum Identifizieren von Agonisten/Antagonisten der met
Transphosphorylierung des Substrates zu messen.
-
Materialien und Reagenzien:
-
- 1. Corning 96-Kammer-ELISA-Platten, Corning
Katalog # 25805-96.
- 2. Poly(Glu,Tyr) 4:1, Sigma, Kat. Nr. P 0275.
- 3. PBS, Gibco Katalog # 450-1300EB
- 4. 50 mM HEPES
- 5. Blockierpuffer: Man löse
25 g Rinderserumalbumin, Sigma Kat. Nr. A-7888, in 500 ml PBS auf
und filtere es durch einen 4 μm
Filter.
- 6. Gereinigtes GST-Fusionsprotein, das die Met-Kinasedomäne enthält, Sugen,
Inc.
- 7. TBST-Puffer.
- 8. 10% wasserhaltiges (MilliQue H2O)
DMSO.
- 9. 10 ml wasserhaltiges (dH2O) Adenosin-5'-Triphosphat, Sigma Kat. Nr. A-5394.
- 10. 2× Kinaseverdünnungspuffer:
für 100
ml, mische man 10 ml 1 M HEPES bei pH 7,5 mit 0,4 ml 5% BSA/PBS,
0,2 ml 0,1 M Natriumorthovanadat und 1 ml 5 M Natriumchlorid in
88,4 ml dH2O.
- 11. 4× ATP-Reaktionsmischung:
für 10
ml, mische man 0,4 ml 1 M Manganchlorid und 0,02 ml 0,1 M ATP in
9,56 ml dH2O.
- 12. 4× Mischung
für Negativkontroll:
für 10
ml, mische man 0,4 ml 1 M Manganchlorid in 9,6 ml dH2O.
- 13. NUNC 96-Kammer V-bödige
Polypropylenplatten, Applied Scientific Catalog # S-72092.
- 14. 500 mM EDTA.
- 15. Antikörperverdünnungspuffer:
für 100
ml, mische man 10 ml 5% BSA/PBS, 0,5 ml 5% Carnation lösliche Milch® in
PBS und 0,1 ml 0,1 M Natriumorthovanadat in 88,4 ml TBST.
- 16. Polyklonaler Anti-Phosphotyrosinantikörper vom Hasen, Sugen, Inc.
- 17. Anti-Hasen Meerrettichperoxidase konjugierter Antikörper von
der Ziege, Biosource, Inc.
- 18. ABTS-Lösung:
für 1 l,
mische man 19,21 g Zitronensäure,
35,49 g Na2HPO4 und
500 mg ABTS mit ausreichend dH2O um 1 l
herzustellen.
- 19. ABTS/H2O2:
Man mische 15 ml ABST-Lösung
mit 2 μl
H2O2 fünf Minuten
vor der Verwendung.
- 20. 0,2 M HCl.
-
Verfahrensablauf:
-
- 1. Man beschichte ELISA-Platten mit 2 μg Poly(Glu-Tyr)
in 100 μl
PBS und lagere sie Übernacht
bei 4°C.
- 2. Man blockiere die Platte mit 150 μl an 5% BSA/PBS für 60 min.
- 3. Man wasche die Platte zweimal mit PBS und einmal mit 50 mM
Hepespuffer pH 7,4.
- 4. Man gebe 50 μl
der verdünnten
Kinase zu allen Kammern. (Die gereinigte Kinase wird mit dem Kinaseverdünnungspuffer
verdünnt.
Die Endkonzentration sollte bei 10 ng/Kammer liegen.)
- 5. Man gebe 25 μl
der Testverbindung (in 4% DMSO) oder DMSO alleine (4% in dH2O) für
Kontrollen zur Platte.
- 6. Man inkubiere die Kinase/Verbindungsmischung für 15 Minuten.
- 7. Man gebe 25 μl
an 40 mM MnCl2 zu den Kammern mit der Negativkontrolle.
- 8. Man gebe 25 μl
der ATP/MnCl2-Mischung zu allen anderen
Kammern (mit Ausnahme der Negativkontrollen). Man inkubiere für 5 min.
- 9. Man gebe 25 μl
500 mM EDTA hinzu, um die Reaktion zu stoppen.
- 10. Man wasche die Platte 3× mit
TBST.
- 11. Man gebe 100 μl
des polyklonalen Anti-Ptyr vom Hasen, der auf 1:10000 im Antikörperverdünnungspuffer
verdünnt
wurde, zu jeder Kammer. Man inkubiere unter Schütteln bei Raumtemperatur für eine Stunde.
- 12. Man wasche die Platte 3× mit
TBST.
- 13. Man verdünne
den Biosource HRP konjugierten Anti-Hasen-Antikörper 1:6000 im Antikörperverdünnungspuffer.
Man gebe 100 μl
pro Kammer zu und inkubiere bei Raumtemperatur unter Schütteln für eine Stunde.
- 14. Man wasche die Platte 1× mit
PBS.
- 15. Man gebe 100 μl
ABTS/H2O2-Lösung zu
jeder Kammer.
- 16. Falls erforderlich, stoppe man die Entwicklungsreaktion
durch Zugabe von 100 μl
0,2 M HCl pro Kammer.
- 17. Man lese die Platte auf einem Dynatech MR7000 ELISA-Lesegerät mit dem
Testfilter bei 410 nM und dem Referenzfilter bei 630 nM aus.
-
IGF-1 TRANSPHOSPHORYLIERUNGSASSAY
-
Dieses
Assay wird verwendet, um das Phosphotyrosinniveau in Poly(Glutaminsäure:Tyrosin)
(4:1) zur Identifikation von Agonisten/Antagonisten der gst-IGF-Transphosphorylierung
eines Substrates zu messen.
-
Materialien und Reagenzien:
-
- 1. Corning 96-Kammer-ELISA-Platten.
- 2. Poly(Glu-Tyr) (4:1), Sigma Kat. Nr. P 0275.
- 3. PBS, Gibco Katalog # 450-1300EB.
- 4. 50 mM HEPES.
- 5. TBB-Blockierpuffer: für
1 l, mische man 100 g BSA, 12,1 g TRIS (pH 7,5), 58,44 g Natriumchlorid
und 10 ml 1% TWEEN-20.
- 6. Gereinigtes GST-Fusionsprotein, das die IGF-1-Kinasedomäne (Sugen,
Inc.) enthält.
- 7. TBST-Puffer: für
1 l, mische man 6,057 g Tris, 8,766 g Natriumchlorid und 0,5 ml
TWEEN-20 mit genügend
dH2O, um 1 Liter herzustellen.
- 8. 4% DMSO in Milli-Q H2O.
- 9. 10 mM ATP in dH2O.
- 10. 2× Kinaseverdünnungspuffer:
für 100
ml, mische man 10 ml 1 M HEPES (pH 7,5), 0,4 ml 5% BSA in dH2O, 0,2 ml 0,1 M Natriumorthovanadat und
1 ml 5 M Natriumchlorid mit genügend
dH2O, um 100 ml herzustellen.
- 11. 4× ATP-Reaktionsmischung:
für 10
ml, mische man 0,4 ml 1 M MnCl2 und 0,008
ml 0,01 M ATP und 9,56 ml dH2O.
- 12. 4× Mischung
für Negativkontrollen:
Man mische 0,4 ml 1 M Manganchlorid in 9,60 ml dH2O.
- 13. NUNC 96-Kammer V-bödige
Polypropylenplatten.
- 14. 500 mM EDTA in dH2O.
- 15. Antikörperverdünnungspuffer:
für 100
ml, mische man 10 ml 5% BSA in PBS, 0,5 ml 5% Carnation lösliche Milch
ohne Fett® in
PBS und 0,1 ml 0,1 M Natriumorthovanadat in 88,4 ml TBST.
- 16. Polyklonaler Antiphosphotyrosin-Antikörper vom Hasen, Sugen, Inc.
- 17. Anti-Hasen HRP konjugierter Antikörper von der Ziege, Biosource.
- 18. ABTS-Lösung.
- 20. ABTS/H2O2:
Man mische 15 ml ABTS mit 2 μl
H2O2 5 Minuten vor
der Verwendung.
- 21. 0,2 M HCl in dH2O.
-
Verfahrensablauf:
-
- 1. Man beschichte eine ELISA-Platte mit 2,0 μg/Kammer
Poly(Glu,Tyr) 4:1 (Sigma P0275) in 100 μl PBS. Man lagere die Platte Übernacht
bei 4°C.
- 2. Man wasche die Platte einmal mit PBS.
- 3. Man gebe 100 μl
des TBB-Blockierpuffers zu jeder Kammer.
Man inkubiere die
Platte für
1 Stunde unter Schütteln
bei Raumtemperatur.
- 4. Man wasche die Platte einmal mit PBS und dann zweimal mit
50 mM Hepes-Puffer pH 7,5.
- 5. Man gebe 25 μl
der Testverbindung in 4% DMSO (erhältlich durch Verdünnen einer
Stammlösung
aus 10 mM der Testverbindung in 100 DMSO mit dH2O)
zur Platte.
- 6. Man gebe 10,0 ng der gst-IGF-1-Kinase in 50 μl Kinaseverdünnungspuffer
zu allen Kammern.
- 7. Man starte die Kinasereaktion durch Zugabe von 25 μl 4× ATP-Reaktionsmischung
zu allen Testkammern und den Kammern mit der Positivkontrolle. Man
gebe 25 μl
4× der
Mischung für
die Negativkontrollen zu allen Kammern mit der Negativkontrolle.
Man inkubiere für
10 Minuten unter Schütteln
bei Raumtemperatur.
- 8. Man gebe 25 μl
0,5 M EDTA (pH 8,0) zu allen Kammern.
- 9. Man wasche die Platte 4× mit
TBST-Puffer.
- 10. Man gebe polyklonales Anti-Phosphotyrosinantiserum vom Hasen
mit einer Verdünnung
von 1:10000 in 100 μl
Antikörperverdünnungspuffer
zu allen Kammern. Man inkubiere unter schütteln bei Raumtemperatur für 1 Stunde.
- 11. Man wasche die Platte wie unter Schritt 9.
- 12. Man gebe 100 μl
Biosource Anti-Hasen HRP mit einer Verdünnung von 1:10000 im Antikörperverdünnungspuffer
zu allen Kammern. Man inkubiere unter Schütteln bei Raumtemperatur für 1 Stunde.
- 13. Man wasche die Platte wie unter Schritt 9 und folge mit
einer Waschung mit PBS, um die Blasen und überschüssiges Tween-20 zu verringern.
- 14. Man entwickle durch Zugabe von 100 μl/Kammer ABTS/H2O2 zu jeder Kammer.
- 15. Nach etwa 5 Minuten, liest man auf einem ELISA-Lesegerät mit dem
Testfilter bei 410 nm und dem Referenzfilter bei 630 nm aus.
-
ASSAYS ZUM EINBAUEN VON
BRDU
-
Die
folgenden Assays verwenden Zellen, die verändert worden sind, um einen
ausgewählten
Rezeptor zu exprimieren und dann die Wirkung einer entsprechenden
Verbindung auf die Aktivität
der Liganden-induzierten DNA-Synthese durch Bestimmen des BrdU-Einbaus
in die DNA zu evaluieren.
-
Die
folgenden Materialien, Reagenzien und Verfahren sind allgemeingültig für alle folgenden
Assays zum Einbauen von BrdU. Unterschiede bei den spezifischen
Assays werden angemerkt.
-
Materialien und Reagenzien:
-
- 1. Den passenden Liganden.
- 2. Die passenden veränderten
Zellen.
- 3. BrdU-Markierungsreagenz: 10 mM in PBS (pH 7,4) (Boehringer
Mannheim, Deutschland).
- 4. FixDenat: Fixierungslösung
(gebrauchsfertig) (Boehringer Mannheim, Deutschland).
- 5. Anti-BrdU-POD: Monoklonaler Antikörper der Maus, der mit einer
Peroxidase konjugiert ist (Boehringer Mannheim, Deutschland).
- 6. TMB-Substratlösung:
Tetramethylbenzidin (TMB, Boehringer Mannheim, Deutschland).
- 7. PBS-Waschlösung:
1× PBS,
pH 7,4.
- 8. Albumin vom Rind (BSA), Fraktion-V-Pulver (Sigma Chemical
Co., USA).
-
Allgemeiner Verfahrensablauf:
-
- 1. Die Zellen werden mit 8000 Zellen/Kammer
in 10% CS, 2 mM Gln in DMEM, in einer 96-Kammer/Platte angeimpft.
Die Zellen werden Übernacht
bei 37°C
unter 5% CO2 inkubiert.
- 2. Nach 24 Stunden werden die Zellen mit PBS gewaschen und werden
dann in einem serumfreien Medium (0% CS DMEM mit 0,1% BSA) für 24 Stunden
ausgehungert ("serum
starved").
- 3. Am dritten Tag werden der passende Ligand und die Testverbindung
gleichzeitig zu den Zellen gegeben. Die Kammern mit den Negativkontrolle
erhalten nur serumfreies DMEM mit 0,1% BSA; die Zellen der Positivkontrolle
erhalten den Liganden jedoch nicht die Testverbindungen. Die Testverbindungen
werden in serumfreiem DMEM mit dem Liganden in einer 96-Kammer-Platte hergestellt
und für
7 Testkonzentrationen fortlaufend verdünnt.
- 4. Nach 18 Stunden der Ligandenaktivierung, wird verdünntes BrdU-Markierungsreagenz
(1:100 in DMEM, 0,1% BSA) zugegeben, und die Zellen werden mit BrdU
(Endkonzentration = 10 μM)
für 1,5
Stunden inkubiert.
- 5. Nach der Inkubation mit dem Markierungsreagenz wird das Medium
durch Dekantieren und ausklopfen der umgedrehten Platte auf einem
Papiertuch entfernt. Man gibt FixDenat-Lösung zu (50 μl/Kammer),
und die Platten werden bei Raumtemperatur für 45 Minuten auf einem Plattenschüttler inkubiert.
- 6. Die FixDenat-Lösung
wird durch Dekantieren und Ausklopfen der umgedrehten Platte auf
einem Papiertuch gründlich
entfernt. Milch wird (5% dehydrierte Milch in PBS, 200 μl/Kammer)
als Blockierlösung
zugegeben, und die Platte wird für
30 Minuten bei Raumtemperatur auf einem Plattenschüttler inkubiert.
- 7. Die Blockierlösung
wird durch Dekantieren entfernt und die Kammern werden einmal mit
PBS gewaschen. Man gibt die Anti-BrdU-POD-Lösung (1:200 Verdünnung in
PBS, 1% BSA) zu (50 μl/Kammer),
und die Platte wird für
90 Minuten bei Raumtemperatur auf einem Plattenschüttler inkubiert.
- 8. Das Antikörperkonjugat
wird durch Dekantieren und fünfmaliges
Ausspülen
der Kammern mit PBS entfernt, und die Platte wird durch Umdrehen
und Ausklopfen auf einem Papiertuch getrocknet.
- 9. Die TMB-Substratlösung
wird zugegeben (100 μl/Kammer)
und für
20 Minuten bei Raumtemperatur auf einem Plattenschüttler inkubiert,
bis die Farbentwicklung für
die photometrische Detektion ausreichend ist.
- 10. Das Absorbtionsvermögen
der Proben wird bei 410 nm (im „dualen Wellenlängen"-Modus mit einem Filter,
der bei 490 nm, als Referenzwellenlänge, ausliest) auf einem Dynatech
ELISA-Platten-Lesegerät
gemessen.
-
EGF-induziertes
Assay zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. EGF von der Maus, 201 (Toyobo Co., Ltd.,
Japan).
- 2. 3T3/EGFRc7.
-
EGF-induziertes Her-2
getriebenes Assay zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. EGF von der Maus, 201 (Toyobo Co., Ltd.,
Japan).
- 2. 3T3/EGFr/Her2/EGFr (EGFr mit einer Her-2-Kinasedomäne).
-
EGF-induziertes Her-4
getriebenes Assay zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. EGF von der Maus, 201 (Toyobo Co., Ltd.,
Japan).
- 2. 3T3/EGFr/Her4/EGFr (EGFr mit einer Her-4-Kinasedomäne)
-
PDGF-induziertes Assay
zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. Humanes PDGF B/B (Boehringer Mannheim, Deutschland).
- 2. 3T3/EGFRc7.
-
FGF-induziertes
Assay zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. Humanes FGF2/bFGF (Gibco BRL, USA).
- 2. 3T3c7/EGFr
-
IGF1-induziertes Assay
zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. Humane Rekombinante (G511, Promega Corp.,
USA)
- 2. 3T3/IGF1r.
-
Insulin-induziertes
Assay zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. Insulin, kristallines, Rinder, Zink (13007,
Gibco BRL, USA).
- 2. 3T3/H25.
-
HGF-induziertes Assay
zum Einbau von BrdU
-
Materialien und Reagenzien:
-
- 1. Rekombinantes, humans HGF (Kat. Nr. 249-HG,
R&D-Systems, Inc. USA).
- 2. BxPC-3-Zellen (ATCC CRL-1687).
-
Verfahrensablauf:
-
- 1. Die Zellen werden mit 9000 Zellen/Kammer
in RPMI 10% FBS in einer 96-Kammer-Platte angeimpft. Die Zellen
werden Übernacht
bei 37°C
unter 5% CO2 inkubiert.
- 2. Nach 24 Stunden werden die Zellen mit PBS gewaschen und dann
werden sie in 100 μl
serumfreiem Medium (RPMI mit 0,1% BSA) für 24 Stunden ausgehungert ("serum starved").
- 3. Am 3. Tag werden 25 μl,
die dem Liganden (hergestellt mit 1 μg/ml in RPMI mit 0,1% BSA; HGF-Endkonzentration
liegt bei 200 ng/ml) und die Testverbindungen enthalten, zu den
Zellen zugegeben. Die Kammern mit der Negativkontrolle erhalten
nur 25 μl
serumfreies RPMI mit 0,1% BSA; die Zellen der Positivkontrolle erhalten
den Liganden (HGF), jedoch keine Testverbindung. Die Testverbindungen
werden mit 5-mal ihrer Endkonzentration in serumfreiem RPMI mit
den Liganden in einer 96-Kammer-Platte hergestellt und fortlaufend
verdünnt,
um 7 Testkonzentrationen zu erhalten. Üblicherweise liegt die höchste Endkonzentration der
Testverbindung bei 100 μM,
und es werden 1:3 Verdünnungen
verwendet (d.h. Endkonzentrationsbereich der Testverbindung liegt
bei 0,137–100 μM).
- 4. Nach 18 Stunden der Ligandenaktivierung werden 12,5 μl des verdünnten BrdU-Markierungsreagenzes (1:100
in RPMI, 0,1% BSA) zu jeder Kammer gegeben, und die Zellen werden
mit BrdU (Endkonzentration ist 10 μM) für 1 Stunde inkubiert.
- 5. Genauso wie beim allgemeinen Verfahren.
- 6. Genauso wie beim allgemeinen Verfahren.
- 7. Die Blockierlösung
wird durch Dekantieren entfernt und die Kammern werden einmal PBS
gewaschen. Die Anti-BrdU-POD-Lösung
(1:100 Verdünnung
in PBS, 1% BSA) wird zugegeben (100 μl/Kammer), und die Platte wird
für 90
Minuten bei Raumtemperatur auf einen Plattenschüttler inkubiert.
- 8. Genauso wie beim allgemeinen Verfahren.
- 9. Genauso wie beim allgemeinen Verfahren.
- 10. Genauso wie beim allgemeinen Verfahren.
-
HUV-EC-C-Assay
-
Dieses
Assay wird verwendet, um die Aktivität einer Verbindung gegenüber PDGF-R,
FGF-R, VEGF, aFGF oder Flk-1/KDR,
wobei alle natürlicherweise
von HUV-EC-Zellen exprimiert werden, zu messen.
-
TAG 0
-
- 1. Man wasche und trypsiniere die HUV-EC-C-Zellen
humane Nabelschnurvenenendothelzellen, American Type Culture Collection,
Katalog Nr. 1730 CRL). Man wasche sie mit Dulbecco's phosphatgepufferter
Salzlösung
(D-PBS, erhältlich
bei Gibco BRL, Katalog Nr. 14190-029) 2 mal bei etwa 1 ml/10 cm2 der Gewebekulturschale. Trypsiniere sie
mit 0,05% Trypsin-EDTA in einer nichtenzymatischen Zelldissoziationslösung (Sigma
Chemical Company, Katalog Nr. C-1544). Das 0,05% Trypsin wird durch
Verdünnen
von 0,25% Trypsin/1 mM EDTA (Gibco, Katalog Nr. 25200-049) in der
Zelldissoziationslösung
hergestellt. Trypsinisiere mit etwa 1 ml/25–30 cm2 der
Gewebekulturschale für
etwa 5 Minuten bei 37°C.
Nachdem sich die Zellen von der Schale abgelöst haben, gebe man das gleiche
Volumen an Assay-Medium hinzu und übertrage sie in ein 50 ml steriles
Zentrifugenröhrchen
(Fisher Scientific, Katalog Nr. 05-539-6).
- 2. Man wasche die Zellen mit etwa 35 ml Assaymedium in einem
50 ml sterilen Zentrifugenröhrchen
durch Zugabe des Assaymediums, man zentrifugiere für 10 Minuten
bei etwa 200 × g,
man verwerfe den Überstand
und resuspendiere mit 35 ml D-PBS. Man wiederhole die Waschung zweimal
mit D-PBS und resuspendiere die Zellen in etwa 1 ml Assaymedium/15
cm2 der Gewebekulturschale. Das Assaymedium
besteht aus F12K-Medium (Gibco BRL, Katalog Nr. 21127-014) und 0,5%
hitzeinaktiviertes fötales
Rinderserum. Man zähle
die Zellen mit einem Coulter Counter® (Coulter
Electronics, Inc.) und gebe das Assaymedium zu den Zellen, um eine
Konzentration von 0,8–1,0 × 105 Zellen/ml zu erhalten.
- 3. Man gebe Zellen zu den 96-Kammer flachbödigen Platten bei 100 μl/Kammer
oder 0,8–1,0 × 104 Zellen/Kammer und inkubiere ~24 h bei 37°C, 5% CO2.
-
TAG 1
-
- 1. Man stelle zweifach Testverbindungstitrationen
in separaten 96-Kammer-Platten her, im allgemeinen von 50 μM herunter
bis auf 0 μM.
Man verwende das gleiche Assaymedium wie am Tag 0, Schritt 2 weiter
oben, erwähnt.
Die Titrationen werden durch Zugabe von 90 μl/Kammer der Testverbindung
bei 200 μM
(4× der Kammer
Endkonzentration) zur oberen Kammer einer bestimmten Plattenspalte
durchgeführt.
Da die Stamm-Testverbindung
im Allgemeinen bei 20 mM in DMSO vorliegt, enthalten die 200 μM Arzneimittelkonzentration
2% DMSO.
Ein Verdünnungsmittel,
hergestellt aus 2% DMSO im Assaymedium (F12K + 0,5% fötales Rinderserum) wird
als Verdünnungsmittel
für die
Testverbindungstitrationen verwendet, um die Testverbindung zu verdünnen, die
DMSO-Konzentration
jedoch konstant zu halten. Man gebe dieses Verdünnungsmittel mit 60 μl/Kammer
zu den verbleibenden Kammern in der Spalte. Man entnehme 60 μl aus den
120 μl der
200 μM Testverbindungsverdünnung in
der oberen Kammer der Spalte und mische sie mit den 60 μl in der
zweiten Kammer der Spalte. Man entnehme 60 μl aus dieser Kammer und mische
sie mit den 60 μl
in der dritten Kammer der Spalte usw., bis die zweifach Titrationen
vollständig
sind. Wenn die vorletzte Kammer zusammengemischt wird, nimmt man
60 μl aus
den 120 μl
in dieser Kammer und verwirft sie. Man behält die letzte Kammer mit 60 μl der DMSO/Mediumverdünnung als
eine die Testverbindung nicht enthaltende Kontrolle bei. Man erstelle
9 Spalten mit titrierter Testverbindung, genügend für dreimal so viele Kammern,
jede für: (1)
VEGF (erhalten bei Pepro Tech Inc.), Katalog Nr. 100–200, (2)
den endothelen Zellwachstumsfaktor (ECGF) (auch bekannt als saurer
Fibroblastenwachstumsfaktor oder aFGF) (erhalten bei Boehringer Mannheim
Biochemica, Katalog Nr. 1439 600), oder (3) humanes PDGF B/B (1276-956,
Boehringer Mannheim, Deutschland) und eine Assaymediumkontrolle.
ECGF kommt als Zubereitung mit Natriumheparin.
- 2. Man gebe 50 μl/Kammer
der Testverbindungsverdünnungen
zu den 96-Kammer-Assayplatten, die 0,8–1,0 × 109 Zellen/100 μl/Kammer
der HUV-EC-C-Zellen vom Tag 0 enthalten und inkubiere sie ~2 h bei 37°C, 5% CO2.
- 3. Man gebe 50 μl/Kammer
an 80 μg/ml
VEGF, 20 ng/ml ECGF oder Mediumkontrolle dreifach zu jeder Testverbindungskondition.
Wie bei den Testverbindungen entsprechen die Wachstumsfaktorkonzentrationen
4× der
gewünschten
Endkonzentration. Man verwende das Assaymedium vom Tag 0, Schritt
2, um die Konzentrationen für
die Wachstumsfaktoren zu erstellen. Man inkubiere für etwa 24
Stunden bei 37°C,
5% CO2. Jede Kammer wird 50 μl der Testverbindungsverdünnung, 50 μl des Wachstumsfaktors
oder des Mediums und 100 μl
Zellen enthalten, was insgesamt 200 μl/Kammer ergibt. Demnach werden
die 4× Konzentrationen
der Testverbindungen und der Wachstumsfaktoren zu 1×, sobald
einmal alles zu den Kammern zugegeben worden ist.
-
TAG 2
-
- 1. Man gebe 3H-Thymidin
(Amersham, Katalog Nr. TRK-686)
bei 1 μCi/Kammer
(10 μl/Kammer
an 100 μCi/ml
Lösung,
hergestellt in RPMI-Medium + 10% hitzeinaktiviertes fötales Rinderserum)
hinzu und inkubiere ~24 h bei 37°C,
5% CO2. RPMI wird bei Gibco BRL, Katalog
Nr. 11875-051 erhalten.
-
TAG 3
-
- 1. Man friere die Platten Übernacht bei –20°C ein.
-
TAG 4
-
Man
taue die Platten auf und ernte mit einem 96-Kammer Plattenerntegerät (Tomtec
Harvester 96®) auf
Filtermatten (Wallac, Katalog Nr. 1205-401) ab, man lese die Treffer
auf einem Wallac BetaplateTM-Liquid-Scintillationszähler aus.
-
Bioassays,
die verwendet worden sind oder verwendet werden können, um
die Verbindungen zu evaluieren, werden im Detail weiter unten beschrieben.
Die Verbindungen 1–9
wurden getestet und waren in den flkGST-, FGFR1- und PDGF-Assays
aktiv.
-
IN VIVO TIERMODELLE
-
XENOTRANSPLANTAT TIERMODELLE
-
Die
Fähigkeit
humaner Tumoren als Xenotransplantate in athymischen Mäusen (z.B.,
Balb/c, nu/nu) zu wachsen, stellt ein nützliches in vivo Modell zum
Studieren der biologischen Reaktion auf Therapien für humane
Tumoren dar. Seit der ersten erfolgreichen Xenotransplantation humaner
Tumoren in athymischen Mäusen
(Rygaard und Povlsen, 1969, Acta Pathol. Microbial. Scand. 77: 758–760) sind
viele verschiedene humane Tumorzelllinien (z.B., Brust, Lungen,
urogenital-, gastrointestinal-, Kopf- und Hals-, Glioblastom, Knochen
und maligne Melanome) transplantiert worden und wuchsen erfolgreich
in Nacktmäusen.
Die folgenden Assays können
verwendet werden, um das Aktivitätsniveau,
die Spezifität
und die Wirkung der verschiedenen Verbindungen der vorliegenden
Erfindung zu bestimmen. Drei allgemeine Assaytypen sind für die Evaluierung
der Verbindungen verwendbar: zellulär/katalytisch, zellulär/biologisch
und in vivo. Das Ziel der zellulären/katalytischen
Assays ist es, die Wirkung einer Verbindung auf die Fähigkeit
einer TK Tyrosin an einem bekannten Substrat in einer Zelle zu phosphorylieren,
zu bestimmen. Das Ziel der zellulären/biologischen-Assays ist
es, die Wirkung einer Verbindung auf die biologische Reaktion, die
durch eine TK in einer Zelle stimuliert wird, zu bestimmen. Das
Ziel der in vivo-Assays ist es, die Wirkung einer Verbindung in
einem Tiermodell einer bestimmten Störung, wie zum Beispiel Krebs,
zu bestimmen.
-
Geeignete
Zelllinien für
subkutane Xenotransplantatexperimente schließen C6-Zellen (Gliom, ATCC
# CCL 107), A375-Zellen (Melanom, ATCC # CRL 1619), A431-Zellen (Plattenepithelkarzinom,
ATCC # CRL 1555), Calu-6-Zellen
(Lunge, ATCC # HTB 56), PC3-Zellen (Prostata, ATCC # CRL 1435),
SKOV3TP5-Zellen und NIH 3T3-Fibroblasten, die genetisch verändert wurden,
um EGFR, PDGFR, IGF-1R oder jede andere Testkinase überzuexprimieren,
ein. Das folgende Protokoll kann verwendet werden, um Xenotransplantatexperimente
durchzuführen.
-
Weibliche
athymische Mäuse
(BALB/c, nu/nu) werden bei den Simonsen Laboratories (Gilroy, CA)
erhalten. Alle Tiere werden unter Reinraumbedingungen in Mikroisolatorkäfigen mit
Alpha-dri-Ausbettung gehalten. Sie erhalten steriles Nagetierfutter
und Wasser ad libitum.
-
Die
Zelllinien werden in geeignetem Medium (zum Beispiel, MEM, DMEM,
Ham's F10 oder Ham's F12 plus 5%–10% fötalem Rinderserum
(FBS) und 2 mM Glutamin (GLN)) herangezogen. Alle Zellkulturmedien, Glutamin
und fötales
Rinderserum werden bei Gibco Life Technologies (Grand Island, NY)
bezogen, soweit nichts anderes angegeben wird. Alle Zellen werden
in einer feuchten Atmosphäre
von 90–95%
Luft und 5–10% CO2 bei 37°C
herangezogen. Alle Zelllinien werden routinemäßig zweimal pro Woche subkultiviert
und sind Mycoplasma negativ, was durch das Mycotect-Verfahren (Gibco)
bestätigt
wird.
-
Die
Zellen werden bei oder bei fast Konfluenz mit 0,05 Trypsin-EDTA
abgeerntet und bei 450 × g
für 10
min pelletiert. Die Pellets werden in sterilem PBS oder Medium (ohne
FBS) bis auf eine bestimmte Konzentration resuspendiert und die
Zellen werden dann in die Hinterflanke der Mäuse (8–10 Mäuse pro Gruppe, 2–10 × 106 Zellen/Tier) implantiert. Das Tumorwachstum
wird über
3 bis 6 Wochen mittels eines Tastzirkels gemessen. Die Tumorvolumen
werden als Produkt der Länge × Breite × Höhe berechnet,
soweit nichts anderes angegeben wird. Die P-Werte werden mittels
des Students t-Test
berechnet. Die Testverbindungen in 50–100 μl Hilfsstoff (DMSO oder VPD:D5W)
können
durch IP Injektion in unterschiedlichen Konzentrationen, allgemein am
ersten Tag nach der Implantation startend, verabreicht werden.
-
TUMORINVASIONSMODELL
-
Das
folgende Tumorinvasionsmodell ist entwickelt worden und kann für die Evaluierung
des therapeutischen Werts und der Wirksamkeit der Verbindungen,
die als den KDR/FLK-1-Rezeptor
selektiv inhibierend identifiziert worden sind, verwendet werden.
-
Verfahrensablauf
-
8
Wochen alte Nacktmäuse
(weiblich) (Simonsen Inc.) werden als Versuchstiere verwendet. Die
Implantation der Tumorzellen kann in einem laminaren Flow-Hood durchgeführt werden.
Für die
Anästhesie
wird ein Xylazin/Ketamin-Cocktail (100 mg/kg Ketamin und 5 mg/kg
Xylazin) intraperitoneal verabreicht. Ein Medianschnitt wird durchgeführt, um
die abdominale Höhlung
(etwa 1,5 cm in der Länge)
freizulegen, um 107 Tumorzellen in einem
Volumen von 100 μl
Medium zu injizieren. Die Zellen werden entweder in den duodenalen Lappen
des Pankreas oder unter die Serosa des Dickdarms injiziert. Das
Peritoneum und die Muskeln werden mit einer 6-0 fortlaufenden Seitennaht verschlossen
und die Haut wird mittels einer Wundklammer verschlossen. Die Tiere
werden täglich
beobachtet.
-
Analyse
-
Nach
2–6 Wochen,
abhängig
von den allgemeinen Beobachtungen der Tiere, werden die Mäuse getötet und
die lokalen Tumormetastasen verschiedener Organe (Lunge, Lebe, Gehirn,
Magen, Milz, Herz, Muskel) werden entnommen und analysiert (Messung
der Tumorgröße, Invasionsgrad,
Immunochemie, in situ Hybridisationsbestimmung, etc.).
-
C-KIT ASSAY
-
Dieses
Assay wird verwendet, um das Niveau der C-Kit-Tyrosin-Phosphorylierung zu detektieren.
-
MO7E
(humane akute granulozitäre
Leukämie)-Zellen
werden Übernacht
in 0,1% Serum ausgehungert. Die Zellen werden mit der Verbindung
vor der Ligandenstimulation vorbehandelt (gleichzeitig zum Aushungern
("serum starved")). Die Zellen werden
mit 250 ng/ml rh-SCF für
15 Minuten stimuliert. Nach der Stimulation werden die Zellen lysiert
und mit einem Anti-C-Kit-Antikörper immunopräzipitiert.
Phosphotyrosin- und Proteinniveaus werden durch Western-Blot bestimmt.
-
MTT PROLIFERATIONSASSAY
-
MO7E-Zellen
werden ausgehungert ("serum
starved") und mit
einer Verbindung, wie sie bei den Phosphorylierungsexperimenten
beschrieben wurde, vorbehandelt. Die Zellen werden mit 4 × 105 Zellen/Kammer in einer 96-Kammer-Kulturschale
in 100 μl
RPMI + 10% Serum ausplattiert. Man gibt rh-SCF (100 ng/ml) zu und
die Platte wird für
48 Stunden inkubiert. Nach 48 Stunden werden 10 μl an 5 mg/ml MTT [3-(4,5-Dimethylthiazol-2-yl)-2,5-Diphenyltetrazoliumbromid)
zugegeben und man lässt
sie für
4 Stunden inkubieren. Saures Isopropanol (100 μl an 0,04 N HCl in Isopropanol)
wird hinzugegeben und die optische Dichte wird bei einer Wellenlänge von
550 nm gemessen.
-
APOPTOSEASSAY
-
MO7E-Zellen
werden +/–SCF
und +/–Verbindung
in 10% FBS mit rh-GM-CSF (10 ng/ml) und rh-IL-3 (10 ng/ml) inkubiert.
Die Proben werden nach 24 und 48 Stunden untersucht. Um die aktivierte
Caspase-3 zu messen, werden die Proben mit PBS gewaschen und mit
eiskaltem 70% Ethanol permeabilisiert. Die Zellen werden dann mit
PE-konjugiertem, polyklonalem anti-aktivem Caspase-3 vom Hasen gefärbt und
durch FACS analysiert. Um abgespaltenes PARP zu messen, werden die
Proben lysiert und durch Western-Blot mit einem Anti-PARP-Antikörper analysiert.
-
Zusätzliche Assays
-
Zusätzliche
Assays, die verwendet werden können,
um die Verbindungen dieser Erfindung zu evaluieren, schließen, ohne
Begrenzung, ein bio-flk-1-Assay, ein EGF-Rezeptor-HER2-chimeräres Rezeptorassay in
ganzen Zellen, ein bio-src-Assay, ein bio-lck-Assay und ein Assay,
das wie Phosphorylierungsfunktion von raf mißt, ein. Die Protokolle für jedes
dieser Assays können
in der U.S. Anmeldung mit der Ser. Nr. 09/099,842, die hierin, einschließlich aller
Zeichnungen, aufgenommen wird, gefunden werden.
-
Messung der
Zelltoxizität
-
Therapeutische
Verbindungen sollten beim Inhibieren der Rezeptor-Tyrosinkinaseaktivität potenter sein,
als beim Ausüben
einer cytotoxischen Wirkung. Eine Messung der Wirksamkeit und der
Zelltoxizität
einer Verbindung kann durch Bestimmen des therapeutischen Indexs,
d.h., IC50/LD50,
erhalten werden. IC50, die Dosis, die erforderlich
ist, um eine 50% Inhibition zu erzielen, kann mit Standardtechniken,
zum Beispiel den hierin beschrieben, gemessen werden. LD50, die Dosis, die zu einer 50% Toxizität führt, kann
ebenfalls durch Standardtechniken als auch (Mossman, 1983, J. Immunol.
Methods, 65: 55–63)
durch Messen der Menge an freigesetzter LDH (Korzeniewski und Callewaert,
1983, J. Immunol. Methods, 64: 313, Decker und Lohmann-Matthes,
1988, J. Immunol. Methods, 115: 61) oder durch Messen der letalen
Dosis in Tiermodellen gemessen werden. Verbindungen mit einem hohen
therapeutischen Index werden bevorzugt. Der therapeutische Index
sollte größer sein
als 2, bevorzugt wenigstens 10, am meisten bevorzugt wenigstens
50.