-
Hintergrund
der Erfindung
-
Die vorliegende Erfindung betrifft
ein Verfahren zum Messen von Cholesterin in Lipoproteinen geringer Dichte
(nachfolgend bezeichnet als „LDL"), die in Lebendkörperproben
vorhanden sind, wie beispielsweise Serum, Plasma, usw.
-
Die Hauptbestandteile von Lipiden
im Serum sind Cholesterin, Triglyceride, Phospholipide, usw. Diese Serumlipide
binden an Apoproteinen unter Erzeugung von Lipoproteinen, die im
Blut zirkulieren. Die Lipoproteine lassen sich nach den Unterschieden
in der Dichte einteilen in Lipoproteine hoher Dichte (HDL), Lipoproteine
geringer Dichte (LDL), Lipoproteine sehr hoher Dichte (VLDL) und
Chylomikrone (CM), usw. Unter diesen Lipoproteinen hat HDL die Funktion
des Transports von überschüssigem Cholesterin,
das sich auf Geweben ablagert, zur Leber zu transportieren und hat
eine antiasteriosklerotische Wirkung. Andererseits ist LDL eine Hauptträgersubstanz
von Cholesterin aus der Leber zum jeweiligen Gewebe. Eine Erhöhung an
LDL scheint in engem Zusammenhang mit der Entstehung von Arteriosklerose
zu stehen.
-
Das Cholesterin im LDL (nachfolgend
bezeichnet als „LDL-Cholesterin") wird daher im Zusammenhang
mit einem Risikofaktor für
Arteriosklerose und ischämischer
Herzerkrankungen (arteriosklerotische Gefäßerkrankung) gebracht. Daher
ist der Gehalt an LDL-Cholesterin ein wichtiger Hinweis für die Diagnose,
Therapie und Prophylaxe dieser Erkrankungen.
-
Als Methoden zur Messung von LDL-Cholesterin
sind eine Fällungsmethode,
eine Ultrazentrifugenmethode, eine Elektrophoresemethode und die
Methode nach Friedewald bekannt gewesen. Unter diesen Methoden haben
die Fällungsmethode,
die Ultrazentrifugenmethode und die Elektrophoresemethode komplizierte
Prozeduren, was auf Vorbehandlungsschritte zurückzuführen ist, wie beispielsweise
die Trennung des LDL von nicht benötigten anderen Lipoproteinen
als LDL durch Ausfällungs-/oder
Zentrifugenbehandlungen, Ultrazentrifugenbehandlung oder Elektrophoresebehandlung.
Das Problem bei diesen Methoden besteht darin, dass eine direkte
Messung unter ausschließlicher
Anwendung eines Autoanalyzers, der auf dem Gebiet der klinischen
Tests breite Anwendung findet, nicht möglich ist.
-
Andererseits besteht bei der Friedewald-Methode,
die durch die Friedewald-Gleichung bekannt ist und worin der Gesamtwert
des Cholesterins, ein HDL-Cholesterinwert und ein Triglyceridwert
für die
Berechnung verwendet werden, ein Problem darin, dass es unmöglich ist,
eine genaue LDL-Cholesterin- Menge
im Fall der Verwendung einer Probe mit einem Gehalt von 500 mg/dl
oder darüber
an Triglyceriden zu messen.
-
Um die vorgenannten Probleme zu lösen, sind
zahlreiche Methoden entwickelt worden. Beispielsweise wird in der
JP-A-7-280812 eine Methode offenbart, die das Koagulieren von LDL
unter Verwendung einer Koagulans und/oder eines Antikörpers umfasst,
das Eliminieren (Verbrauchen) von Cholesterin, das in anderen Lipoproteinen
als LDL enthalten ist, indem es in ein anderes Reaktionssystem eingeführt wird,
das nicht zu der quantitativen Reaktion gehört; Auflösen des koagulierten LDL bis
zu einem Grad, indem man in der Lage ist, die quantitative Reaktion
unter Verwendung eines Tensids und/oder anorganischen Salzes auszuführen; und
Messen der Absorption der Lösung,
indem man das LDL-Cholesterin
der quantitativen Reaktion unterzieht.
-
Da bei dieser Methode jedoch ein
System mit drei Reagenzien oder ein System mit vier Reagenzien bei
der Messung eingesetzt wird, wenn sie auf nur wenige Autoanalyzer
angewendet werden, bei denen derartige Mehrfachreagenziensysteme
verwendet werden können.
Viele Autoanalyzer, die üblicherweise
bei klinischen Tests verwendet werden, können nicht zur Anwendung kommen,
da diese Autoanalyzer lediglich mit einer Zweireagenzienmethode
verwendet werden können.
Außerdem
besteht bei dieser Methode ein Problem darin, dass aufgrund der
Verwendung einer Reihe von Reagenzien die Reproduzierbarkeit der
gemessenen Werte herabgesetzt ist.
-
Um LDL-Cholesterin ohne komplizierte
Vorbehandlungen zu messen, gibt es ein Verfahren, das in der JP-A-58-165800
offenbart wurde. Nach diesem Verfahren wird jedoch die Herstellung
von Reagenzien kompliziert, da die anwendbaren Konzentrationen eines
Tensids und einer Cholesterinesterase z. B. in den Reagenzien beschränkt ist.
Darüber
hinaus lassen sich die Messbedingungen, wie beispielsweise der pH-Wert zum
Zeitpunkt der Messung, die Intervalle der Messzeiten, usw. schwer
einstellen. Darüber
hinaus kann das LDL-Cholesterin,
da das Cholesterin in dem HDL in gewissem Umfang reagiert, lediglich
mit Hilfe einer kinetischen Messung gemessen werden, d. h. mit einem
Geschwindigkeitsassay. So lässt
sich von einem derartigen Prozess nicht gerade sagen, dass es ein
praktisches Messverfahren ist.
-
Die WO 96/29599 und EP-A-0 764 848
offenbaren eine Methode zum Quantifizieren der Cholesterin-Menge
in LDL, die das enzymatische Bestimmen (unter Verwendung von Cholesterinesterase
und Cholesterinoxidase/Dehydrogenase) der Cholesterin-Menge in einer
Probe in Gegenwart einer Zuckerverbindung und/oder eines nicht ionischen
oder anionischen Tensids als Protein solubilisierendes Mittel umfasst.
Das Verfahren ist hinsichtlich der Genauigkeit jedoch unzureichend.
-
Die EP-A-0 698 791 offenbart eine
Methode zum Bestimmen der Cholesterin-Menge in dem jeweiligen LDL,
VLDL und CM in einer Probe unter Anwendung der in der EP-A-0 764
848 beschriebenen Methode und der Berechnung der Differenz zwischen
dem vorgenannten Gehalt und dem Gesamtgehalt an Cholesterin in der
Probe.
-
Die EP-A-0 763 741 offenbart eine
Methode zum Bestimmen der Cholesterin-Menge in LDL in einer Probe,
die das Eliminieren von Cholesterin in HDL in der Probe umfasst
und das enzymatische Messen der Menge von LDL-Cholesterin in Gegenwart von Cyclodextrin
und einem nicht ionischen oder kationischen Tensid.
-
Die EP-A-0 402 094 offenbart eine
Methode zum quantitativen Bestimmen der Menge des Gesamtcholesterins
in Körperflüssigkeiten,
in denen die enzymatische Reaktion in Gegenwart von einem oder mehreren kationischen
und/oder amphoteren Tensiden ausgeführt wird.
-
Zusammenfassung
der Erfindung
-
Es ist eine Aufgabe der vorliegenden
Erfindung, ein Verfahren zum Messen von LDL-Cholesterin in einer
Lebendkörperprobe
zu gewähren,
indem ein Autoanalyzer oder dergleichen direkt ohne komplizierte
Vorbehandlungen für
das Abtrennen von LDL von nicht erforderlichen anderen Lipoproteinen
als LDL (was in den vorstehend genannten bekannten Verfahren erforderlich
ist) verwendet wird sowie Reagenzien, die bei einem solchen Prozess
angewendet werden.
-
Die vorliegende Erfindung gewährt ein
Verfahren zum Messen von Cholesterin in Lipoproteinen geringer Dichte,
die in einer Lebendkörperprobe
vorliegen, indem ein Reaktionsprodukt der Probe mit einem Reagens
optisch gemessen wird und die Ausführung der Reaktion der Probe
mit Cholesterinoxidase oder Cholesterindehydrogenase in Gegenwart
eines Amphotensids und mindestens eines Vertreters umfasst, ausgewählt aus
der Gruppe, bestehend aus Cyclodextrin und Derivaten davon.
-
Nach einer der Ausführungsformen
der vorliegenden Erfindung umfasst das Verfahren:
Behandeln
der Probe mit einem ersten Reagens, das mindestens einen Vertreter
aufweist, ausgewählt
aus der Gruppe, bestehend aus Cyclodextrin und Derivaten davon;
Messen
eines Absorptionsgrades oder Transmissionsgrades der resultierenden
Lösung;
Behandeln
der resultierenden Lösung
mit einer zweiten Reagenslösung,
die Cholesterinoxydase enthält;
Messen
eines anderen Absorptionsgrades oder Transmissionsgrades der resultierenden
abschließenden
Lösung;
sowie
Ermitteln der Cholesterin-Menge in der Probe auf der
Grundlage der vorstehend gemessenen Daten des Absorptionsgrades
oder Transmissionsgrades;
worin in mindestens entweder dem
ersten Reagens oder dem zweiten Reagens ein Kuppler, ein Entwickler, Peroxidase,
ein Amphotensid und Cholesterinesterase enthalten sind.
-
Die vorliegende Erfindung gewährt ferner
Reagenzien, die bei den vorgenannten Verfahren verwendet werden
können.
-
Beschreibung
der bevorzugten Ausführungsformen
-
Für
die Messung der Cholesterin-Menge in Lipoproteinen geringer Dichte
in einer Lebendkörperprobe, wie
beispielsweise Serum und Plasma, ohne eine Vorbehandlung zum Abtrennen
des LDL-Cholesterins von nicht erforderlichen anderen Lipoproteinen
als LDL haben die Erfinder der vorliegenden Patentanmeldung entdeckt,
dass, wenn LDL-Cholesterin in der Probe in Gegenwart eines Amphotensids
und Cyclodextrin und/oder eines Derivats davon gemessen wird, die
Cholesterin-Menge in LDL präzise
und direkt unter Verwendung eines Autoanalyzers ohne bekannte komplizierte
Vorbehandlungen erhalten wird.
-
Nach der vorliegenden Erfindung kann
LDL-Cholesterin in einer Lebendkörperprobe
präzise
in Gegenwart eines Amphotensids und Cyclodextrin und/oder eines
Derivats davon unter Anwendung beispielsweise eines Autoanalyzers
gemessen werden.
-
Das Verfahren zum Messen der Menge
von LDL-Cholesterin in einer Lebendkörperprobe nach der vorliegenden
Erfindung umfasst:
Ausführen
der Reaktion der Probe mit Cholesterinoxidase oder Cholesterindehydrogenase
in Gegenwart eines Amphotensids und mindestens eines Vertreters,
ausgewählt
aus der Gruppe, bestehend aus Cyclodextrin und Derivaten davon,
und
optisches Messen der Cholesterin-Menge, z. B. durch konventionelles
Messen von optischen Änderungen.
-
Nach einer der Ausführungsformen
der vorliegenden Erfindung umfasst das Verfahren:
Behandeln
der Lebendkörperprobe
mit einem ersten Reagens, das mindestens einen Vertreter aufweist,
ausgewählt
aus der Gruppe, bestehend aus Cyclodextrin und Derivaten davon;
Messen
einer optischen Änderung,
wie beispielsweise des Absorptionsgrades oder Transmissionsgrades
der resultierenden Lösung;
Behandeln
der resultierenden Lösung
mit einer zweiten Reagenslösung,
die Cholesterinoxidase (nachfolgend bezeichnet als „COD") enthält;
Messen
einer anderen optischen Änderung,
wie beispielsweise eines Absorptionsgrades oder Transmissionsgrades,
der resultierenden abschließenden
Lösung;
sowie
Ermitteln der Cholesterin-Menge in der Probe auf der
Grundlage der vorstehend gemessenen Daten der optischen Änderungen;
worin
in mindestens entweder dem ersten Reagens oder dem zweiten Reagens
ein Kuppler, ein Entwickler, Peroxidase, ein Amphotensid und Cholesterinesterase
enthalten sind.
-
Nach einer weiteren Ausführungsform
der vorliegenden Erfindung umfasst das Verfahren:
Behandeln
der Probe mit einem ersten Reagens, das mindestens einen Vertreter
aufweist, ausgewählt
aus der Gruppe, bestehend aus Cyclodextrin und Derivaten davon;
Messen
einer optischen Änderung,
wie beispielsweise einem Absorptionsgrad, Transmissionsgrad, usw.,
der resultierenden Lösung;
Behandeln
der resultierenden Lösung
mit einer zweiten Reagenslösung,
die Cholesterindehydrogenase enthält (nachfolgend bezeichnet
als „CHD");
Messen einer
anderen optischen Änderung,
wie beispielsweise Absorptionsgrad, Transmissionsgrad, usw., der
resultierenden abschließenden
Lösung;
und
Ermitteln der Cholesterin-Menge in der Probe auf der Grundlage
der vorstehend gemessenen Daten der optischen Änderungen;
worin in mindestens
entweder dem ersten Reagens oder dem zweiten Reagens Nicotinamid-Adenin-Dinukleotid
(Phosphat), ein Amphotensid und Cholesterinesterase enthalten sind.
-
Eine Reagens-Zusammensetzung zum
Messen von LDL-Cholesterin der vorliegenden Erfindung weist Cholesterinoxidase
oder Cholesterindehydrogenase, ein Amphotensid und Cyclodextrin
und/oder ein Derivat davon auf.
-
Nach einer der Ausführungsformen
der Reagens-Zusammensetzung der vorliegenden Erfindung weist die
Reagens-Zusammensetzung auf:
- (a) ein erstes
Reagens, das mindestens einen Vertreter enthält, ausgewählt aus der Gruppe, bestehend
aus Cyclodextrin und Derivaten davon;
- (b) ein zweites Reagens, das COD enthält, und
- (c) einen Kuppler, einen Entwickler, Peroxidase (nachfolgend
bezeichnet als „POD"), ein Amphotensid
und Cholesterinesterase (nachfolgend bezeichnet als „CHE"), die mindestens
entweder in dem ersten Reagens oder dem zweiten Reagens enthalten
sind.
-
Nach einer weiteren Ausführungsform
der Reagens-Zusammensetzung der vorliegenden Erfindung weist die
Reagens-Zusammensetzung auf:
- (a) ein erstes
Reagens, das Cyclodextrin und/oder ein Derivat davon, ein Amphotensid
und CHE enthält;
- (b) ein zweites Reagens, das COD und CHE enthält; und
- (c) einen Kuppler, einen Entwickler und POD, die mindestens
entweder in dem ersten Reagens oder dem zweiten Reagens enthalten
sind.
-
Die Reagenzien der vorliegenden Erfindung
können
in Form einer diagnostischen Ausrüstung verwendet werden, aufweisend:
einen
ersten Behälter,
der ein erstes, Cyclodextrin und/oder ein Derivat davon aufweisendes
Reagens enthält, ein
Amphotensid, CHE und einen Kuppler (oder Entwickler); und
einen
zweiten Behälter,
der ein zweites, COD, CHE, POD und einen Entwickler (oder eine Kuppler)
aufweisendes Reagens enthält.
-
Als das Amphotensid können alle
beliebigen so lange verwendet werden, wie sie verhindern, dass das in
anderen Lipoproteinen als dem LDL enthaltene Cholesterin an der
Reaktion der Cholesterinmessung in gleichzeitiger Gegenwart von
Cyclodextrin und/oder Derivaten davon teilnimmt. Beispiele für das Amphotensid sind
Betain-Derivate, z. B. Alkylbetaine, wie beispielsweise: Laurylbetain,
Stearylbetain, Lauryldimethylammoniumbetain, Kokosnuss-Betain, Kokosnussöl-Fettsäureamidopropylbetain
und Laurinsäureamidopropylbetain; Imidazoliniumbetain-Derivate,
wie beispielsweise Laurylcarboxymethylhydroxyethylimidazoliniumbetain,
2-Alkyl-N-carboxymethyl-N-hydroxyethylimidazoliniumbetaine, 2-Alkyl-N-carboxyethyl-N-hydroxyethylimidazoliniumbetain
und 2-Undecyl-N-carboxymethyl-N-hydroxyethylimidazoliniumbetain;
Sulfobetain-Derivate, wie beispielsweise N-Octyl-N,N-dimethyl-3-ammonio-1-propansulfonsäure, N-Decyl-N,N-dimethyl-3-ammonio-1-propansulfonsäure, N-Dodecyl-N,N-dimethyl-3-ammonio-1-propansulfonsäure, N-Tetradecyl-N,N-dimethyl-3-ammonio-1-propansulfonsäure und
N-Hexadecyl-N,N-dimethyl-3-ammonio-1-propan-sulfonsäure; Aminocarbonsäure-Derivate,
wie beispielsweise Alkylglycine, Alkyldi(aminoethyl)glycine, Dioctylpolyaminoethylglycin,
N-Alkylpolyaminoethylglycine und β-Alanin-Derivate;
Imidazolin-Derivate, wie beispielsweise Bis-(2-undecyl-N-hydroxyethylimidazolin)chloressigsäure-Komplex
und Alkylimidazolin-Derivate; Aminoxid-Derivate, wie beispielsweise
Lauryldimethylaminoxid. Diese Amphotenside können allein oder als Mischung
davon verwendet werden. Diese Amphotenside können solche sein, die kommerziell
verfügbar
sind, und solche, die nach konventionellen Methoden synthetisch
dargestellt werden.
-
Die Konzentration der Anwendung dieser
Amphotenside im Fall der gleichzeitigen Anwesenheit von Cyclodextrin
ist so lange nicht speziell beschränkt, wie das Amphotensid verhindern
kann, dass das in anderen Lipoproteinen als LDL enthaltene Cholesterin
an der Reaktion der Cholesterinmessung teilnimmt. Die bevorzugte
Konzentration des Amphotensids in der abschließenden Lösung (Reaktionslösung) zum
Zeitpunkt der Cholesterinmessung beträgt 0,0001 bis 10% (Gewicht/Volumen)
und mehr bevorzugt 0,001 bis 1% (Gewicht/Volumen).
-
Die Konzentration des Amphotensids
im jeweiligen Reagens bei der Durchführung der Methode mit 2 Reagenzien
für die
Messung der Änderungen
von LDL-Cholesterin hängt
von den Mengen der Probe ab, von dem ersten Reagens und dem zweiten
Reagens. Wenn das Amphotensid lediglich im ersten Reagens enthalten
ist, wird die Konzentration des Amphotensids bevorzugt ausgewählt aus
dem Bereich 0,0002 bis 20% (Gewicht/Volumen) und mehr bevorzugt
0,002 bis 2% (Gewicht/Volumen). Wenn das Amphotensid lediglich in
dem zweiten Reagens enthalten ist, wird die Konzentration des Amphotensids
bevorzugt ausgewählt
aus dem Bereich 0,0002 bis 20% (Gewicht/Volumen) und mehr bevorzugt
0,002 bis 2% (Gewicht/Volumen). Wenn darüber hinaus das Amphotensid
sowohl in dem ersten als auch in dem zweiten Reagens enthalten ist,
beträgt
die Konzentration des Amphotensids bevorzugt 0,0001 bis 20% (Gewicht/Volumen)
und mehr bevorzugt 0,001 bis 2% (Gewicht/Volumen) im ersten Reagens
und bevorzugt 0,0001 bis 20% (Gewicht/Volumen) und mehr bevorzugt 0,001
bis 20% (Gewicht/Volumen) im zweiten Reagens.
-
Als das Cyclodextrin und/oder Derivat
davon kann so lange jedes beliebige verwendet werden, wie sie verhindern
können,
dass das in anderen Lipoproteinen als LDL enthaltene Cholesterin
zu der Reaktion der Cholesterinmessung in gleichzeitiger Gegenwart
von Amphotensid beiträgt.
-
Beispiele für Cyclodextrin sind α-Cyclodextrin, β-Cyclodextrin, γ-Cyclodextrin,
usw.
-
Beispiele für Cyclodextrin-Derivate sind
alkylierte Cyclodextrine, wie beispielsweise 2,6-Di-O-methyl-α-cyclodextrin,
2,3,6-Tri-O-methyl-α-cyclodextrin,
2,6-Di-O-ethyl-α-cyclodextrin,
2,3,6-Tri-O-ethyl-α-cyclodextrin,
2,6-Di-O-methyl-β-cyclodextrin, 2,3,6-Tri-O-methyl-β-cyclodextrin,
2,6-Di-O-ethyl-β-cyclodextrin, 2,3,6-Tri-O-ethyl-β-cyclodextrin,
2,6-Di-O-methyl-γ-cyclodextrin,
2,3,6-Tri-O-methyl-γ-cyclodextrin, 2,6-Di-O-ethyl-γ-cyclodextrin
und 2,3,6-Tri-O-ethyl-γ-cyclodextrin;
hydroxyalkylierte Cyclodextrine, wie beispielsweise 2-Hydroxyethyl-α-cyclodextrin, 2-Hydroxypropyl-α-cyclodextrin,
3-Hydroxypropyl-α-cyclodextrin, 2,3-Dihydroxypropyl-α-cyclodextrin,
2-Hydroxyethyl-β-cyclodextrin,
2-Hydroxypropyl-β-cyclodextrin,
3-Hydroxypropyl-β-cyclodextrin,
2,3-Dihydroxypropyl-β-cyclodextrin, 2-Hydroxyethyl-γ-cyclodextrin,
2-Hydroxypropyl-γ-cyclodextrin,
3-Hydroxypropyl-γ-cyclodextrin
und 2,3-Dihydroxypropyl-γ-cyclodextrin;
acylierte Cyclodextrine, wie beispielsweise 2,3,6-Tri-O-acetyl-α-cyclodextrin,
2,3,6-Tri-O-acetyl-β-cyclodextrin
und 2,3,6-Tri-O-acetyl-γ-cyclodextrin;
Zucker-modifizierte Cyclodextrine, wie beispielsweise 6-O-α-D-Glucosyl-α-cyclodextrin,
6-O-α-D-Maltosyl-α-cyclodextrin,
6-O-α-D-Glucosyl-β-cyclodextrin,
6-O-α-D-Maltosyl-β-cyclodextrin, 6-O-α-D-Glucosyl-γ-cyclodextrin
und 6-O-α-D-Maltosyl-γ-cyclodextrin;
carboxyalkylierte Cyclodextrine, wie beispielsweise O-Carboxymethyl-α-cyclodextrin, O-Carboxymethyl-β-cyclodextrin
und O-Carboxymethyl-γ-cyclodextrin;
polymere Cyclodextrine, wie beispielsweise Poly-α-cyclodextrin, Poly-β-cyclodextrin und
Poly-γ-cyclodextrin.
Für diese
Cyclodextrine und Derivate davon können kommerzielle verfügbare verwendet
werden. Außerdem
können
in der vorliegenden Erfindung solche verwendet werden, die nach
bekannten Methoden synthetisch dargestellt wurden, die offenbart
wurden in den US-P-3 453 258, 3 453 259, Polymer Journal, Bd. 13,
Nr. 8, S. 777–781
(1981), die JP-A-61-266401, 63-122701 und 62-243602.
-
Die Konzentration der Anwendung dieser
Cyclodextrine und/oder Derivate davon ist so lange nicht speziell.
beschränkt,
wie diese Cyclodextrine und deren Derivate verhindern können, dass
das in anderen Lipoproteinen als dem LDL enthaltene Cholesterin
an der Reaktion der Cholesterinmessung teilnimmt. Die bevorzugte
Konzentration der Cyclodextrin und deren Derivate in der abschließenden Lösung (Reaktionslösung) zum
Zeitpunkt der Cholesterinmessung beträgt bevorzugt 0,0001 bis 10%
(Gewicht/Volumen) und mehr bevorzugt 0,001 bis 1% (Gewicht/Volumen).
-
Darüber hinaus hängt die
Konzentration der Cyclodextrine und deren Derivate in dem ersten
Reagens bei der Ausführung
der Methode mit zwei Reagenzien zur Messung der Änderungen des LDL-Cholesterins
von den Mengen der Probe ab, von dem ersten Reagens und dem zweiten
Reagens. In der Regel liegt der Bereich der Konzentration bei 0,0002
bis 20% (Gewicht/Volumen), vorzugsweise 0,002 bis 2% (Gewicht/Volumen).
-
Diese Cyclodextrine und deren Derivate
lassen sich allein oder als eine Mischung davon verwenden.
-
Zusätzlich zu den vorgenannten
Amphotensiden und Cyclodextrinen und deren Derivate können nach den
erfindungsgemäßen Verfahren
zum Messen konventionelle Reagenzien zu Cholesterinmessung verwendet
werden.
-
Das bedeutet, LDL-Cholesterin kann
in einer Lebendprobe, wie beispielsweise Serum, Plasma, usw., speziell
mit Hilfe einer konventionellen Methode in Gegenwart von Cyclodextrin
und/oder einem Derivat davon, beispielsweise unter Anwendung einer
enzymatischen Reaktion, gemessen werden.
-
Ein solcher konventioneller Prozess
(ein Prozess der oxidativen Farberzeugung) umfasst das Zersetzen
des Cholesterinesters in einer Probe mit CHE, um freies Cholesterin
und die Fettsäure
zu ergeben, Oxidieren des Produktes zusammen mit freiem Cholesterin,
das von Beginn an mit COD vorliegt, um Cholest-4-en-3-on und Wasserstoffperoxid
zu ergeben; Ausführen
der Reaktion der oxidativen Farberzeugung eines oxidierbaren farberzeugenden
Reagens mit dem erzeugten Wasserstoffperoxid in Gegenwart von POD; und
den erzeugten oxidierten Farbstoff einer colorimetrischen Bestimmung
unterziehen.
-
Ein anderer konventioneller Prozess
(Prozess der UV-Messung) umfasst das Zersetzen von Cholesterinester
in einer Probe mit CHE, um freies Cholesterin und die Fettsäure zu ergeben,
Umsetzen mit Nicotinamidadenindinukleotid oder dessen Phosphat (nachfolgend
bezeichnet als „NAD(P)") in Gegenwart des
von Beginn an vorhandenen freien Cholesterins und CHD; und Messen
des erzeugten NAD(P)H unter Anwendung von ultraviolettem Licht von
340 nm.
-
Das in der vorliegenden Erfindung
verwendete COD ist auf seine Herkunft nicht speziell beschränkt. Es
können
solche verwendet werden, wie sie konventionell auf dem Gebiet zur
Anwendung gelangen, beispielsweise solche, die von Mikroorganismen
hergeleitet sind, wie beispielsweise Nocardia Genera und Pseudomonas
Genera sowie von tierischen Organen, wie beispielsweise Rinderpankreas.
Die Anwendungsmenge von COD in der abschließenden Reaktionslösung zum
Zeitpunkt der Cholesterinmessung beträgt vorzugsweise 0,02 bis 10
u/ml und mehr bevorzugt 0,1 bis 2 u/ml.
-
Das in der vorliegenden Erfindung
verwendete CHE ist auf seine Herkunft nicht speziell beschränkt. Es
können
solche verwendet werden, wie sie konventionell auf dem Gebiet zur
Anwendung gelangen, beispielsweise solche, die von Mikroorganismen
hergeleitet sind, wie beispielsweise Candida Genera und Pseudomonas
Genera, sowie von tierischen Organen, wie beispielsweise Rinderpankreas.
Die Anwendungsmenge von CHE in der abschließenden Reaktionslösung zum
Zeitpunkt der Cholesterinmessung beträgt bevorzugt 0,02 bis 10 u/ml,
mehr bevorzugt 0,1 bis 2 u/ml.
-
Das in der vorliegenden Erfindung
verwendete POD ist auf seine Herkunft nicht speziell beschränkt. Es
können
solche verwendet werden, wie sie konventionell auf dem Gebiet zur
Anwendung gelangen, beispielsweise solche, die von Pflanzen hergeleitet
sind, wie beispielsweise Meerrettich und Rettich; Mikroorganismen,
wie beispielsweise Schimmel und Hefe; sowie Leukozyten und Schilddrüsen von
Tieren. Die Anwendungsmenge von POD in der abschließenden Reaktionslösung zum
Zeitpunkt der Cholesterinmessung beträgt bevorzugt 0,01 bis 50 u/ml,
mehr bevorzugt 0,1 bis 5 u/ml.
-
Als die Reagenzien zur oxidativen
Farberzeugung, die in der vorliegenden Erfindung verwendet werden,
können
solche zur Anwendung gelangen, die eine Farbe erzeugen, wenn sie
mit Wasserstoffperoxid in Gegenwart von POD reagieren. Beispiele
dafür sind
eine Kombination eines Kupplers, wie beispielsweise 4-Aminoantipyrin
(4-AA) und ein Entwickler, der einen Farbstoff durch oxidative Kondensation
mit dem Kuppler erzeugen kann, beispielsweise eine Kombination von
4-AA und einer phenolischen Verbindung, einer Naphthol-Verbindung oder einer
Anilin-Verbindung, einer Kombination von 3-Methyl-2-benzothiazolinon-hydrozon und
einer Anilin-Verbindung, usw.; farberzeugende Mittel, die eine Farbe
von sich aus durch Oxidation erzeugen können, wie beispielsweise 2,2'-Azinobis-(3-ethylbenzothiazolin-6-sulfonsäure), Triphenylmethan-Leukofarbstoffe,
Diphenylamin-Derivate, Benzidin-Derivate, Triallylimidazol-Derivate,
Leuco-Methanblau-Derivate und o-Phenylendiamin-Derivate.
-
Als Entwickler können Phenyl-Verbindungen verwendet
werden, wie beispielsweise: Phenol, p-Chlorphenol und 2,4-Dichlorphenol;
Naphthanol-Verbindungen, wie beispielsweise 1-Naphthol, 1-Naphthol-2-sulfonsäure und
1-Naphthol-2-carbonsäure;
Anilin-Verbindungen, wie beispielsweise N,N-Diethylanilin, N-Ethyl-N-(β-hydroxyethyl)-m-toluidin,
N-Ethyl-N-(2-hydroxy-3-sulfopropyl)-3,5-dimethoxyanilin, (DAOS), N-Ethyl-N-(2-hydroxy-3-sulfopropyl)-3,5-dimethoxy-4-fluoranilin (FDAOS),
N-(2-Hydroxy-3-sulfopropyl)-3,5-dimethoxyanilin (HDAOS), N-Ethyl-N-(2-hydroxy-3-sulfopropyl)-m-toluidin
(TOOS) und N-Ethyl-N-(3-methylphenyl)-N'-succinyl-ethylendiamin (EMSE).
-
Die Anwendungsmenge des Kupplers,
sofern der Kuppler in Kombination mit einem Entwickler verwendet
wird, ändert
sich in Abhängigkeit
von der Art des Kupplers, von der Art des Entwicklers, die vereint
werden sollen. Die Konzentration des Kupplers in der abschließenden Lösung (Reaktionslösung zum Zeitpunkt der
Cholesterinmessung beträgt
bevorzugt 0,01 bis 100 mM und mehr bevorzugt 0,1 bis 10 mM. Sofern
4-AA als Kuppler verwendet wird, beträgt die Konzentration von 4-AA
in der abschließenden
Reaktionslösung
zum Zeitpunkt der Cholesterinmessung bevorzugt 0,01 bis 50 mM, mehr
bevorzugt 0,1 bis 5 mM.
-
Die Anwendungsmenge des Entwicklers ändert sich
in Abhängigkeit
von der Art des Entwicklers und der Art des Kupplers, die vereint
werden. Die Konzentration des Entwicklers in der abschließenden Reaktionslösung zum
Zeitpunkt der Cholesterinmessung beträgt bevorzugt 0,01 bis 50 mM,
mehr bevorzugt 0,1 bis 5 mM.
-
Beispiele für die Triphenylmethan-Leukofarbstoffe
sind Leukomalachitgrün,
Bis(p-diethylaminophenyl)-2-sulfophenylmethan, Bis-(p-diethylaminophenyl)-3,4-disulfopropoxyphenylmethan-Dinatriumsalz,
usw.
-
Beispiele für die Diphenylamin-Derivate
sind Bis(4-di(2-butoxyethyl)amino-2-methylphenyl]amin, N,N-bis(4-diethylamino-2-methylphenyl)-N'-p-toluolsulfonylharnstoff,
usw.
-
Beispiele für die Leukomethylenblau-Derivate
sind 10-(Carboxymethylaminocarbonyl)-3,7-bis(dimethylamino)phenothiazin-Natriumsalz,
10-[3-(Methoxycarbonylaminomethyl)phenylmethylaminocarbonyl]-3,7-bis(dimethylamino)phenothiazin,
usw.
-
Beispiele für die Benzidin-Derivate sind
Benzidin, o-Toluidin, o-Dianisidin, 3,3'-Diaminobenzidin, 3,3',5,5'-Tetraaminobenzidin,
usw.
-
Beispiele für Triallylimidazol-Derivate
sind 2-(4-Carboxyphenyl)-3-N-methylcarbamoyl-4,5-bis(4-diethylaminophenyl)imidazol,
2-(3-Methoxy-4-diethylaminophenyl)-3-N-methylcarbamoyl-4,5-bis(2-methyl-4-diethylaminophenyl)imidazol,
usw.
-
Die Anwendungsmenge dieser farberzeugenden
Mittel wird geeigneterweise aus den konventionell zur Anwendung
gelangenden Bereichen auf diesem Gebiet gewählt.
-
Das in der vorliegenden Erfindung
verwendete CHD ist auf seine Herkunft nicht beschränkt. Es
können konventionell
verwendete zur Anwendung gelangen, wie beispielsweise die von Nocardia
Genera hergeleiteten, usw. Die Anwendungsmenge in der fertigen Reaktionslösung zum
Zeitpunkt der Cholesterinmessung beträgt vorzugsweise 0,1 bis 100
u/ml, mehr bevorzugt 1 bis 50 u/ml.
-
Das in der vorliegenden Erfindung
verwendete NAD(P) ist nicht speziell beschränkt und es können auch
solche verwendet werden die konventionell auf diesem Gebiet zur
Anwendung gelangen. Die Anwendungsmenge von NAD(P) in der fertigen
Lösung
(Reaktionslösung)
zum Zeitpunkt der Cholesterinmessung beträgt bevorzugt 0,02 bis 50 mM,
mehr bevorzugt 0,1 bis 10 mM.
-
Die Reagenzien für die Messung von LDL-Cholesterin,
die in der vorliegenden Erfindung verwendet werden, sind solche,
wie sie konventionell zur Messung von LDL-Cholesterin in einer Probe
zur Anwendung gelangen, die von einem Lebendkörper abgenommen wurde, wie
beispielsweise Serum, Plasma, usw. mit der Ausnahme der Verwendung
des Amphotensids und Cyclodextrins und/oder dessen Derivate. Die
konventionell verwendeten Reagenzien schließen ein: COD, CHE, POD, oxidierbare
farberzeugende Reagenzien, usw., die in dem Prozess der oxidativen
Farberzeugung verwendet werden; CHE, CHD, NAD(P), usw., die in dem
Prozess der Messung von violettem Licht verwendet werden. Diese
Reagenzien werden in Konzentrationen verwendet, die zum Messen von
LDL-Cholesterin geeignet sind.
-
Die Reagenzien zum Messen von LDL-Cholesterin,
die in der vorliegenden Erfindung verwendet werden, können für eine Methode
mit einem Reagens, für
eine Methode mit zwei Reagenzien oder eine Methode mit drei oder
mehreren Reagenzien hergestellt werden. Wenn die Reagenzien in zwei
oder mehrere Reagenzien unterteilt sind, sind die folgenden Zusammensetzungen
hinsichtlich der Spezifizität,
der Messgenauigkeit, usw. bevorzugt.
-
Im Fall des Prozesses der oxidativen
Farberzeugung schließt
das erste Reagens Cyclodextrin und/oder dessen Derivat ein und das
zweite Reagens schließt
COD ein. Andere Reagenzien, wie beispielsweise Amphotenside, Enzyme,
wie beispielsweise CHE und POD, Kuppler und Entwickler, können in
mindestens dem ersten oder zweiten Reagens einbezogen werden.
-
Im Fall des Prozesses der UV-Messung
ist in dem ersten Reagens Cyclodextrin und/oder ein Derivat davon
einbezogen und in dem zweiten Reagens CHD einbezogen sowie andere
Reagenzien, wie beispielsweise NAD(P), die in mindestens entweder
dem ersten oder zweiten Reagens einbezogen sind.
-
Wenn das erfindungsgemäße Verfahren
nach einer Methode mit zwei Reagenzien ausgeführt wird, wird eine Probe mit
einem ersten Reagens behandelt, das Cyclodextrin und/oder ein Derivat
davon einschließt, beispielsweise
durch Mischen der Probe mit dem ersten Reagens, wobei die behandelte
Probe umgesetzt wird mit einem zweiten Reagens, in das COD oder
CHD einbezogen ist, und zwar in Gegenwart des Cyclodextrins und/oder
eines Derivats davon und des Amphotensids. Diese vorgenannten Schritte
sind vom Standpunkt der Spezifizität, der Messgenauigkeit, usw.
bevorzugt.
-
Im Fall des Prozesses der oxidativen
Farberzeugung werden die folgenden Kombinationen von Reagenzien
bevorzugt verwendet:
- (i) ein erstes Reagens,
einschließend
Cyclodextrin und/oder ein Derivat davon und ein Amphotensid,
ein
zweites Reagens, einschließend
COD, und
ein Kuppler, ein Entwickler, POD und CHE, die in mindestens
entweder dem ersten Reagens oder dem zweiten Reagens einbezogen
sind;
- (ii) ein erstes Reagens, einschließend Cyclodextrin und/oder
ein Derivat davon und CHE,
ein zweites Reagens, einschließend COD,
und
ein Kuppler, ein Entwickler, POD und ein Amphotensid, die
in mindestens entweder dem ersten Reagens oder dem zweiten Reagens
einbezogen sind, und
- (iii) ein erstes Reagens, einschließend Cyclodextrin und/oder
ein Derivat davon, Amphotensid und CHE,
ein zweites Reagens,
einschließend
COD, und
ein Kuppler, ein Entwickler und POD, die in mindestens
entweder dem ersten Reagens oder dem zweiten Reagens einbezogen
sind;
-
Im Fall des Prozesses der Messung
von ultraviolettem Licht sind die folgenden Kombinationen von Reagenzien
bevorzugt verwendet:
- (i') ein erstes Reagens, einschließend Cyclodextrin
und/oder ein Derivat davon und ein Amphotensid,
ein zweites
Reagens, einschließend
CHD, und
NAD(P) und CHE, die in mindestens dem ersten Reagens
oder dem zweiten Reagens einbezogen sind;
- (ii') ein erstes
Reagens, einschließend
Cyclodextrin und/oder ein Derivat davon und CHE,
ein zweites
Reagens, einschließend
CHD, und
NAD(P) und ein Amphotensid, die in mindestens dem
ersten Reagens oder dem zweiten Reagens einbezogen sind, und
- (iii') ein erstes
Reagens, einschließend
Cyclodextrin und/oder ein Derivat davon, ein Amphotensid und CHE,
ein
zweites Reagens, einschließend
CHD, und
NAD(P), das in entweder dem ersten Reagens oder dem
zweiten Reagens einbezogen ist.
-
Wenn die Reagenzien zum Messen des
LDL-Cholesterins der vorliegenden Erfindung für eine Methode mit zwei Reagenzien
hergestellt werden, liegen vorzugsweise das Amphotensid und/oder
CHE gemeinsam mit dem Cyclodextrin und/oder einem Derivat davon
in dem ersten Reagens vor, um die Spezifizität des LDL-Cholesterins und
die Messgenauigkeit des LDL-Cholesterins
zu verbessern.
-
Darüber hinaus besteht unter den
Kombinationen der vorstehend genannten Reagenzien, bei gleichzeitigem
Vorhandensein von Amphotensid und CHE die Möglichkeit einer Verringerung
der Stabilität
der CHE-Aktivität
durch das Amphotensid. Daher wird in diesem Fall vorzugsweise CHE
sowohl in das erste Reagens als auch in das zweite Reagens einbezogen.
Im Fall von Reagenzien für
den Prozess der oxidativen Farberzeugung werden in das erste Reagens
Cyclodextrin und/oder ein Derivat davon, ein Amphotensid und CHE
einbezogen und in das zweite Reagens werden COD und CHE einbezogen,
und ein Kuppler, ein Entwickler und POD werden in mindestens entweder
dem ersten Reagens oder dem zweiten Reagens einbezogen. Im Fall
von Reagenzien für
den Prozess der UV-Messung sind in das erste Reagens Cyclodextrin
und/oder ein Derivat davon, ein Amphotensid und CHE einbezogen,
in das zweite Reagens sind CHD und CHE einbezogen und NAD(P) ist
in mindestens entweder dem ersten Reagens oder dem zweiten Reagens
einbezogen.
-
Zusätzlich zu der vorgenannten
Kombination von Reagenzien für
den Prozess der oxidativen Farberzeugung sind in dem ersten Reagens
entweder bevorzugt ein Kuppler und ein Entwickler einbezogen, während der
Rest von ihnen bevorzugt in dem zweiten Reagens einbezogen ist.
-
Die Reagenzien zum Messen von LDL-Cholesterin
nach der vorliegenden Erfindung können ein oder mehrere Puffer
enthalten. Die in der vorliegenden Erfindung verwendbaren Puffer
hängen
von den Kombinationen der verschiedenen Enzyme und Reagenzien der
oxidativen Farberzeugung ab, wobei jedoch konventionelle Puffer
verwendet werden können,
die üblicherweise
auf diesem Gebiet zur Anwendung gelangen. Bevorzugt ist die Verwendung
von Puffern mit einer Pufferwirkung im pH-Bereich 5 bis 11. Die
Puffer können
vorzugsweise in einer Konzentration von 1 mM bis 5 M und mehr bevorzugt
5 mM bis 1 M verwendet werden.
-
Unter Berücksichtigung der Spezifizität auf LDL-Cholesterin
sind bevorzugte Beispiele für
die Puffer: Aminoethansulfonsäure-Derivate,
wie beispielsweise N-(2-Acetamido)-2-aminoethansulfonsäure (ACES), N,N-Bis(2-hydroxyethyl)-2-aminoethansulfonsäure (BES),
N-Cyclohexyl-2-aminoethansulfonsäure
(CHES), 2-[4-(2-Hydroxyethyl)-1-piperazinyl]ethansulfonsäure (HEPES),
2- Morpholinoethansulfonsäure (MES),
Piperazin-1,4-bis(2-ethansulfonsäure)
(PIPES) und N-Tris(hydroxymethyl)methyl-2-aminoethansulfonsäure (TES); Aminopropansulfonsäure-Derivate,
wie beispielsweise N-Cyclohexyl-3-aminopropansulfonsäure (CAPS), N-Cyclohexyl-2-hydroxy-3-aminopropansulfonsäure (CAPSO),
3-[N,N-Bis(2-hydroxyethyl)amino]-2-hydroxypropansulfonsäure (DEPSO),
3-[4-(2-Hydroxyethyl)-1-piperazinyl]propansulfonsäure (EPPS),
2-Hydroxy-3-[4-(2-hydroxyethyl)-1-piperazinyl]propansulfonsäure (HEPPSO),
3-Morpholinopropansulfonsäure (MOPS),
2-Hydroxy-3-morpholinopropansulfonsäure (MOPSO), Piperazin-1,4-bis(2-hydroxy-3-propansulfonsäure) (POPSO),
N-Tris(hydroxymethyl)methyl-3-aminopropan-sulfonsäure (TAPS)
und 2-Hydroxy-N-tris(hydroxymethyl)methyl-3-aminopropansulfonsäure (TAPSO);
aliphatische Amine, die eine Carboxyl-Gruppe oder Sulfonsäure-Gruppe
haben, wie beispielsweise Glycin-Derivate, z. B. N-(2-Acetamido)iminodiessigsäure (ADA),
N,N-Bis(2-hydroxyethyl)glycin
(Bicine), N-[Tris(hydroxymethyl)-methyl]glycin (Tricine), usw.
-
In die Reagenzien zur Messung von
LDL-Cholesterin nach der vorliegenden Erfindung können eine oder
mehrere ionische Verbindungen einbezogen sein, wie beispielsweise
Polyanionen, z. B. Dextransulfat, Heparin, Heparansulfat und Wolframatophosphorsäure, und
zwar einzeln oder als Mischung davon. Darüber hinaus ist es möglich, zweiwertige
Kationen zu verwenden, wie beispielsweise Mg2+,
Mn2+ und Ca2+ (oder
ein oder mehrere Metallsalze, die diese zweiwertigen Kationen erzeugen
können)
in Kombination mit der ionischen Verbindung. Die Konzentration dieser
Additive ist nicht speziell beschränkt. Die Konzentration der
ionischen Verbindung in der abschließenden Lösung (Reaktionslösung) beträgt vorzugsweise
0,01 bis 10% (Gewicht/Volumen). Die Konzentration der zweiwertigen
Kationen in der abschließenden
Lösung
(Reaktionslösung)
beträgt
bevorzugt 0,1 bis 200 mM.
-
In die Reagenzien zur Messung von
LDL-Cholesterin nach der vorliegenden Erfindung können ein oder
mehrere polyklonale Antikörper
oder monoklonale Antikörper
einbezogen sein, um Cholesterin in anderen Lipoproteinen als LDL
an der Teilnahme der Reaktion der Cholesterinmessung abzuhalten.
-
Beispiele für derartige Antikörper sind
Anti-Apoliprotein-A-Antikörper,
Anti-Apoliprotein-C-Antikörper, Anti-Apoliprotein-E-Antikörper, Anti-α-Lipoprotein-Antikörper, usw.
-
Die Konzentration dieser Antikörper ist
so lange nicht speziell beschränkt,
wie sie verhindern, dass in anderen Lipoproteinen als dem LDE-enthaltenes
Cholesterin an der Reaktion der Cholesterinmessung teilnimmt. Bevorzugt
werden diese Antikörper
der abschließenden
Lösung
(Reaktionslösung)
zuge setzt, um die Konzentration auf 0,001 bis 10 mgAb/ml und mehr
bevorzugt 0,01 bis 1 mgAb/ml zu bringen.
-
Die Reagenzien zur Messung des LDL-Cholesterins
nach der vorliegenden Erfindung können ferner ein oder mehrere
andere Tenside als die Amphotenside enthalten, die konventionell
auf diesem Gebiet zur Anwendung gelangen, wie beispielsweise nicht
ionische Tenside, wie beispielsweise Polyoxyethylen- isooctylphenyether,
Polyoxyethylenalkylphenylether, Polyoxyethylennonylphenylether,
Polyoxyethylencetylether, Polyoxyethylenoleylether, Polyethylglykolmonolaurat
und Polyethylenlaurylether; Kationtenside, wie beispielsweise Stearyltrimethylammoniumchlorid
und Alkylbenzyldimethylammoniumchloride; Aniontenside, wie beispielsweise
Cholinsäure,
Desoxycholinsäure
und Polyoxyethylenalkylphenylether-Natriumsulfonat. Diese Tenside
können
einzeln oder als eine Kombination davon verwendet werden. Die Konzentration
dieser Tenside ist nicht speziell beschränkt, liegt vorzugsweise jedoch
im Bereich von 0,0001 bis 10% (Gewicht/Volumen), mehr bevorzugt
0,001 bis 1% (Gewicht/Volumen) in der abschließenden Lösung (Reaktionslösung).
-
Das LDL-Cholesterin kann nach der
vorliegenden Erfindung im Fall der Methode mit zwei Reagenzien wie
folgt gemessen werden:
-
1) Prozess der oxidativen
Farberzeugung
-
Es wird eine Lebendkörperprobe,
wie beispielsweise Serum und Plasma, mit einem ersten Reagens gemischt,
das beispielsweise ein Amphotensid enthält, Cyclodextrin und/oder ein
Derivat davon, CHE und einen Kuppler (oder einen Entwickler) und
nach Erfordernis einen oder mehrere Puffer, Antikörper, ionische
Verbindungen, zweiwertige Kationen, usw., um die Probe zu behandeln,
gefolgt von einer Reaktion für
1 bis 30 Minuten bei 2° bis
40°C und
der Messung der Absorption (OD1). Danach
wird die Reaktionslösung
mit einem zweiten Reagens gemischt, das beispielsweise COD enthält, CHE,
POD und einen Entwickler (oder einen Kuppler) und nach Erfordernis
einen oder mehrere Puffer, usw., gefolgt von der Reaktion für 1 bis
60 Minuten bei 2° bis
40°C und
der Messung der Absorption (OD2). Sodann
wird die Absorption (OD3) erhalten, indem
der von OD1 abgeleitete Wert (z. B. ein
Wert, der durch Multiplikation von OD1 mit
einem Korrekturkoeffizienten erhalten wird) von OD2 subtrahiert
wird. Der resultierende OD3-Wert wird auf
eine Eichkurve angewendet, in der eine Beziehung zwischen den LDL-Cholesterinkonzentrationen
dargestellt ist, und der OD3-Wert nach den gleichen
Prozeduren, wie sie vorstehend ausgeführt wurden, unter Verwendung
von Standardlösungen
erhalten, z. B. mit einem Gehalt bekannter Cholesterin-Mengen. Auf diese
Weise lässt
sich der LDL-Cholesterinwert in der Lebendprobe erhalten.
-
2) Prozess der UV-Messung
-
Eine Lebendkörperprobe, wie beispielsweise
Serum und Plasma, wird mit einem ersten Reagens gemischt, das beispielsweise
ein Amphotensid enthält,
Cyclodextrin und/oder ein Derivat davon und CHE und nach Erfordernis
ein oder mehrere Puffer, Antikörper,
ionische Verbindungen, zweiwertige Kationen, usw., um die Probe
zu behandeln, gefolgt von der Reaktion für 1 bis 30 Minuten bei 2° bis 40°C und Messung
der Absorption (OD1') bei 340 nm. Danach wird die Reaktionslösung mit
einem zweiten Reagens gemischt, das beispielsweise CHD enthält, CHE
und NAD(P) sowie nach Erfordernis einen oder mehrere Puffer, gefolgt
von einer Reaktion für
1 bis 60 Minuten bei 2° bis
40°C und
der Messung der Absorption (OD2') bei 340 nm. Danach wird
die Absorption (OD3') erhalten, indem der von OD1 derivierte Wert (beispielsweise ein Wert,
der durch Multiplikation von OD1' mit einem Korrekturkoeftzienten
erhalten wird) von OD2' subtrahiert wird. Der resultierende OD3'-Wert
wird auf eine Eichkurve angewendet, die eine Beziehung zwischen
den LDL-Cholesterinkonzentrationen und dem OD3' darstellt, der nach
den gleichen Prozeduren, wie sie vorstehend erwähnt wurden, unter Anwendung
von Standardlösungen
erhalten wird, z. B. mit einem Gehalt bekannter Cholesterin-Mengen.
Auf diese Weise lässt
sich der LDL-Cholesterinwert in der Lebendprobe erhalten.
-
Wenn der Prozess der Messung des
LDL-Cholesterins nach der vorliegenden Erfindung mit Hilfe der Methode
mit einem Reagens ausgeführt
wird, können
die folgenden Schritte eingesetzt werden:
-
1) Prozess der oxidativen
Farberzeugung
-
Es wird eine Lebendkörperprobe,
wie beispielsweise Serum und Plasma, mit einer Reagenslösung gemischt,
die beispielsweise CHE enthält,
COD, POD, ein Reagens zur oxidativen Farberzeugung, ein Amphotensid
und Cyclodextrin und/oder ein Derivat davon und nach Erfordernis
einen oder mehrere Puffer, Antikörper,
ionische Verbindungen, zweiwertige Kationen, usw., gefolgt von einer
Reaktion für
1 bis 30 Minuten bei 2° bis
40°C und
der Messung der Absorption (ODS). Ein Blindwert
(ODB1) wird erhalten, indem die gleichen
Reagenzien, wie sie vorstehend genannt wurden, verwendet werden
und die gleichen Prozeduren, wie sie vorstehend ausgeführt wurden,
ausgeführt
werden, während
anstelle der Lebendkörperprobe
physiologische Kochsalzlösung
verwendet wird. Sodann wird die Absorption (ODR)
erhalten, indem ODB1 von ODS subtrahiert
wird. Der resultierende ODR-Wert wird auf
die Eichkurve angewendet, die eine Beziehung zwischen den LDL-Cholesterinkonzentrationen
und dem ODR darstellt, das unter Anwendung
der gleichen Prozeduren, wie sie vorstehend ausgeführt wurden,
unter Verwendung von Standardlösungen
erhalten wird, z. B. mit einem Gehalt bekannter Cholesterin-Mengen.
Auf diese Weise lässt
sich der LDL-Cholesterinwert in der Lebendkörperprobe erhalten.
-
2) Prozess der UV-Messung
-
Eine Lebendkörperprobe, wie beispielsweise
Serum und Plasma, wird mit einer Reagenslösung gemischt, die beispielsweise
CHE enthält,
CHD, NAD(P), ein Amphotensid, Cyclodextrin und/oder ein Derivat
davon und nach Erfordernis einen oder mehrere Puffer, Antikörper, ionische
Verbindungen, zweiwertige Kationen, usw., gefolgt von der Reaktion
für 1 bis
30 Minuten bei 2° bis
40°C und
Messung der Absorption (ODS') bei 340 nm. Ein
Blindwert (ODB1') wird erhalten, indem die gleichen
Reagenzien, wie sie vorstehend genannt wurden, zur Anwendung gelangen
und die gleichen Prozeduren, wie sie vorstehend ausgeführt wurden,
ausgeführt
werden, während
anstelle der Lebendprobe physiologische Kochsalzlösung verwendet
wird. Sodann wird die Absorption (ODR') erhalten, indem ODB1' von ODS' subtrahiert wird.
Der resultierende ODS'-Wert wird auf eine Eichkurve angewendet,
die eine Beziehung zwischen den LDL-Cholesterinkonzentrationen und dem ODS' darstellt,
der unter Anwendung der gleichen Prozeduren, wie sie vorstehend
ausgeführt
wurden, unter Verwendung von Standardlösungen erhalten wird, z. B.
mit einem Gehalt bekannter Cholesterin-Mengen. Auf diese Weise lässt sich
der LDL-Cholesterinwert in der Lebendprobe erhalten.
-
In den vorgenannten Fällen können anstelle
der Absorption als eine optische Änderung andere optische Änderungen
verwendet werden, wie beispielsweise der Transmissionsgrad.
-
Die Ausrüstung zum Messen des LDL-Cholesterins
nach der vorliegenden Erfindung wird für LDL-Cholesterin in einer
Probe angewendet, die von einem Lebendkörper abgenommen wird, wie beispielsweise
Serum und Plasma, und die folgende Beschaffenheit hat:
- 1) für
den Prozess der oxidativen Farberzeugung
ein erster Behälter, der
ein erstes Reagens enthält,
das Cyclodextrin und/oder ein Derivat davon aufweist, ein Amphotensid,
CHE und einen Kuppler (oder einen Entwickler) und
ein zweiter
Behälter,
der ein zweites Reagens enthält,
das COD aufweist, CHE, POD und einen Entwickler (oder einen Kuppler);
- 2) für
einen Prozess der UV-Messung
ein erster Behälter, der ein erstes Reagens
enthält,
das Cyclodextrin und/oder ein Derivat davon aufweist, ein Amphotensid
und CHE, und
ein zweiter Behälter, der ein zweites Reagens
enthält,
das CHD aufweist, NAD(P) und CHE.
-
Bevorzugte Ausführungsformen und Beispiele
für einzelne
elementare Bestandteile sind die, wie sie vorstehend genannt wurden.
Es muss nicht erwähnt
werden, dass die Ausrüstung
mit LDL-Cholesterin-Standardsubstanzen kombiniert werden kann.
-
Die erfindungsgemäßen Verfahren zum Messen des
LDL-Cholesterins können
in Gegenwart eines Amphotensids und Cyclodextrin und/oder einem
Derivat davon ausgeführt
werden, so dass das Cholesterin in anderen Lipoproteinen als dem
LDL, z. B. nicht nur HDL, sondern auch VLDL, CM, usw., nicht wesentlich
zu der Reaktion beiträgt
und LDL-Cholesterin spezifisch reagiert, was dazu führt, dass
die Messung des LDL-Cholesterins mit Hilfe des Endpunktassays möglich wird,
was bei konventionellen Prozessen unmöglich war. Was die Standardsubstanzen
betrifft, ist es außerdem
nicht erforderlich, reines LDL-Cholesterin
zu verwenden. Anstelle dessen ist es möglich, eine Standardlösung zu
verwenden, die Cholesterin oder ein Standardserum mit den gleichen
Eigenschaften wie Viskosität
und Dichte enthält,
wie normales Serum.
-
Die vorliegende Erfindung wird anhand
der folgenden Beispiele veranschaulicht, die jedoch nicht einschränkend sind.
-
Beispiel 1
-
Unter Verwendung eines Autoanalyzers
vom Typ Hitachi 7170 (hergestellt von Hitachi, Ltd.) wurde zur Untersuchung
des Reaktionsvermögens
von Cholesterin in verschiedenen durch Ultrazentrifugation fraktionierten
Lipoproteinen nach dem Verfahren der vorliegenden Erfindung gemessen.
-
[Proben]
-
Als Proben wurden LDL-Fraktionen,
HDL-Fraktionen, VLDL-Fraktionen und CM-Fraktionen verwendet, die
aus Serum durch Fraktionierung unter Anwendung bekannter Methoden
der Ultrazentrifugation erhalten wurden.
-
In jeder Probe wurde Cholesterin
wie früher
unter Verwendung einer kommerziell verfügbaren Reagensausrüstung zum
Messen von Gesamtcholesterin gemessen (L-Typ Wako CHO·H, ein
Warenzeichen, hergestellt von der Wako Pure Chemical Industries,
Ltd.), und zwar nach einer Standardprozedur, wie sie in der Bedienungsanweisung
für die
Ausrüstung
beschrieben wurde.
-
[Reagenzien]
-
(Reagens 1)
-
R-1: 50 mM Piperazin-1,4-bis(2-ethansulfonsäure) (PIPES)-NaON-Puffer
(pH 7,0) mit einem Gehalt von:
- (i) 2,6-Di-O-methyl-α-cyclodextrin
(hergestellt von der Wako Pure Chemical Industries, Ltd., nachfolgend bezeichnet
als „DM-α-CD") 0,06% (Gewicht/Volumen);
- (ii) N-(2-Nydroxy-3-sulfopropyl)-3,5-dimethoxyanilin-Natriumsalz
(HDAOS, hergestellt von Dojindo Laboratories Co., Ltd.) 0,6 mM;
und
- (iii) Na2SO4 0,4
M
-
R-2: 50 mM PIPES-NaOH-Puffer (pH
7,0) mit einem Gehalt von:
- (i) COD (hergestellt
von Amano Pharmaceutical Co., Ltd.) 4 u/ml;
- (ii) CHE (hergestellt von Asahi Kasei Kogyo K. K.) 4 u/ml;
- (iii) POD (hergestellt von Toyobo Co., Ltd.); 4-AA 3 mM; und
- (iv) einem Amphotensid, das in Tabelle 1 dargestellt ist; 0,01%
(Gewicht/Volumen).
-
(Amphotenside)
-
Es wurden die folgenden verwendet:
Lipomin
LA (Warenzeichen, hergestellt von Lion Corp.),
ein Aminocarbonsäure-Derivat.
-
Softazolin LPB-R (Warenzeichen, hergestellt
von Kawa-Ken Fine Chemical Co., Ltd.), Laurinsäureamidopropylbetain,
-
Softazolin CL (Warenzeichen, hergestellt
von Kawa-Ken Fine Chemical Co., Ltd.), 2-Alkyl-N-carboxymethyl-N-hydroxyethylimidazoliniumbetain,
-
Anhitol 24B (Warenzeichen, hergestellt
von Kao Corp.), Laurylbetain,
-
Enadicol L-30AN (Warenzeichen, hergestellt
von Lion Corp.), Natrium-N-lauroyl-N-methyl-β-alanin,
-
Zwittergent 3-08 (Warenzeichen, hergestellt
von Wako Pure Chemical Industries, Ltd.), N-Octyl-N,N-dimethyl-3-ammonio-1-propansulfonsäure.
-
(Reagens 2) [Vergleichsreagens]
-
R-1: das gleiche wie Reagens 1
-
R-2: das gleiche wie Reagens 1 mit
der Ausnahme der Verwendung der folgenden Tenside anstelle der Amphotenside.
-
(Tenside)
-
Emalgen A-90 (Warenzeichen, hergestellt
von Kao Corp.), Polyoxyethylen-Derivat,
-
Emalgen 709 (Warenzeichen, hergestellt
von Kao Corp.), Polyoxyethylenhöherer
Alkoholether,
-
Triton X-100 (Warenzeichen, hergestellt
von Rohm & Haas
Co.), Polyoxyethylenalkylphenylether.
-
(Reagens 3) [Vergleichsreagens]
-
R-1: 50 mM PIPES-NaOH-Puffer (pH
7,0) mit einem Gehalt von NDAOS von 0,6 mM und Na2SO4 0,4 M,
R-2: 50 mM PIPES-NaON-Puffer
(pH 7,0) mit einem Gehalt von:
- (i) COD (hergestellt
von Amano Pharmaceutical Co., Ltd.), 4 u/ml,
- (ii) CHE (hergestellt von der Asahi Kasei Kogyo K. K.), 4 u/ml,
- (iii) POD (hergestellt von der Toyobo Co., Ltd.), 6 u/ml, und
- (iv) 4-AA, 3 mM.
-
[Messbedingungen]
-
Die Messparameter wurden zur Messung
des Cholesterins in jeder Probe. wie folgt eingestellt:
Messmethode:
2 Punkt-Endpunkt [16]–[34]
Probenmenge:
3 μl
R-1:
270 μl
R-2:
90 μl
Wellenlänge der
Messung: 700/600 nm
Messtemperatur: 37°C
Konzentration der Standardsubstanz:
100 mg/dl
-
[Ergebnisse]
-
Umwandlung jedes Lipoproteins in%
wurde erhalten, indem der Cholesterinwert, der von jeder Probe erhalten
wurde, und der Cholesterinwert, der von jeder Probe unter Verwendung
einer kommerziell verfügbaren
Ausrüstung
verwendet wurde, in die folgende Formel eingesetzt wurden:
Formel:
Umwandlung (%) = (aus der Probe erhaltener Cholesterinwert) (mit
kommerzieller Ausrüstung
erhaltener Cholesterinwert) × 100
-
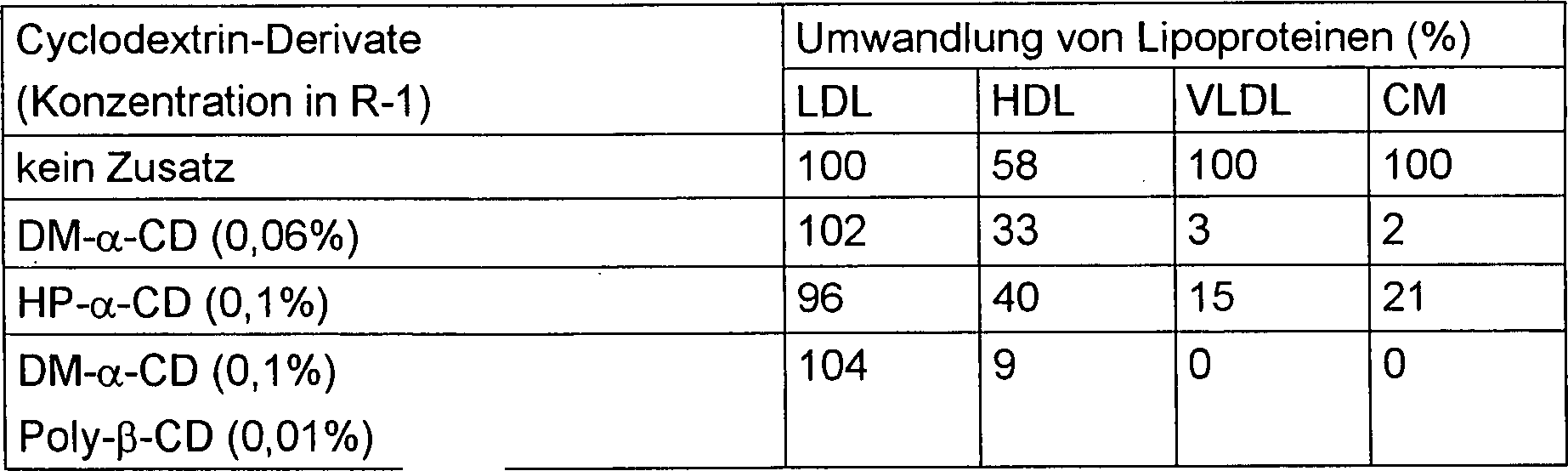
Diese Ergebnisse sind in Tabelle
1 dargestellt.
-
-
Wie aus den in Tabelle 1 gezeigten
Ergebnissen klar zu entnehmen ist, werden andere Lipoproteine als
LDL bei Verwendung von Reagens 1 kaum umgesetzt, da Cholesterin
in Gegenwart eines Amphotensids und DM-α-CD gemessen wird, woraus resultiert,
dass die Messung des Cholesterins in LDL spezifisch möglich wird.
Im Gegensatz dazu reagieren auch andere Lipoproteine als LDL bei
Ausführung
der Messung in Gegenwart eines nicht ionischen Tensids und DM-α-CD (Reagens
2) und in Abwesenheit eines Tensids und von DM-α-CD (Reagens 3), woraus resultiert,
dass spezifisch kein LDL-Cholesterin gemessen werden kann.
-
Wie vorstehend ausgeführt, ist
es erforderlich, zur spezifischen Messung des Cholesterins in LDL
die Messung in Gegenwart eines Amphotensids und von Cyclodextrin
und/oder einem Derivat davon auszuführen.
-
Beispiel 2
-
Ein anderes typisches Beispiel für die Ausrüstung zum
Messen von LDL-Cholesterin
in einer Lebendprobe läuft
wie folgt ab:
- (1) erstes Reagens (pH 6–8)
Cyclodextrin
und/oder ein Derivat davon,
Amphotensid,
CHE, und
Kuppler
(oder ein Entwickler);
- (2) zweites Reagens (pH 6–8)
COD,
CHE,
POD,
und
Entwickler (oder ein Kuppler).
-
Es wurden die gleichen Ergebnisse
wie in Beispiel 1 erhalten, indem die Ausrüstung verwendet wurde.
-
Beispiel 3 (nicht im Geltungsbereich
der beigefügten
Ansprüche)
-
Unter Verwendung eines Autoanalyzers
vom Typ Hitachi 7170 (hergestellt von Hitachi, Ltd.) wurde zur Untersuchung
des Reaktionsvermögens
von Cholesterin Cholesterin in verschiedenen durch Ultrazentrifugation
fraktionierten Lipoproteinen nach dem Verfahren der vorliegenden
Erfindung gemessen.
-
[Proben]
-
Als Proben wurden LDL-Fraktionen,
NDL-Fraktionen, VLDL-Fraktionen und CM-Fraktionen verwendet, die
aus Serum durch Fraktionierung unter Anwendung bekannter Methoden
der Ultrazentrifugation erhalten wurden.
-
In jeder Probe wurde Cholesterin
wie bisher unter Verwendung einer kommerziell verfügbaren Reagensausrüstung zum
Messen von Gesamtcholesterin gemessen (L-Typ Wako CNO·H, ein
Warenzeichen, hergestellt von der Wako Pure Chemical Industries,
Ltd.), und zwar nach einer Standardprozedur, wie sie in der Bedienungsanweisung
für die
Ausrüstung
beschrieben wurde.
-
[Reagenzien]
-
R-1: 100 mM PIPES-NaOH-Puffer (pH
7,0) mit einem Gehalt von:
- (i) HDAOS 0,6 mM;
- (ii) Na2SO4 0,4
M;
- (iii) ein Cyclodextrin-Derivat, das in Tabelle 2 gezeigt ist;
-
R-2: 100 mM PIPES-NaOH-Puffer (pH
7,0) mit einem Gehalt von:
- (i) COD (hergestellt
von Amano Pharmaceutical Co., Ltd.), 4 u/ml;
- (ii) CHE (hergestellt von Asahi Kasei Kogyo K. K.), 4 u/ml;
- (iii) POD (hergestellt von Toyobo Co., Ltd.), 6 u/ml; und
- (iv) 4-AA, 3 mM.
-
[Cyclodextrin-Derivate]
-
DM-α-CD (hergestellt von der Wako
Pure Chemical Industries, Ltd.)
-
HP-α-CD (Hydroxypropyl-α-cyclodextrin)
(hergestellt von der Wako Pure Chemical Industries, Ltd.)
-
Poly-β-DC (Poly-β-cyclodextrin) (hergestellt
von der Wako Pure Chemical Industries, Ltd.)
-
[Messbedingungen]
-
Die Messparameter zur Messung des
Cholesterins in jeder Probe wurden wie folgt eingestellt:
Messmethode:
2 Punkt-Endpunkt [16]–[34]
Probenmenge:
3 μl
R-1:
270 μl
R-2:
90 μl
Wellenlänge der
Messung: 700/600 nm
Messtemperatur: 37°C
Konzentration der Standardsubstanz:
100 mg/dl
-
[Ergebnisse]
-
Die Umwandlung jedes Lipoproteins
in % wurde in der gleichen Weise erhalten, wie in Beispiel 1 beschrieben
wurde.
-
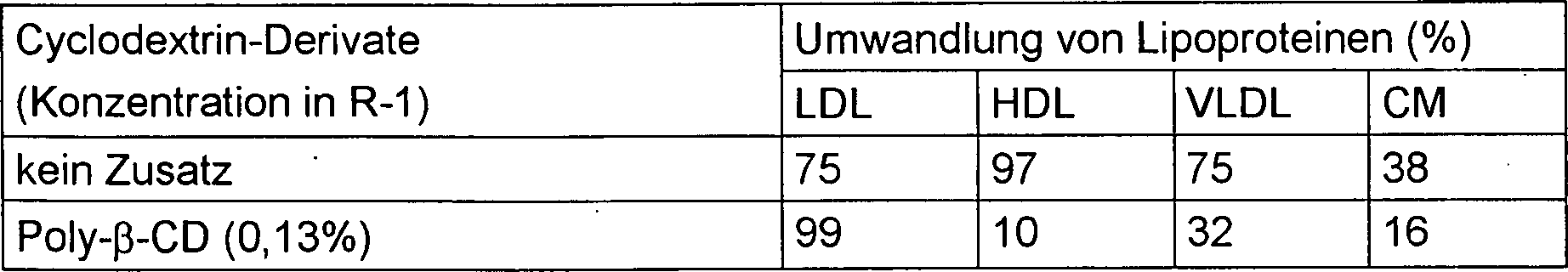
Die Ergebnisse sind in Tabelle 2
gezeigt.
-
-
Wie aus den in Tabelle 2 gezeigten
Ergebnisse klar zu ersehen ist, wird die Reaktion von anderen Lipoproteinen
als LDL bei Ausführung
der Cholesterinmessung in Gegenwart des/der speziellen Cyclodextrin-Derivates/Derivate
merklich unterdrückt.
Besonders bei gemeinsamer Verwendung von DM-α-CD und Poly-β-CD reagieren
andere Lipoproteine als LDL kaum. Im Gegensatz dazu wurden bei Messung
in Abwesenheit eines Cyclodextrin-Derivates die Reaktionen von VLDL
und CM überhaupt
nicht unterdrückt,
woraus resultiert, das LDL-Cholesterin
nicht spezifisch gemessen werden kann.
-
Wie vorstehend ausgeführt, kann
bei Messung des Cholesterins in Lipoproteinen in Gegenwart von mindestens
einer Verbindung, die ausgewählt
ist aus der Gruppe, bestehend aus DM-α-CD und Poly-β-CD das Cholesterin
in LDL spezifisch gemessen werden.
-
Beispiel 4 (nicht im Geltungsbereich
der beigefügten
Ansprüche)
-
Unter Verwendung eines Autoanalyzers
vom Typ Hitachi 7170 (hergestellt von Hitachi, Ltd.) wurde zur Untersuchung
des Reaktionsvermögens
von Cholesterin Cholesterin in verschiedenen durch Ultrazentrifugation
fraktionierten Lipoproteinen nach dem Verfahren der vorliegenden
Erfindung gemessen.
-
[Proben]
-
Die gleichen wie in Beispiel 3.
-
[Reagenzien]
-
R-1: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) 4-AA, 1,2 mM;
- (ii) CHE (hergestellt von der Kasei Kogyo K. K.), 1 u/ml, und
- (iii) ein Cyclodextrin-Derivat entsprechend der Angabe in Tabelle
3;
-
R-2: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) COD (hergestellt
von Amano Pharmaceutical Co., Ltd.), 4 u/ml;
- (ii) POD (hergestellt von Toyobo Co., Ltd.), 6 u/ml; und
- (iii) HDAOS, 1,2 mM.
-
[Cyclodextrin-Derivate]
-
Poly-β-CD (hergestellt von der Wako
Pure Chemical Industries, Ltd.)
-
[Messbedingungen]
-
Die gleichen wie in Beispiel 3.
-
[Ergebnisse]
-
Die Umwandlungen der einzelnen Lipoproteine
wurden in der gleichen Weise erhalten, wie in Beispiel 3 beschrieben
wurde.
-
Die Ergebnisse sind in Tabelle 3
gezeigt.
-
-
Wie aus den Ergebnissen von Tabelle
3 klar ersichtlich, wird die Reaktion mit LDL bei Ausführung der Cholesterinmessung
in Gegenwart eines ersten Poly-β-CD und CHE
aufweisenden Reagens insgesamt nicht beeinflusst, während die
Reaktionen mit anderen Lipoproteinen als LDL merklich unterdrückt werden,
woraus resultiert, dass die Ausführung
einer spezifischen Messung von LDL-Cholesterin möglich ist. Im Gegensatz dazu
werden, wenn das erste Reagens lediglich CHE enthält, nicht
nur die Reaktionen mit anderen Lipoproteinen als LDL und speziell
die Reaktionen mit HDL und VLDL kaum unterdrückt, wobei jedoch auch die
Reaktion mit LDL merklich unterdrückt wird, woraus resultiert,
dass Cholesterin in LDL nicht spezifisch gemessen werden kann.
-
Beispiel 5
-
Unter Verwendung eines Autoanalyzers
vom Typ Hitachi 7170 (hergestellt von Hitachi, Ltd.) wurde LDL-Cholesterin
in Serum gemessen.
-
[Proben]
-
8 Proben, die aus frischem Humanserum
erhalten wurden.
-
[Reagenzien]
-
(Reagens 1) [Vergleichsreagens]
-
R-1: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) 4-AA, 1,2 mM,
und
- (ii) Poly-β-CD,
0,13%;
-
R-2: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) COD (hergestellt
von Toyobo Co., Ltd.), 4 u/ml;
- (ii) CHE (hergestellt von Amanu Pharmaceutical Co., Ltd.), 4
u/ml; und
- (iii) POD (hergestellt von Toyobo Co., Ltd.), 6 u/ml,
- (iv) HDAOS, 1,2 mM, und
- (v) Lipomin LA, 0,4%.
-
(Reagens 2)
-
R-1: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) 3-AA, 1,2 mM;
- (ii) CHE (hergestellt von Amano Pharmaceutical Co., Ltd.), 1
u/ml;
- (iii) Poly-β-CD,
0,13%, und
- (iv) Lipomin LA (Warenzeichen für Aminocarbonsäure-Derivat,
hergestellt von Lion Corp.)
-
R-2: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) COD (hergestellt
von Toyobo Co., Ltd.), 4 u/ml;
- (ii) POD (hergestellt von Toyobo Co., Ltd.), 6 u/ml, und
- (iii) HDAOS, 1,2 mM.
-
(Reagens 3)
-
R-1: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) 4-AA, 1,2 mM;
- (ii) Poly-β-CD,
0,13%;
- (iii) CHE (hergestellt von Amano Pharmaceutical Co., Ltd.),
1 u/ml, und
- (iv) Lipomin LA, 0,1%.
-
R-2: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) COD (hergestellt
von Toyobo Co., Ltd.), 4 u/ml;
- (ii) CHE (hergestellt von Amanu Pharmaceutical Co., Ltd.), 4
u/ml;
- (iii) POD (hergestellt von Toyobo Co., Ltd.), 6 u/ml, und
- (iv) HDAOS, 1,2 mM.
-
(Reagens 4) [Vergleichsreagens]
-
R-1: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) 4-AA, 1,2 mM;
- (ii) CHE (hergestellt von Amano Pharmaceutical Co., Ltd.), 1
u/ml, und
- (iii) Lipomin LA, 0,1%.
-
R-2: 25 mM PIPES-NaOH-Puffer (pH
7,2) mit einem Gehalt von:
- (i) COD (hergestellt
von Toyobo Co., Ltd.), 4 u/ml;
- (ii) POD (hergestellt von Toyobo Co., Ltd.), 6 u/ml, und
- (iii) HDAOS, 1,2 mM.
-
[Messbedingungen]
-
Die gleichen wie in Beispiel 3.
-
[Ergebnisse]
-
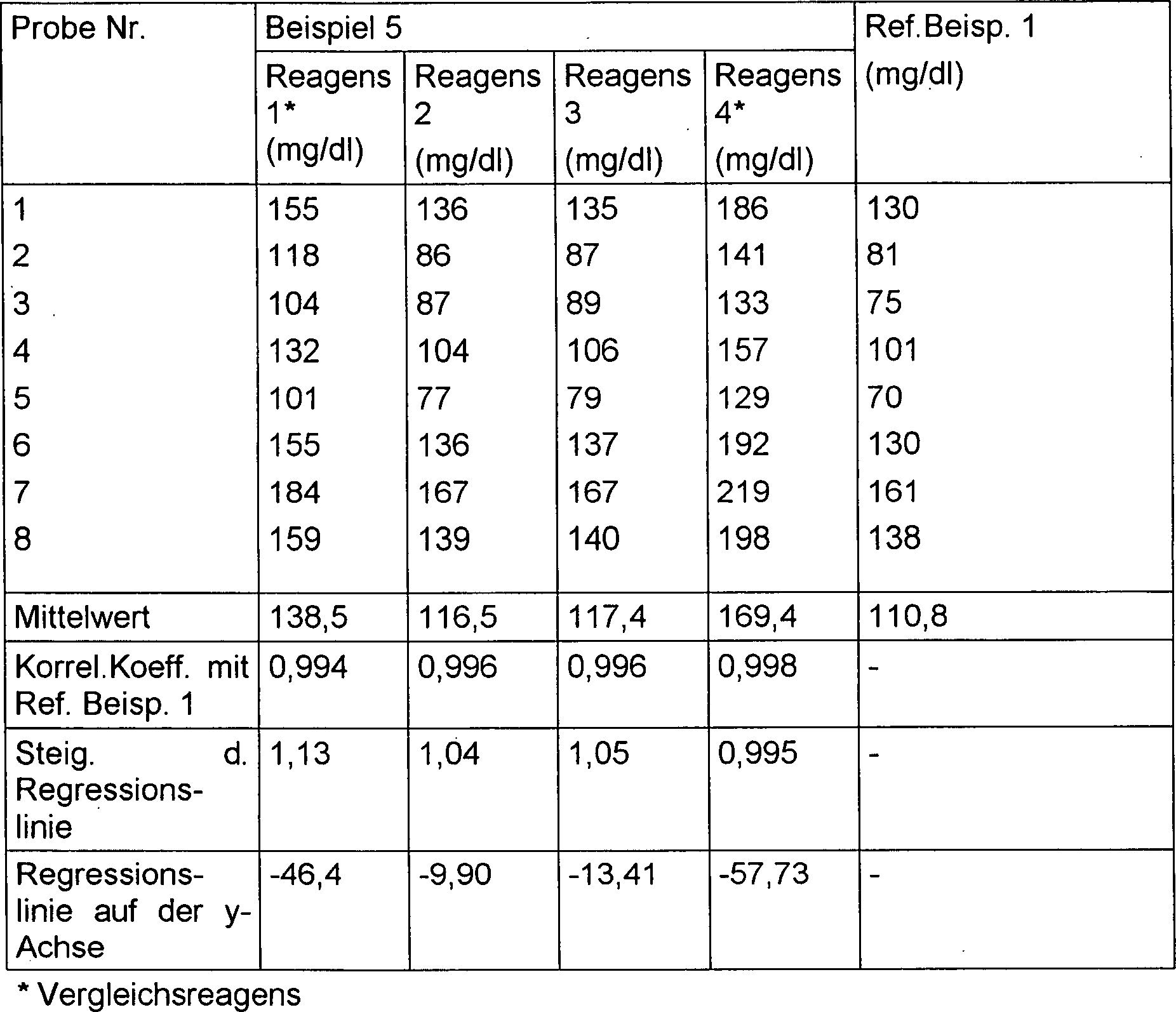
Die Ergebnisse sind in Tabelle 4
gezeigt.
-
Referenzbeispiel 1
-
Wie bei der in Beispiel 5 verwendeten
Serumprobe wurde der Cholesterinwert in LDL mit Hilfe der Friedewald-Gleichung
nach einer konventionellen Methode berechnet.
-
-
Wie aus den in Tabelle 4 gezeigten
Ergebnissen klar ersichtlich ist, liegen die unter Anwendung der Reagenzien,
die Poly-β-CD
(d. h. Reagens 1 bis 3) enthielten, erhaltenen LDL-Cholesterinwerte
nahe den mit Hilfe der konventionellen Friedewald-Gleichung, wie
sie in Referenzbeispiel 1 dargestellt wurde berechneten LDL-Cholesterinwert
im Vergleich zu dem, der unter Verwendung der Reagenzien erhalten
wurde, die kein Poly-β-CD
(d. h. Reagens 4) enthielten. Mit anderen Worten kann das LDL-Cholesterin
spezifisch gemessen werden.
-
Darüber hinaus liegen bei Verwendung
von Poly-β-CD
gemeinsam mit einem Amphotensid und nach Erfordernis mit CHE (Reagens
2 und 3) die erhaltenen LDL-Cholesterinwerte näher an denjenigen, die durch Berechnung
mit der Friedewald-Gleichung erhalten wurden, als dies der Fall
unter Verwendung von Poly-β-CD allein
ist.
-
Beispiel 6
-
Unter Verwendung eines Autoanalyzers
vom Typ Hitachi 7170 (hergestellt von Hitachi, Ltd.) wurde LDL-Cholesterin
in Serum gemessen.
-
[Proben]
-
15 Proben, die aus frischem Humanserum
erhalten wurden.
-
[Reagenzien]
-
R-1: 25 mM 2-Hydroxy-N-tris(hydroxymethyl)-methyl-3-aminopropansulfonsäure (TAPSO)-NaON-Puffer
(pH 7,0) mit einem Gehalt von:
- (i) HDAOS, 0,6
mM;
- (ii) CHE (hergestellt von Amano Pharmaceutical Co., Ltd.), 2
u/ml;
- (iii) Poly-β-CD
(Poly-β-cyclodextrin)
(hergestellt von Wako Pure Chemical Industries, Ltd.), 0,125%;
- (iv) ein Tensid nach Tabelle 5, 0,15%;
-
R-2: 25 mM TAPSO-NaON-Puffer (pH
7,0) mit einem Gehalt von:
- (i) COD (hergestellt
von Toyobo Co., Ltd.), 4 u/ml;
- (ii) POD (hergestellt von Toyobo Co., Ltd.), 10 u/ml,
- (iii) 4-AA, 6 mM.
-
[Tensid]
-
Lipomin LA (Warenzeichen, hergestellt
von der Kao Corp.)
-
EMALEX 712 (Warenzeichen, hergestellt
von der Nihon Emulsion Co., Ltd. ), Polyoxyethylenlaurylether
-
EMALEX 1615 (Warenzeichen, hergestellt
von der Nihon Emulsion Co., Ltd.), Polyoxyethylenhexyldecylether
-
EMALEX NP-20 (Warenzeichen, hergestellt
von der Nihon Emulsion Co., Ltd.), Polyoxyethylennonylphenylether
-
[Messbedingungen]
-
Die gleichen wie in Beispiel 3.
-
[Ergebnisse]
-
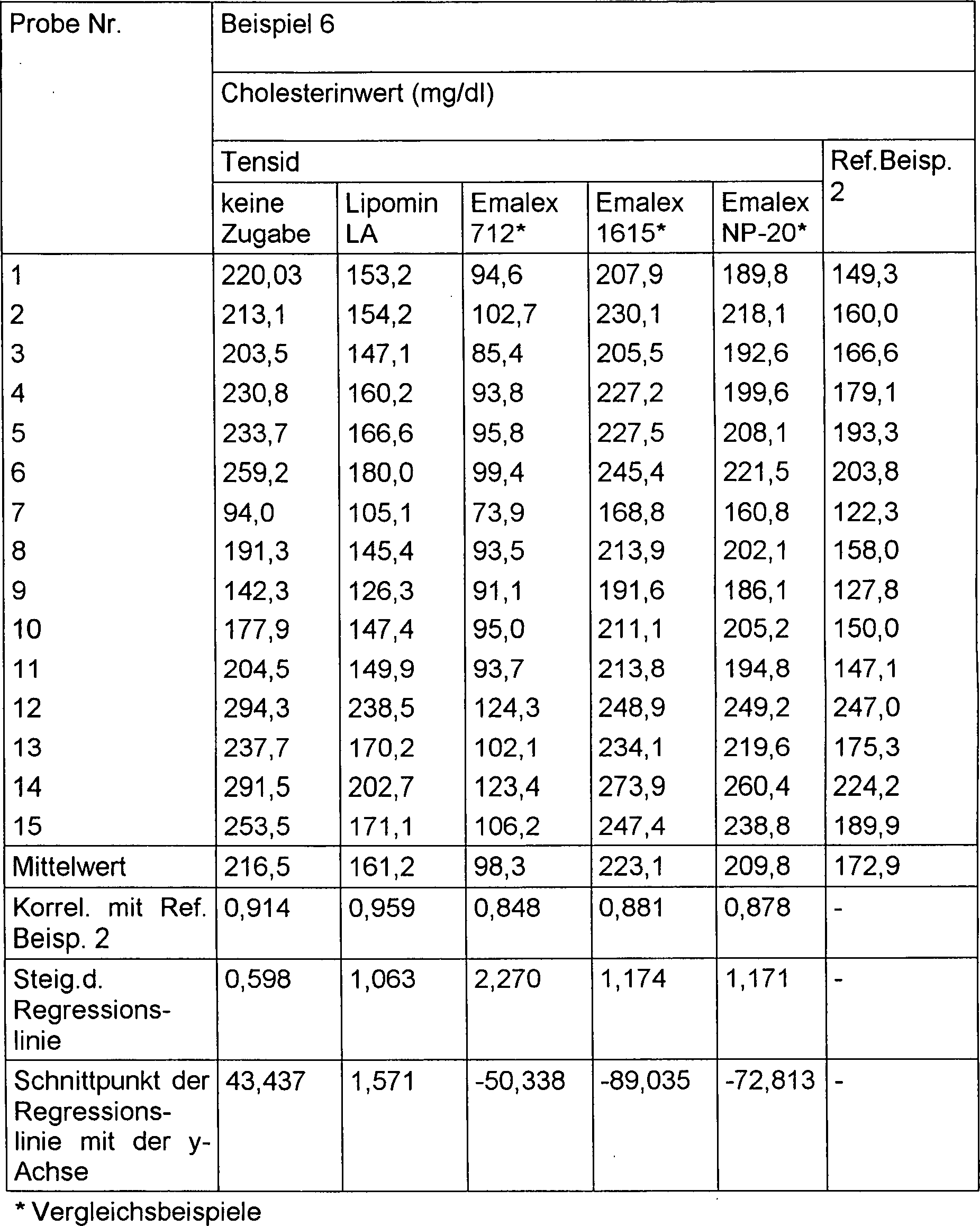
Die Ergebnisse sind in Tabelle 5
gezeigt.
-
Referenzbeispiel 2
-
Wie bei der in Beispiel 5 verwendeten
Serumprobe wurde der Cholesterinwert in LDL mit Hilfe der Friedewald-Gleichung
nach einer konventionellen Methode berechnet.
-
-
Wie aus den in Tabelle 5 gezeigten
Ergebnissen klar ersichtlich ist, liegen die unter Anwendung der Reagenzien
der vorliegenden Erfindung, die Poly-β-CD und Lipomin LA enthalten,
erhaltenen LDL-Cholesterinwerte nahe den mit Hilfe der konventionellen
Friedewald-Gleichung, wie sie in Referenzbeispiel 2 dargestellt wurde
berechneten LDL-Cholesterinwert im Vergleich zu dem, der unter Verwendung
der Reagenzien erhalten wurde, die Poly-β-CD und nicht ionisches Tensid
enthielten. Mit anderen Worten kann das LDL-Cholesterin nach der
vorliegenden Erfindung spezifisch gemessen werden.
-
Wie vorstehend ausgeführt, kann
nach der vorliegenden Erfindung das LDL-Cholesterin in einer Lebendprobe
spezifisch und genau unter Verwendung der speziellen Reagenzien
der vorliegenden Erfindung gemessen werden. Darüber hinaus kann das LDL-Cholesterin
unter Anwendung der vorliegenden Erfindung direkt unter Verwendung
eines Mehrzweckautoanalyzers gemessen werden, was nach Prozessen
des Standes der Technik nicht möglich
war.